- 2021-05-12 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
鲁教版九年级化学第六单元测试题含答案
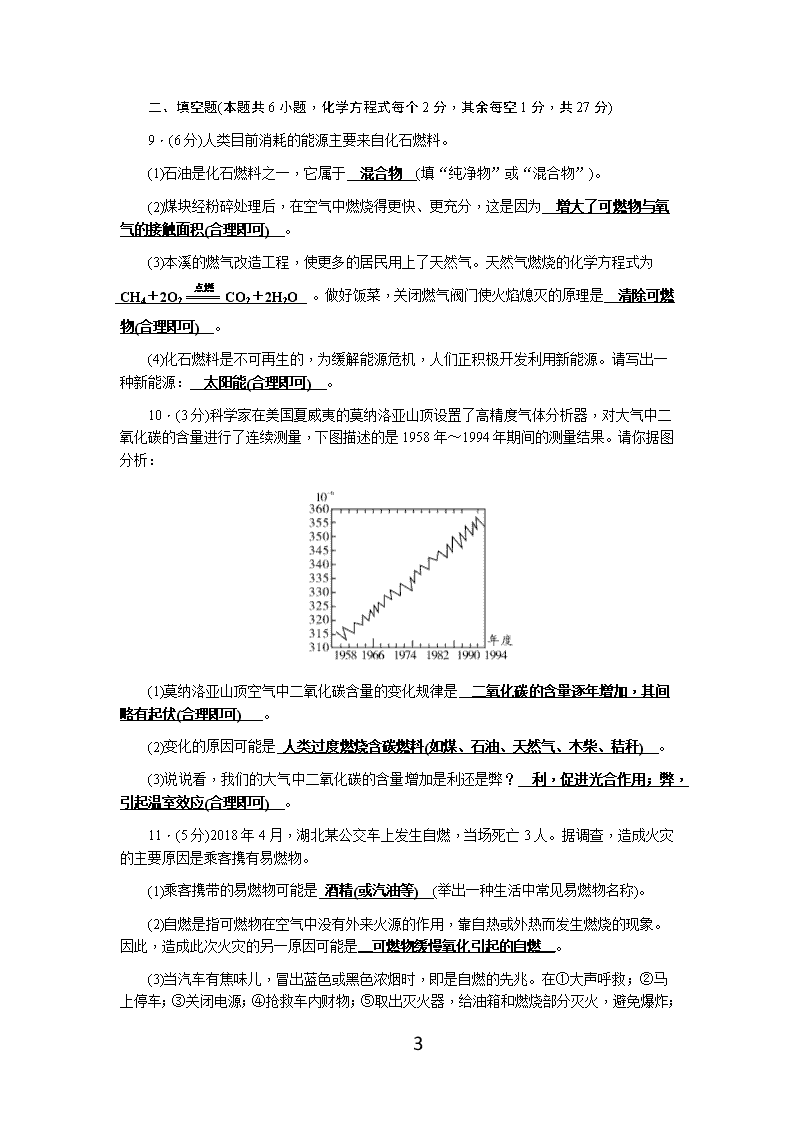
鲁教版九年级化学第六单元测试题含答案 (时间:60分钟 满分:75分) 可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40 第Ⅰ卷 (选择题 24分) 一、选择题(本题共8小题,每小题3分,共24分。每小题只有一个选项符合题意) 1.下列说法中不正确的是( B ) A.燃烧不一定有火焰产生 B.物质跟氧气的反应就是燃烧 C.物质在有限的空间内燃烧,可能会引起爆炸 D.物质燃烧的剧烈程度与氧气的浓度有关 2.(德阳中考)下列有关二氧化碳的说法正确的是( B ) A.实验室常用块状石灰石和稀硫酸反应制取二氧化碳气体 B.二氧化碳用于灭火,既利用了它的物理性质也利用了它的化学性质 C.将二氧化碳气体通入紫色石蕊试液中,试液呈红色,说明二氧化碳能使石蕊试液变红色 D.将燃着的木条伸入一瓶气体中,木条立即熄灭,证明瓶内原有气体是二氧化碳 3.打火机给人们带来了方便,图示是普通电子打火机的实物照片。下面可以做到符合燃烧条件能打火的组合是( A ) A.①③⑤ B.①③④ C.①②③ D.①②④ 4.下列措施不能考虑用于油井灭火的是( C ) A.设法使着火的油井与空气隔绝 B.设法阻止石油的喷射 7 C.设法降低石油的着火点 D.设法降低油井井口的温度 5.2015年3月9日,太阳能飞机“阳光动力2号”开始环球飞行,并在名古屋和夏威夷之间创下了118小时不间断飞行的记录,下列有关能源和环保的说法错误的是( C ) A.“阳光动力2号”所用太阳能是绿色环保新能源 B.煤、石油、天然气等化石燃料是不可再生能源 C.煤完全燃烧后就不会对环境造成污染 D.可燃冰具有能量高、燃烧热值大等优点,其主要成分是CH4 6.“归纳与比较”是化学学习的主要方法,下列关于CO2和CO的不同点比较错误的是( C ) A.组成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子 B.性质:CO2能溶于水,并能与水反应;CO难溶于水,但能燃烧 C.用途:CO2可用于光合作用、灭火等;CO可作气体燃料,还可用于人工降雨 D.危害:CO2会造成“温室效应”;CO易与血液中的血红蛋白结合引起中毒 7.“节能减排、低碳生活”的主题旨在倡导节约能源和利用清洁能源,减少温室气体二氧化碳的排放。下列措施中不符合该主题的是( C ) A.广泛使用太阳能和风能等清洁能源 B.回收利用废旧金属 C.多使用一次性筷子 D.减少使用私家车次数,多乘公交车或骑自行车 8.下列有关图象中不正确的是( D ) 第Ⅱ卷 (非选择题 51分) 7 二、填空题(本题共6小题,化学方程式每个2分,其余每空1分,共27分) 9.(6分)人类目前消耗的能源主要来自化石燃料。 (1)石油是化石燃料之一,它属于 混合物 (填“纯净物”或“混合物”)。 (2)煤块经粉碎处理后,在空气中燃烧得更快、更充分,这是因为 增大了可燃物与氧气的接触面积(合理即可) 。 (3)本溪的燃气改造工程,使更多的居民用上了天然气。天然气燃烧的化学方程式为 CH4+2O2CO2+2H2O 。做好饭菜,关闭燃气阀门使火焰熄灭的原理是 清除可燃物(合理即可) 。 (4)化石燃料是不可再生的,为缓解能源危机,人们正积极开发利用新能源。请写出一种新能源: 太阳能(合理即可) 。 10.(3分)科学家在美国夏威夷的莫纳洛亚山顶设置了高精度气体分析器,对大气中二氧化碳的含量进行了连续测量,下图描述的是1958年~1994年期间的测量结果。请你据图分析: (1)莫纳洛亚山顶空气中二氧化碳含量的变化规律是 二氧化碳的含量逐年增加,其间略有起伏(合理即可) 。 (2)变化的原因可能是 人类过度燃烧含碳燃料(如煤、石油、天然气、木柴、秸秆) 。 (3)说说看,我们的大气中二氧化碳的含量增加是利还是弊? 利,促进光合作用;弊,引起温室效应(合理即可) 。 11.(5分)2018年4月,湖北某公交车上发生自燃,当场死亡3人。据调查,造成火灾的主要原因是乘客携有易燃物。 (1)乘客携带的易燃物可能是 酒精(或汽油等) (举出一种生活中常见易燃物名称)。 (2)自燃是指可燃物在空气中没有外来火源的作用,靠自热或外热而发生燃烧的现象。因此,造成此次火灾的另一原因可能是__可燃物缓慢氧化引起的自燃__。 (3)当汽车有焦味儿,冒出蓝色或黑色浓烟时,即是自燃的先兆。在①大声呼救;②马上停车;③关闭电源;④抢救车内财物;⑤取出灭火器,给油箱和燃烧部分灭火,避免爆炸; 7 ⑥尽快远离现场逃生等项措施中,你认为司机此时最应该做的三件事是 ②③⑤ (填序号)。 (4)灭火器是必须随车携带的装备,则车用灭火器最好使用 干粉 (填“水基型”或“干粉”)灭火器。 (5)灾难发生后,最重要的是生命安全。若乘车人员衣服被火烧着,可 用水泼灭或尽快脱掉着火衣服或就地打滚等 。 12.(3分)大气是大自然对人类的恩赐,与人类的生存休戚相关。 (1)大量化石燃料的燃烧会造成较多污染物的排放,这不仅污染大气,还是形成 酸雨的主要原因。 (2)“节能减排”是我国的重要国策,过多的CO2排放会造成 温室 效应,为了减缓大气中CO2含量的增加,目前以下建议可行的是 A (填字母序号)。 A.开发太阳能、水能、风能、地热能等新能源 B.电解水生产清洁燃料氢气 C.禁止使用煤、石油、天然气等化石燃料 D.开发燃煤新技术使其充分燃烧 13.(4分)某化学兴趣小组用如图所示的装置做有关CO2气体的实验: (1)甲同学将收集满CO2气体的试管倒插入紫色石蕊溶液中(如图A所示),并轻轻振荡试管。 ①描述产生的现象: 试管内液面上升,溶液变成红色 ; ②写出反应的化学方程式: H2O+CO2===H2CO3 。 (2)乙同学将挤压图B所示装置中滴管的胶头,使其中的Ca(OH)2溶液滴入烧瓶,并轻轻振荡,发现系在导管一端的气球慢慢胀大,产生这一现象的原因是: CO2与Ca(OH)2反应,使瓶内气压小于外界大气压,外界空气进入气球使其胀大 。 14.(6分)已知A、E、F是单质,B、C、D是化合物,它们分别是由碳、氢、氧三种元素中的一种或者几种组成。其中B是相对分子质量最小的氧化物,D物质很不稳定,容易分解生成B和C,它们之间的转化关系如图所示。 7 (1)A、E的化学式为A: O2 ,E: H2 。 (2)请你写出以下变化的化学方程式。 A+F→C O2+CCO2 ; D→B+C H2CO3H2O+CO2↑ 。 三、实验与探究题(本题共2小题,化学方程式每个2分,其余每空1分,共17分) 15.(9分)(苏州中考)实验室常用块状大理石和稀盐酸制取CO2气体。 (1)写出实验室制取CO2的化学方程式: CaCO3+2HCl===CaCl2+H2O+CO2↑ 。 (2)若用如图所示装置(固定装置省略)制CO2。连接好装置后,需检查装置气密性。具体操作方法是:先 B (填字母,下同),后 A ,若导管口有气泡,放手后导管内上升一段稳定的水柱,则气密性良好。 A.用手捂住试管 B.将导管一端浸入水中 (3)实验室收集CO2可用的方法是 C (填字母)。 A.排水法 B.向下排空气法 C.向上排空气法 (4)实验室常用澄清石灰水检验CO2,写出反应的化学方程式: CO2+Ca(OH)2 ===CaCO3↓+H2O 。 (5)某些大理石中含少量硫化物,使制得的CO2中混有H2S气体。欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下: 查阅资料:Ⅰ.H2S能与NaOH等碱溶液、CuSO4溶液反应。 Ⅱ.CO2中混有的HCl气体可用饱和NaHCO3溶液吸收。 ①装置甲中所盛试剂应选用 D (填字母)。 A.浓硫酸 B.NaOH溶液 C.澄清石灰水 D.CuSO4溶液 ②装置丙的作用是 除去CO2中的水蒸气或干燥CO2。 7 16.(8分)下面是两个探究可燃物燃烧条件的实验,请回答相关问题。 (1)写出标有编号的仪器名称:① 分液漏斗 ,② 锥形瓶 。 (2)如图(1)向C中加入少量白磷,再加入热水,塞好胶塞,使导管口浸入热水中,白磷不燃烧。打开K1,将A中溶液滴入B中,C中有气泡冒出,白磷燃烧。C中发生反应的化学方程式为 4P+5O22P2O5 。此实验运用 对比 的方法研究了燃烧的一个条件,它是 燃烧需要氧气 。 (3)如图(2)所示,在空气中放置时,两团棉花均不燃烧;若将足量二氧化碳倒入烧杯时,可以观察到的现象有:① 蜡烛熄灭 ;②粘有过氧化钠的棉花燃烧;③未粘有过氧化钠的棉花不燃烧。 通过上述实验的对比分析,写出产生现象②的原因: 反应产生热量,有氧气生成 。 四、计算题(本题共1小题,共7分) 17.小英同学为了测定某地区石灰石样品中碳酸钙的质量分数,取该样品15 g,现将75 mL的稀盐酸分三次加入石灰石样品中,每次充分反应后测得生成气体的质量,实验数据如下表: 实验 第一次 第二次 第三次 加入稀盐酸的量/mL 25 25 25 生成气体的质量/g 2.2 m 1.1 试求: (1)m的值是 2.2 。 (2)求该样品中碳酸钙的质量分数。(保留一位小数) 解:由题意可知,产生CO2气体的总质量为:2.2 g+2.2 g+1.1 g=5.5 g。 设样品中碳酸钙的质量为x。 CaCO3+2HCl===CaCl2+H2O+CO2↑ 100 44 x 5.5 g 7 = x=12.5 g 样品中碳酸钙的质量分数=×100%≈83.3% 答:样品中碳酸钙的质量分数为83.3%。 7查看更多