- 2021-02-26 发布 |
- 37.5 KB |
- 3页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
(新课标)广西2020高考化学二轮复习 题型八 化学实验基础专项练
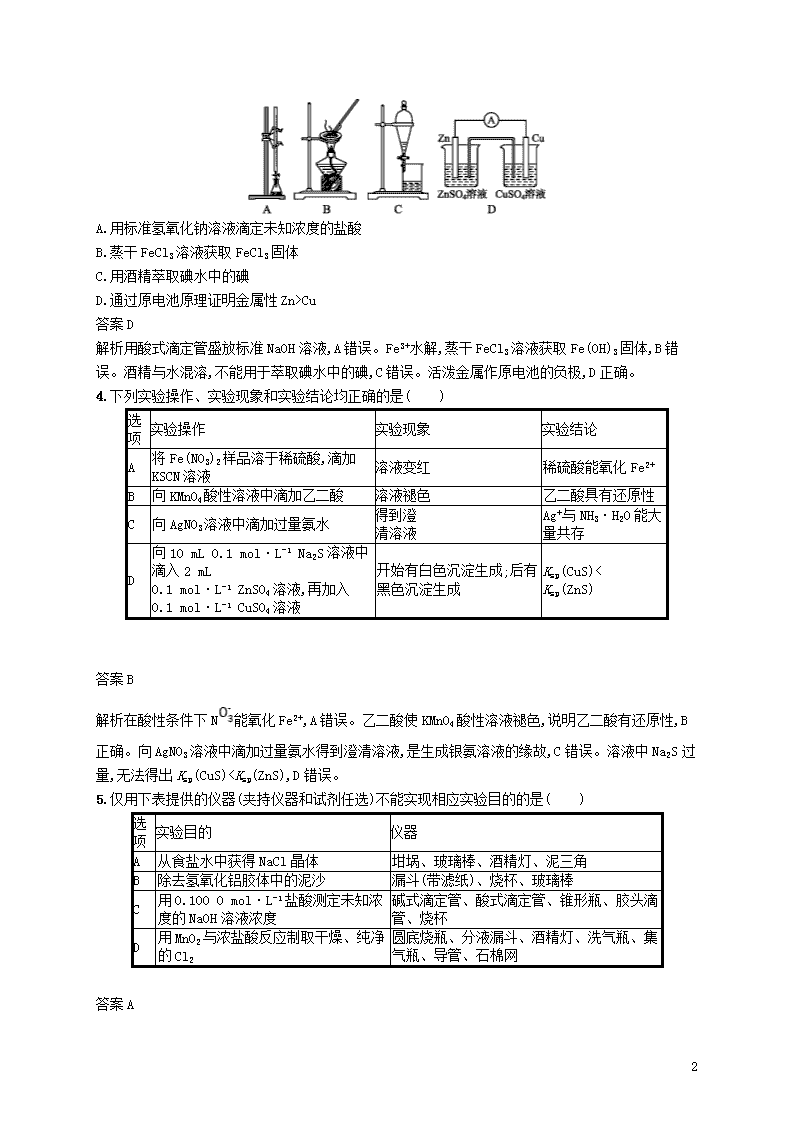
题型八 化学实验基础 1.(2018全国Ⅱ,13)下列实验过程可以达到实验目的的是( ) 编号 实验目的 实验过程 A 配制0.400 0 mol·L-1的 NaOH溶液 称取4.0 g固体NaOH于烧杯中,加入少量蒸馏水溶解,转移至250 mL 容量瓶中定容 B 探究维生素C的还原性 向盛有2 mL黄色氯化铁溶液的试管中滴加浓的维生素C溶液,观察颜色变化 C 制取并纯化氢气 向稀盐酸中加入锌粒,将生成的气体依次通过NaOH溶液、浓硫酸和KMnO4溶液 D 探究浓度对反应速率的影响 向2支盛有5 mL不同浓度NaHSO3溶液的试管中同时加入2 mL 5% H2O2溶液,观察实验现象 答案B 解析转移溶液后应用适量的蒸馏水洗涤烧杯内壁和玻璃棒2~3次,并将洗涤液转入容量瓶后再定容,A项错误;维生素C具有还原性,与Fe3+反应,溶液由棕黄色变为浅绿色,B项正确;用盐酸和Zn粒反应制取的氢气中混有氯化氢气体和水蒸气,先用氢氧化钠溶液除去氯化氢,然后用KMnO4溶液检验氯化氢是否除尽,最后用浓硫酸干燥,若先用浓硫酸干燥,最后用KMnO4溶液检验氯化氢是否除尽,又会重新带入水蒸气,达不到干燥的目的,C项错误;亚硫酸氢钠和过氧化氢反应生成硫酸氢钠和水,无明显现象,D项错误。 2.下列有关实验操作、现象和解释或结论都正确的是( ) 选项 操作 现象 解释或结论 A 在KSCN与FeCl3的混合液中再加入KCl固体 溶液颜色变浅 增大Cl-浓度,平衡逆向移动 B 将氯化铝溶液蒸干 析出白色固体 白色固体是氯化铝 C 向某溶液中滴加NaOH溶液,将湿润红色石蕊试纸置于试管口 试纸不变蓝 原溶液中无N D 石蕊溶液中通入氯气 溶液先变红后红色褪去 氯气与水反应产生了酸和具有漂白性的物质 答案D 解析加入KCl固体,平衡不移动,溶液颜色基本不变,A错误。氯化铝水解生成的氯化氢容易挥发,溶液蒸干后得到氢氧化铝,B错误。向某溶液中滴加NaOH溶液,生成的氨气极易溶于水生成一水合氨,因此将湿润红色石蕊试纸置于试管口,试纸不变蓝,C错误。氯气与水反应生成的次氯酸具有强氧化性,加入石蕊溶液,溶液先变红后红色褪去,D正确。 3.用下列实验装置进行相应实验,能达到实验目的的是( ) 3 A.用标准氢氧化钠溶液滴定未知浓度的盐酸 B.蒸干FeCl3溶液获取FeCl3固体 C.用酒精萃取碘水中的碘 D.通过原电池原理证明金属性Zn>Cu 答案D 解析用酸式滴定管盛放标准NaOH溶液,A错误。Fe3+水解,蒸干FeCl3溶液获取Fe(OH)3固体,B错误。酒精与水混溶,不能用于萃取碘水中的碘,C错误。活泼金属作原电池的负极,D正确。 4.下列实验操作、实验现象和实验结论均正确的是( ) 选项 实验操作 实验现象 实验结论 A 将Fe(NO3)2样品溶于稀硫酸,滴加KSCN溶液 溶液变红 稀硫酸能氧化Fe2+ B 向KMnO4酸性溶液中滴加乙二酸 溶液褪色 乙二酸具有还原性 C 向AgNO3溶液中滴加过量氨水 得到澄 清溶液 Ag+与NH3·H2O能大量共存 D 向10 mL 0.1 mol·L-1 Na2S溶液中滴入2 mL 0.1 mol·L-1 ZnSO4溶液,再加入0.1 mol·L-1 CuSO4溶液 开始有白色沉淀生成;后有黑色沉淀生成 Ksp(CuS)< Ksp(ZnS) 答案B 解析在酸性条件下N能氧化Fe2+,A错误。乙二酸使KMnO4酸性溶液褪色,说明乙二酸有还原性,B正确。向AgNO3溶液中滴加过量氨水得到澄清溶液,是生成银氨溶液的缘故,C错误。溶液中Na2S过量,无法得出Ksp(CuS)查看更多