- 2021-05-12 发布 |
- 37.5 KB |
- 4页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
高考化学专题复习练习卷原电池的工作原理及应用练习卷
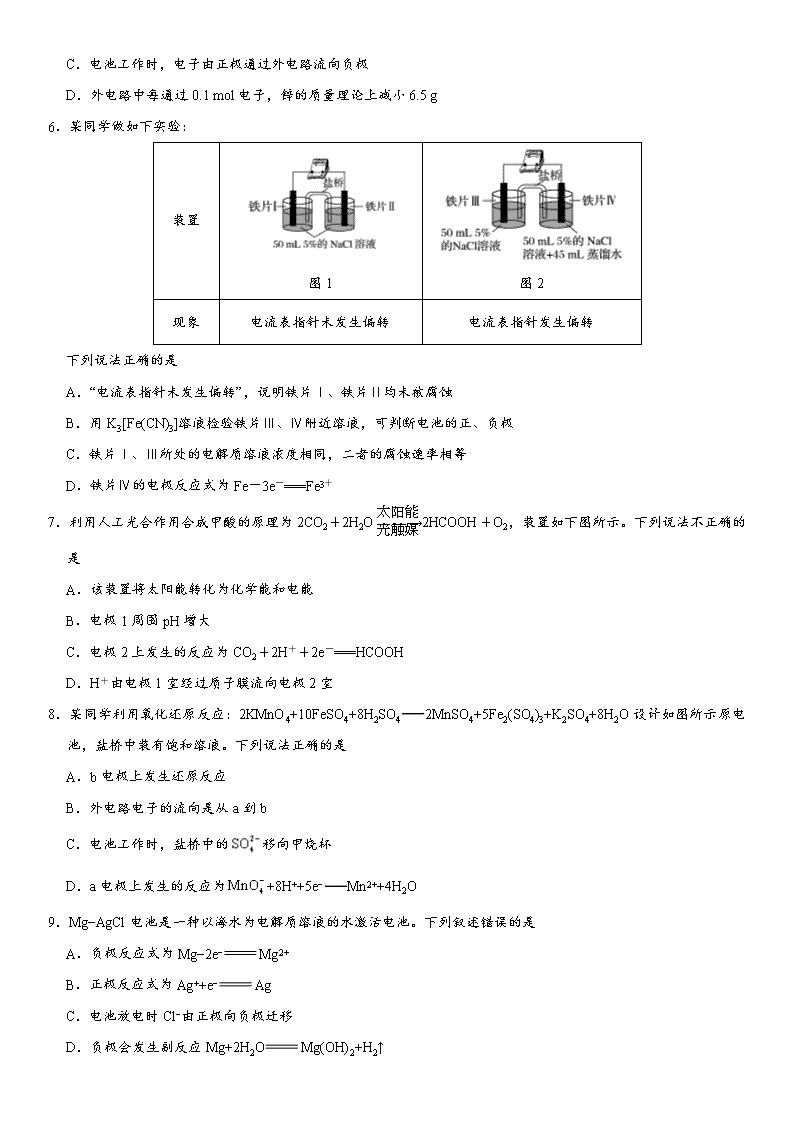
原电池的工作原理及应用练习卷 1.某原电池装置如图所示。下列有关叙述中正确的是 (盐桥中装有含琼胶的KCl饱和溶液) A.Fe作正极,发生氧化反应 B.负极反应:2H++2e-===H2↑ C.工作一段时间后,两烧杯中溶液pH均不变 D.工作一段时间后,NaCl溶液中c(Cl-)增大 2.实验发现,298 K时,在FeCl3酸性溶液中加少量锌粒后,Fe3+立即被还原成Fe2+。某夏令营兴趣小组根据该实验事实设计了如图所示原电池装置。下列有关说法正确的是 A.该原电池的正极反应是Zn-2e-===Zn2+ B.左烧杯中溶液的红色逐渐褪去 C.该电池铂电极上有气泡出现 D.该电池总反应为3Zn+2Fe3+===2Fe+3Zn2+ 3.有A、B、C、D、E五块金属片,进行如下实验:①A、B用导线相连后,同时浸入稀硫酸中,A极为负极;②C、D用导线相连后,同时浸入稀硫酸中,电流由D→导线→C;③A、C用导线相连后,同时浸入稀硫酸中,C极产生大量气泡;④B、D用导线相连后,同时浸入稀硫酸中,D极发生氧化反应;⑤用惰性电极电解含B离子和E离子的溶液,E先析出。据此判断五种金属的活动性顺序是 A. A>B>C>D>E B. A>C>D>B>E C. C>A>B>D>E D. B>D>C>A>E 4.如图所示,杠杆AB两端分别挂有大小相同、质量相等的空心铜球和空心铁球,调节杠杆并使其在水中保持平衡,然后小心地向水槽中分别滴入CuSO4浓溶液和FeSO4浓溶液。一段时间后,下列有关杠杆的偏向判断正确的是(实验过程中,不考虑两球的浮力变化) A.杠杆为导体或绝缘体时,均为A端高B端低 B.杠杆为导体或绝缘体时,均为A端低B端高 C.当杠杆为导体时,A端低B端高 D.当杠杆为导体时,A端高B端低 5.普通锌锰干电池的简图(如图所示),它是用锌皮制成的锌筒作电极兼作容器,中央插一根碳棒,碳棒顶端加一铜帽。在石墨碳棒周围填满二氧化锰和炭黑的混合物,并用离子可以通过的长纤维纸包裹作隔膜,隔膜外是用氯化锌、氯化铵和淀粉等调成糊状作电解质溶液;该电池工作时的总反应为Zn+2+2MnO2[Zn(NH3)2]2++Mn2O3+H2O 关于锌锰干电池的下列说法中正确的是 A.当该电池电压逐渐下降后,利用电解原理能重新充电复原 B.电池正极的电极反应式为2MnO2+2+2e−Mn2O3+2NH3+H2O C.电池工作时,电子由正极通过外电路流向负极 D.外电路中每通过0.1 mol电子,锌的质量理论上减小6.5 g 6.某同学做如下实验: 装置 图1 图2 现象 电流表指针未发生偏转 电流表指针发生偏转 下列说法正确的是 A.“电流表指针未发生偏转”,说明铁片Ⅰ、铁片Ⅱ均未被腐蚀 B.用K3[Fe(CN)3]溶液检验铁片Ⅲ、Ⅳ附近溶液,可判断电池的正、负极 C.铁片Ⅰ、Ⅲ所处的电解质溶液浓度相同,二者的腐蚀速率相等 D.铁片Ⅳ的电极反应式为Fe-3e-===Fe3+ 7.利用人工光合作用合成甲酸的原理为2CO2+2H2O2HCOOH+O2,装置如下图所示。下列说法不正确的是 A.该装置将太阳能转化为化学能和电能 B.电极1周围pH增大 C.电极2上发生的反应为CO2+2H++2e-===HCOOH D.H+由电极1室经过质子膜流向电极2室 8.某同学利用氧化还原反应:2KMnO4+10FeSO4+8H2SO42MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如图所示原电池,盐桥中装有饱和溶液。下列说法正确的是 A.b电极上发生还原反应 B.外电路电子的流向是从a到b C.电池工作时,盐桥中的移向甲烧杯 D.a电极上发生的反应为+8H++5e−Mn2++4H2O 9.Mg−AgCl电池是一种以海水为电解质溶液的水激活电池。下列叙述错误的是 A.负极反应式为Mg−2e−Mg2+ B.正极反应式为Ag++e−Ag C.电池放电时Cl−由正极向负极迁移 D.负极会发生副反应Mg+2H2OMg(OH)2+H2↑ 10.某电池以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液。下列说法正确的是 A.Zn为电池的负极 B.正极反应式为2FeO42−+ 10H++6e−Fe2O3+5H2O C.该电池放电过程中电解质溶液浓度不变 D.电池工作时向负极迁移 11.图1是铜锌原电池示意图。图2中,x轴表示实验时流入正极的电子的物质的量,y轴表示 A.铜棒的质量 B.c(Zn2+) C.c(H+) D.c(SO42−) 12.锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过。下列有关叙述正确的是 A.铜电极上发生氧化反应 B.电池工作一段时间后,甲池的c()减小 C.电池工作一段时间后,乙池溶液的总质量增加 D.阴阳离子分别通过交换膜向负极和正极移动,保持溶液中电荷平衡 13.某实验小组同学用电化学原理模拟湿法炼钢,进行了一系列探究活动。 (1)如图(Ⅰ)为某实验小组设计的原电池装置,盐桥内装载足量的用饱和氯化钾溶液浸泡的琼脂,反应前,电极质量相等,一段时间后,两电极质量相差6.00 g,则导线中通过了 mol电子,若不考虑甲、乙两池电解质溶液中的离子向盐桥中移动,则甲、乙两池电解质溶液的总质量与实验开始前的电解质溶液的总质量相差 g。 学#科网 (2)其他条件不变,若将盐桥换成光亮的U形弯铜丝浸入甲池与乙池,如图(Ⅱ)所示,电流计指针偏转方向与先前一样,但偏转角度明显减小。一段时间后,乙池石墨棒浸入液面以下部分也析出了一层紫红色固体,则甲池铜丝附近溶液的pH (填“减小”“增大”或“不变”),乙池中石墨为 (填“正”“负”“阴”或“阳”)极。 参考答案 1.【答案】D 2.【答案】B 3.【答案】B 4.【答案】C 5.【答案】B 6.【答案】B 7.【答案】B 8.【答案】D 9.【答案】B 10.【答案】AD 11.【答案】C 12.【答案】C 13.【答案】(1)0.1 7.05 (2)增大 阴查看更多