江西省景德镇一中2021届高三8月月考化学试题 Word版含答案
景德镇一中2021届高三8月月考化学试卷
可能用到的相对原子质量:H-1 C-12 O-16 Zn-65
一、单项选择题(本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是最符合题意)
1.化学无处不在,下列说法错误的是( )
A. 《元丰行示德逢》里“雷蟠电掣云滔滔,夜半载雨输亭皋”涉及化学反应N2+O22NO
B. 根据化学学科核心素养之一(证据推理与模型认知)可推知Cr(OH)3胶体也可吸附悬浮杂质
C. 纳米铁粉可以高效地去除污水中的重金属离子是因为其具有较强的还原性
D. 二氧化硅广泛用于制作光导纤维,光导纤维遇强酸强碱都会“断路”
2.阿伏加德罗常数的值为NA。下列说法正确的是( )
A. 23gC2H6O含C-H键数目一定为3NA B. 标准状况下,22.4LCH3Cl含氢原子数目为3NA
C. 1mol·L-1NH4Fe(SO4)2溶液中NH4+数目小于NA
D. 电解法精炼铜时,阳极溶解32g,转移电子数一定为NA
3.我清代《本草纲目拾遗》中记载药物“鼻冲水”写道:“贮以玻璃瓶,紧塞其口,勿使泄气,则药力不减,气甚辛烈,触人脑,非有病不可嗅……虚弱者忌之。宜外用,勿服”。“鼻冲水”的主要成分可能是( )
A. 醋 B. 氢氟酸 C. 氨水 D. 稀硫酸
4.某研究小组探究石蜡油裂解产物,设计如图实验。下列说法正确的是( )
A.本实验能证明其产物含有碳碳不饱和键
B.两支试管中发生的反应类型相同
C.可观察到B和C试管中液体褪色和分层
D.实验完毕后先熄灭酒精灯后拆导管
5.下列物质能实现“”转化关系的是( )
A. Al B. FeO C. NaHCO3 D. NH3
6.如图是中学化学中常见的有机物转化关系,A可以提供生命活动所需要的能量,D是石油裂解气的主要成分,E
- 8 -
可以发生银镜反应,F的相对分子质量为60,且分子中碳元素的质量分数为40%,下列说法错误的是( )
A. D→E的化学方程式:2CH2=CH2+O22CH3CHO
B. A的分子式C6H12O6 C. ①的反应类型为水解反应
D. 与B含有相同官能团的同分异构体有2种
7.向恒温恒容密闭容器中充入1molX和2molY,发生反应4X(g)+2Y(g)⇌3Z(g),下列选项表明反应一定已达平衡状态的是( )
A. 气体密度不再变化 B. Y的体积分数不再变化
C. 3v(X)=4v(Z) D. 容器内气体的浓度c(X):c(Y):c(Z)=4:2:3
8.下列离子方程式书写正确的是( )
A. NaHSO4溶液中加Ba(OH)2溶液至中性:Ba2++OH-+H++SO===BaSO4↓+H2O
B. 往NH4HCO3溶液中加过量NaOH溶液并加热:NH+OH-===NH3↑+H2O
C. 往酸性碘化钾溶液中滴加适量的双氧水:2I-+2H++H2O2===I2+2H2O
D. 金属钠和水反应:Na+2H2O===Na++2OH-+H2↑
9. SO2是大气污染物,造成酸雨的主要原因,用如图所示装置可以既吸收工厂排放的废气中的SO2,又可以生成一定量的硫酸,下列说法正确的是( )
A. a为正极,b为负极 B. 生产过程中氢离子由右移向左
C. 从左下口流出的硫酸的质量分数一定大于50%
D. 负极反应式为SO2+2H2O-2e-=SO42-+4H+
10. 如图所示,a和b是盐酸和氢氧化钠溶液相互反应的pH值变化曲线,下列说法不正确的是( )
A. NaOH的物质的量浓度:c(NaOH)=0.1mol·L-1
B. a和b曲线上的任何一点都有:c(Na+)+c(H+)=c(Cl-)+c(OH-)
C. P点溶液中:c(Na+)=c(Cl-)>c(H+)=c(OH-)
D. 曲线b是氢氧化钠溶液中逐滴加入盐酸的pH值变化曲线
11. 常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. 含大量Fe3+的溶液中:Na+、Mg2+、SO42—、SCN—
B. =106的溶液中:NH4+、K+、AlO2—、NO3—
- 8 -
C. 能使甲基橙变红的溶液中:Cu2+、Mg2+、SO42—、Cl—
D. 1.0 mol·L—1的KNO3溶液中:Fe2+、H+、Cl—、I—
12. 短周期主族元素W、X、Y、Z的原子序数依次增加,K、L、M均是由这些元素组成的二元化合物,甲、乙分别是元素X、Y的单质,甲是常见的固体,乙是常见的气体。K是无色气体,是主要的大气污染物之一,0.05mol/L丙溶液的pH为l,上述物质的转化关系如图所示。下列说法正确的是( )
A. 原子半径:W
Y>X
C. 化合物XYZ中只含共价键 D. K、L、M中沸点最高的是M
13.下列有机物分子中所有原子一定不在同一平面内的是( )
A.乙烯 B.苯乙烯() C.异戊烷 D.氯乙烯(CH2===CHCl)
14.分子式为C9H10O2的有机物,其结构中含有苯环且可以与饱和NaHCO3溶液反应放出气体的同分异构体(不考虑立体异构)有( )
A.12种 B.13种 C.14种 D.15种
二、非选择题
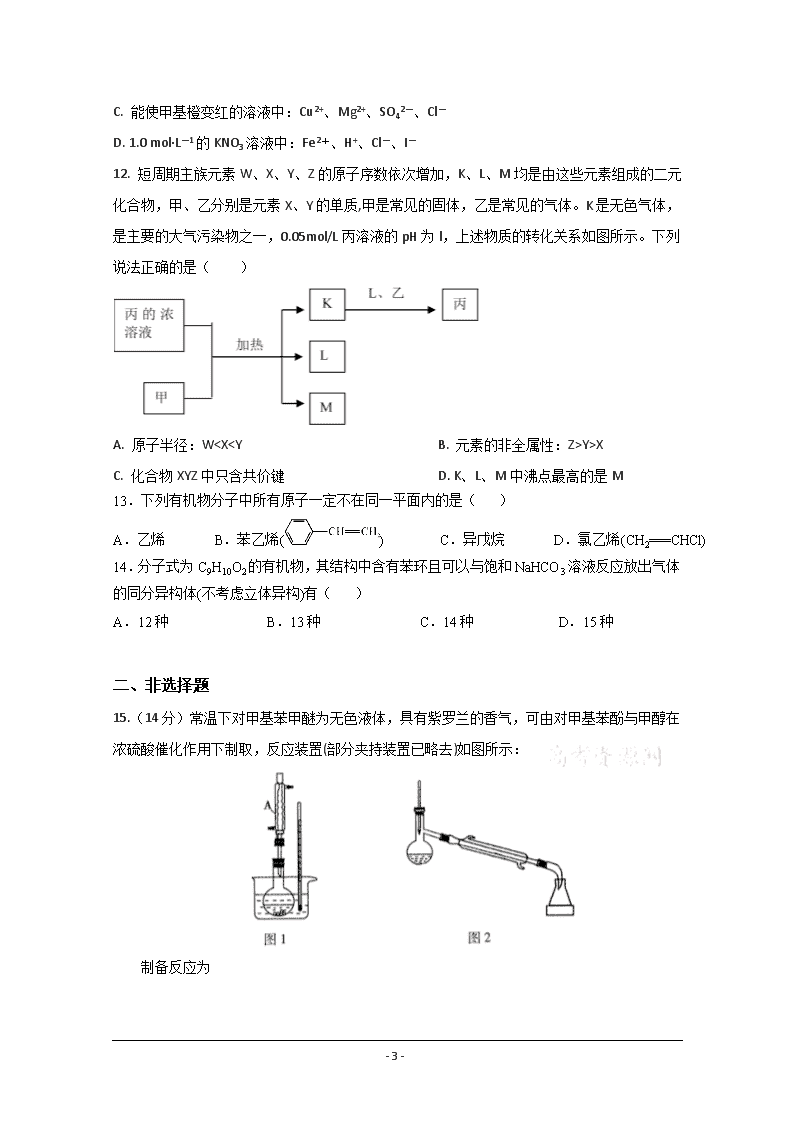
15.(14分)常温下对甲基苯甲醚为无色液体,具有紫罗兰的香气,可由对甲基苯酚与甲醇在浓硫酸催化作用下制取,反应装置(部分夹持装置已略去)如图所示:
制备反应为+CH3OH
- 8 -
+H2O。可能用到的数据如下:
Ⅰ.合成反应:在图1的烧瓶中先加入几片碎瓷片,再依次加入10.8g对甲基苯酚、10mL甲醇,最后加入2mL浓硫酸,控制反应温度为60℃(水浴加热)进行反应。
Ⅱ.产物提纯:①将反应混合液冷却后加入足量饱和碳酸钠溶液,充分反应后转移至分液漏斗中,静置分液;②将有机层转移至图2烧瓶中,加热,控制温度为100℃进行蒸馏,待蒸馏结束后,向烧瓶内剩余液体中加入足量无水氯化钙,然后趁热过滤,并将所得液体再次进行蒸馏,收集177℃左右馏分,蒸馏结束后,称量所得馏分为7.32g。
回答下列问题:
(1)仪器A的名称为__。
(2)向图1的烧瓶中加入碎瓷片的目的是__;采用水浴加热的目的是__。
(3)产物提纯时,向反应混合液中加入足量饱和碳酸钠溶液的作用是__;产物提纯时,先控制温度为100℃进行蒸馏的目的是__。
(4)加入足量无水氯化钙的目的是__。
(5)收集到的177℃左右的馏分主要是__(填名称)。
(6)对甲基苯甲醚的产率为__。
16.(15分).纳米氧化锌是一种多功能性的新型无机材料,在橡胶、玻璃、涂料等各个领域广泛的应用。工业由粗氧化锌(含少量FeO、CuO 等杂质) 制备活性氧化锌的工业流程如下:
已知:Fe3+、Fe2+、Cu2+完全沉淀的pH分别是:3.2,8.1,6.7
- 8 -
(1)“酸浸”时用的硫酸溶液的密度为1.4g/mL,质量分数为70%,则该硫酸的物质的量浓度为____。
(2)焙烧前粉碎的目的是____________________________________________。
(3)滤液中加锌粉的目的是_____________________________________。
(4)物质A的主要成分_______________(填化学式),检验A中阳离子的方法是_______________。
(5)滤液中加H2O2发生反应的离子方程式__________________________。
(6)6.82g碱式碳酸锌[aZn(OH)2·bZnCO3·cH2O]恰好溶解在40mL3mol/LHCl中,同时产生448mLCO2(标准状况下),试推算碱式碳酸锌的化学式为___________________________。
17.(14分).碳和氮的化合物在生产生活中广泛存在。回答下列问题:
(1)三氯化氮(NCl3)是一种黄色、油状、具有刺激性气味的挥发性有毒液体,各原子均满足8电子稳定结构。其电子式是__________________。氯碱工业生产时,由于食盐水中通常含有少量NH4Cl,而在阳极区与生成的氯气反应产生少量NCl3,该反应的化学方程式为_____________。
(2)利用CO可以将NO转化为无害的N2,其反应为: 2NO(g) +2CO(g) N2(g) +2CO2(g),向容积均为1L的甲、乙两个恒温(温度分别为300℃、T℃)容器中分别加入2.00molNO和2.00molCO,测得各容器中n(CO)随反应时间t的变化情况如下表所示:
t/min
0
40
80
120
160
N甲(CO)/mol
2.00
1.50
1.10
0.80
0.80
N乙(CO)/mol
2.00
1.45
1.00
1.00
1.00
①甲容器中,0~40min 内用NO的浓度变化表示的反应速率v(NO)=_____________。
②该反应的△H____0(填“>”或“<”)。
③甲容器反应达到平衡后,若容器内各物质的量均增加1倍,则平衡______(填“正向”、“逆向”或“不”)移动。
(3)在酸性电解质溶液中,以惰性材料作电极,将CO2转化为丙烯的原理如下图所示
①太阳能电池的负极是__________(填“a”或“b”)
②生成丙烯的电极反应式是_____________________________。
- 8 -
18.(15分)有机物A是一种重要的有机合成原料,B是植物果实的催熟剂。以有机物A为原料合成G(医药中间体和材料中间体)的路线如下图所示:
已知:
①(R表示烃基,R’和R”表示烃基或氢)
② 同一个碳原子上连两个-OH不稳定。
请回答下列问题:
(1)A→C的反应类型是_______。A→B的反应条件是_________。 G中所含官能团的名称是________。
(2)C→D反应的化学方程式___________。
(3)与F具有相同的碳骨架和相同的官能团种数的同分异构体数目共有__________种(不含F)。
(4)写出一种满足下列条件的物质G的同分异构体的结构简式:_______。
①能发生银镜反应; ②核磁共振氢谱有3个峰; ③含有甲基的数目最多
(5)聚苯乙烯(PS)是一种多功能塑料,广泛应用于食品包装、绝缘板、商业机器设备等许多领域中。写出以D和苯为主要原料制备聚苯乙烯的合成路线流程图(无机试剂任选)。
- 8 -
江西省景德镇一中2021届高三摸底考试化学试题答案
1.【答案】D
2.【答案】B
3.【答案】C
4.【答案】A
5.【答案】D
6.【答案】D
7.【答案】B
8.【答案】C
9.【答案】D
10.【答案】B
11. 【答案】C
12.【答案】C
13.【答案】C
14.【答案】C
15.【答案】(1)(球形)冷凝管(1分) (2)防暴沸(1分) 使反应液受热均匀(或易于控制反应温度) (1分)
(3)除去混合液中的硫酸(1分) 蒸出混合物中的甲醇、水(1分)
(4)除去混合液中少量的水(或干燥有机相) (2分) (5)对甲基苯甲醚(1分) (6)60% (2分)
16.【答案】 (1). 10mol·L-1 (2). 增大接触面积,加快反应速率 (3). 除去滤液中含有的Cu2+离子 (4). (NH4)2SO4 (5). 取少量的A溶液于试管中,加入氢氧化钠并加热,产生能使湿润的红色石蕊试纸变蓝的气体,则含有NH4+ (6). 2Fe2++H2O2+2H+=2H2O+2Fe3+ (7). 2Zn(OH)2·ZnCO3·H2O
17.【答案】 (1). (2). NH4Cl+3Cl2=NCl3+4HCl (3). 0.0125mol/(L·min) (4). < (5). 正向 (6). a (7). 3CO2+18H++18e-=C3H6+6H2O
18.【答案】 (1). 取代反应 (2). 氢氧化钠的醇溶液、加热 (3). 碳碳双键、羟基 (4). 2CH3CH2OH+O2 2CH3CHO+2H2O (5). 8 (6). C(CH3)3CH2CHO (7).
- 8 -
- 8 -