- 2021-04-17 发布 |
- 37.5 KB |
- 8页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2016-2017学年山东省济宁市金乡县九年级(上)期中化学试卷
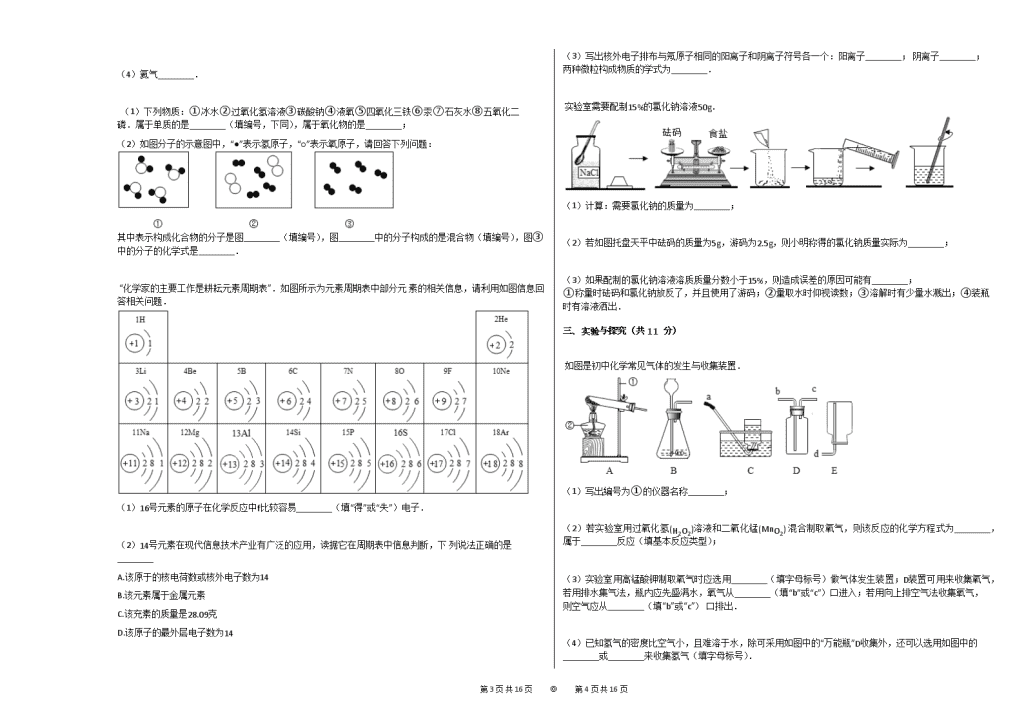
2016-2017学年山东省济宁市金乡县九年级(上)期中化学试卷 一、选择题(下列各题只有一个正确选项,其中1-4小题各1分,5-10小题各2分,本题共16分) 1. 物质的角途与性质密切相关,下列说法错误的是( ) A.氮气常用作保护气,是由于氮气的化学性质不活泼 B.洗涤剂常用来去除油污,是因为洗涤剂具有乳化作用 C.甩镁粉制作照明弹,是因为镁条燃烧发出耀眼的白光 D.氧气可用作火箭发射的燃料,是因为氧气具有助燃性 2. 下列化学用语中既能表示一种物质,也表示组成这种物质的元素,还能表示该元素的一个原子的是( ) A.2N2 B.Ag C.H D.Mg2+ 3. 对下面一些实验现象的描述,正确的是( ) A.铁在空气中加热,剧烈燃烧、生成黑色固体 B.氢气在空气中点燃,发出黄光、放出热量 C.测定空气中氧气含量的实验里,铜粉加热变黑 D.碳在氧气中燃烧,生成二氧化碳气体 4. 溶液在生产,生活中应用广泛.下列有关溶液的说法正确的是( ) A.均一、稳定的液体都是溶液 B.溶液中不能同时存两种溶质 C.只有固体和液体可以作为溶质 D.外界条件不改变,溶质溶剂不会分离 5. 硝酸铵(NH4NO3)是由铵根离子(NH4+)和硝酸根离子(NO3−)构成的,在农业上可用做化肥.则硝酸铵中NH4+和NO3−中氮元素的化合价分别为( ) A.+1,−l B.+2,−2 C.−3,+4 D.−3,+5 6. 现代科技证明,葡萄酒中含有的白藜芦醇具有美容养颜之功效.下列关于白藜芦醇(C14H12O3)的说法错误的是( ) A.白藜芦醇由碳、氢、氧三种元素组成 B.白藜芦醇中碳、氢、氧元素的个数比为14:12:3 C.白藜芦醇的相对分子质量为228 D.白藜芦醇中碳、氢、氧三种元素的质量比为14:1:4 7. 如图表示两种气体发生化学反应的微观示意图,其中相同的球代表同种原子。你认为下列说法正确的是( ) A.生成物一定是混合物 B.分子在化学变化中不可分 C.该反应属于化合反应 D.化学反应前后元素的种类发生了变化 8. 根据事物的某些相似性类推其他的相似性,并预测类似的可能性,是我们经常使用的一种思维方法.下列说法正确的是( ) A.氧化物中都含有氧元素---含有氧元素的化合物都是氧化物 B.饱和溶液不能继续溶解某种溶质---饱和溶液也不继续溶解其他溶质 C.单质中只含有一种元素---但是只含有一种元素的物质不一定是单质 D.H2O和H2O2的组成元素相同-----所以他们的化学性质也相同 9. 发射“神舟十号”的长三甲火箭燃料是偏二甲肼(C2H8N2),氧化剂是四氧化二氮(N2O4),反应的化学方程式为C2H8N2+2N2O4=3X+2CO2+4H2O,则X的化学式为( ) A.CH4 B.N2 C.NO D.NO2 10. 下列有关水的说法中不正确的是( ) A.水分子中含有两个氢原子、一个氧原子 B.电解水实验证明水是由氢、氧两种元素组成的 C.用肥皂水可以区分软水和硬水 D.水是一种氧化物 二、填空与简答(共17分) 分子、原子和离子都是构成物质的粒子,请按要求用符号完成下面问题: (1)氧化镁中镁元素为+2价________; (2)三个氮分子________; (3)2个亚铁离子________; 第13页 共16页 ◎ 第14页 共16页 (4)氦气________. (1)下列物质:①冰水②过氧化氢溶液③碳酸钠④液氧⑤四氧化三铁⑥汞⑦石灰水⑧五氧化二磷.属于单质的是________(填编号,下同),属于氧化物的是________; (2)如图分子的示意图中,“●”表示氢原子,“○”表示氧原子,请回答下列问题: 其中表示构成化合物的分子是图________(填编号),图________中的分子构成的是混合物(填编号),图③中的分子的化学式是________. “化学家的主要工作是耕耘元素周期表”.如图所示为元素周期表中部分元 素的相关信息,请利用如图信息回答相关问题. (1)16号元素的原子在化学反应中f比较容易________(填“得”或“失”)电子. (2)14号元素在现代信息技术产业有广泛的应用,读据它在周期表中信息判断,下 列说法正确的是________ A.该原于的核电荷数或核外电子数为14 B.该元素属于金属元素 C.该充素的质量是28.09克 D.该原子的最外层电子数为14 (3)写出核外电子排布与氖原子相同的阳离子和阴离子符号各一个:阳离子________; 阴离子________; 两种微粒构成物质的学式为________. 实验室需要配制15%的氯化钠溶液50g. (1)计算:需要氯化钠的质量为________; (2)若如图托盘天平中砝码的质量为5g,游码为2.5g,则小明称得的氯化钠质量实际为________; (3)如果配制的氯化钠溶液溶质质量分数小于15%,则造成误差的原因可能有________; ①称量时砝码和氯化钠放反了,并且使用了游码;②量取水时仰视读数;③溶解时有少量水溅出;④装瓶时有溶液洒出. 三、实验与探究(共11分) 如图是初中化学常见气体的发生与收集装置. (1)写出編号为①的仪器名称________; (2)若实验室用过氧化氢(H2O2)溶液和二氧化锰(MnO2) 混合制取氧气,则该反应的化学方程式为________,属于________反应(填基本反应类型); (3)实验室用高锰酸钾制取氧气时应选用________(填字母标号)做气体发生装置;D装置可用来收集氧气,若用排水集气法,瓶内应先盛满水,氧气从________(填“b”或“c”)口进入;若用向上排空气法收集氧气,则空气应从________(填“b”或“c”) 口排出. (4)已知氢气的密度比空气小,且难溶于水,除可采用如图中的“万能瓶”D收集外,还可以选用如图中的________或________来收集氢气(填字母标号). 第13页 共16页 ◎ 第14页 共16页 某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究.他们进行了以下实验: ①往盛有5mL 5% H2O2溶液的试管中,伸入带火星的木条,木条不复燃________. ②往盛有5mL w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃. ③往盛有5mL w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃. ④经检验,②③中反应后试管中仍分别含有a g MnO2和a g Fe2O3. 问题: (1)MnO2、Fe2O3在上述反应中的作用是________. (2)实验②④中H2O2的浓度(w%)以________为宜. 研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究.下表选取了部分实验数据: 用足量等体积H2O2溶液制取相同体积O2所需的时间 时间 (min) 浓度 条件 30%H2O2 15%H2O2 5%H2O2 加入agMnO2 0.2 0.8 2.0 加入agFe2O3 7.0 9.0 16.0 问题: (3)从表中能得出哪些结论?________. 四、计算与应用(共6分) 某公共场所张贴有以下广告: 由于纯净的碳酸氢铵中氮元素的质量分数是________,因此这是一则________(填“真实”或“虚假”)广告. 实验室常用过氧化氢溶液与二氧化锰混合制取氧气。现将2.5g二氧化锰放入盛有100g过氧化氢溶液的锥形瓶中,反应完全结束后,共收集到1.6g气体。请完成下列问题: (1)反应结束后,过滤,洗涤并烘干滤渣,称得滤渣的质量为________g。 (2)计算原过氧化氢溶液中溶质的质量分数。 第13页 共16页 ◎ 第14页 共16页 参考答案与试题解析 2016-2017学年山东省济宁市金乡县九年级(上)期中化学试卷 一、选择题(下列各题只有一个正确选项,其中1-4小题各1分,5-10小题各2分,本题共16分) 1. 【答案】 D 【考点】 常见气体的用途 乳化现象与乳化作用 【解析】 氮气的化学性质不活泼; 洗涤剂对油污具有乳化作用; 镁在空气中燃烧时发出耀眼的白光; 氧气能够支持燃烧. 【解答】 解:A、氮气常用作保护气,是由于氮气的化学性质不活泼,该选项说法正确; B、洗涤剂常用来去除油污,是因为洗涤剂具有乳化作用,该选项说法正确; C、甩镁粉制作照明弹,是因为镁条燃烧发出耀眼的白光,该选项说法正确; D、氧气能够支持燃烧,但是不能燃烧,因此不能用作燃料,该选项说法不正确. 故选:D. 2. 【答案】 B 【考点】 化学式的书写及意义 元素的符号及其意义 【解析】 根据元素符号的含义进行分析解答,金属、固体非金属、稀有气体都是由原子直接构成的,故它们的元素符号,既能表示一个原子,又能表示一种元素,还能表示一种物质。 【解答】 A.只能表示2个氮分子,故错误; B.Ag属于金属元素,可表示银元素,表示一个银原子,还能表示银这一纯净物,故正确; C.H可表示氢元素,表示一个氢原子,但不能表示一种物质,故错误; D.只能表示1个镁离子,故错误。 3. 【答案】 C 【考点】 氧气与碳、磷、硫、铁的反应 【解析】 A、根据铁在空气中加热的现象进行分析判断. B、根据氢气在空气中燃烧的现象进行分析判断. C、根据铜粉在空气在加热的现象进行分析判断. D、根据碳在氧气中燃烧的现象进行分析判断. 【解答】 解:A、铁在空气中加热,只能烧至发红,不会产生火星,故选项说法错误. B、氢气在空气中燃烧,产生淡蓝色火焰,放出热量,故选项说法错误. C、铜粉在空气在加热,逐渐变黑,故选项说法正确. D、碳在氧气中燃烧,生成二氧化碳气体,是实验结论而不是实验现象,故选项说法错误. 故选:C. 4. 【答案】 D 【考点】 溶液的相关概念、组成及其特点 【解析】 A、根据溶液的特点考虑;B、根据溶液中溶质的种数考虑;C、根据溶液中溶质的种类考虑;D、根据溶液均一的特点考虑 【解答】 A、溶液是均一、稳定的混合物,均一、稳定的液体不一定是混合物,例如蒸馏水,故A错; B、溶液中溶质可以是一种或多种,溶剂只有一种,故B错; C、汽水中的溶质有二氧化碳,属于气体,故C错; D、由于溶液具有稳定性,所以外界条件不改变,溶质溶剂不会分离,故D正确。 5. 【答案】 D 【考点】 有关元素化合价的计算 【解析】 根据原子团中元素的化合价代数和等于原子团的化合价,结合硝酸铵(NH4NO3)的化学式进行解答本题. 【解答】 硝酸铵(NH4NO3)中铵根显+1价,氢元素显+1价,设铵根中氮元素的化合价是x,由原子团中元素的化合价代数和等于原子团的化合价,可得:x+(+1)×4=+1,则x=−3价。 硝酸根显−1价,氧元素显−2价,设硝酸根中氮元素的化合价是y,由原子团中元素的化合价代数和等于原子团的化合价,可得:y+(−2)×3=−1,则y=+5价。 6. 【答案】 B 【考点】 化学式的书写及意义 相对分子质量的概念及其计算 元素质量比的计算 【解析】 A、根据白藜芦醇化学式的含义进行分析判断. B、根据元素只讲种类、不讲个数,进行分析判断. C、根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析判断. 第13页 共16页 ◎ 第14页 共16页 D、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析判断. 【解答】 A、白藜芦醇是由碳、氢、氧三种元素组成的,故选项说法正确。 B、元素只讲种类、不讲个数,故选项说法错误。 C、白藜芦醇的相对分子质量为12×14+1×12+16×3=228,故选项说法正确。 D、白藜芦醇中碳、氢、氧元素的质量比为=(12×14):(1×12):(16×3)=14:1:4,故选项说法正确。 故选:B。 7. 【答案】 C 【考点】 微粒观点及模型图的应用 【解析】 根据化学反应的微观示意图,对比反应前后微粒的变化,分析分子、原子的变化;分析生成物的种类;分析反应的特点,判断反应的类型等。 【解答】 A、由生成物的微观构成可知,反应后生成了一种新的化合物。故A说法不正确; B、由反应前后微粒的变化可知,分子在化学变化中发生了变化,说明了分子在化学变化中可以再分。故B说法不正确; C、由化学反应的微观示意图可知,该反应由两种物质生成了一种物质,属于化合反应。故C说法正确; D、由反应前后微粒的变化可知,化学反应前后原子的种类和数量不变,元素的种类没有发生变化。故D说法不正确。 8. 【答案】 C 【考点】 饱和溶液和不饱和溶液 氧化物的概念与特性 单质和化合物的概念及判别 分子的定义与分子的性质 【解析】 A、根据氧化物的定义判断. B、根据饱和溶液的定义判断. C、根据由一种元素组成的物质可能是单质,也可能是混合物考虑. D、根据水和过氧化氢是由不同分子构成的判断. 【解答】 解:A、氧化物是指由两种元素组成且其中一种是氧元素的化合物,含有氧元素的化合物不一定是氧化物,如氯酸钾,所以错误. B、某溶质的饱和溶液不能再继续溶解该溶质,但还可能再溶解其它的物质,所以错误. C、由一种元素组成的物质可能是单质,例如氧气是由氧元素组成,属于单质,也可能是混合物,例如金刚石和石墨都是由碳元素组成,二者的混合物属于混合物,所以正确. D、水和过氧化氢是由不同分子构成,所以他们的化学性质不相同,所以错误. 故选:C. 9. 【答案】 B 【考点】 质量守恒定律及其应用 【解析】 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断生成物X的化学式. 【解答】 解:根据反应的化学方程式C2H8N2+2N2O4=3X+2CO2+4H2O,反应物中碳、氢、氮、氧原子个数分别为2、8、6、8,反应后的生成物中碳、氢、氮、氧原子个数分别为2、8、0、8,根据反应前后原子种类、数目不变,则3X分子中含有6个氮原子,则每个X分子由2个氮原子构成,则物质X的化学式为N2. 故选:B. 10. 【答案】 A 【考点】 硬水与软水 电解水实验 氧化物的概念与特性 分子和原子的区别和联系 【解析】 1个水分子是由2个氢原子和1个氧原子构成的; 电解水生成氢气和氧气; 利用肥皂水可以区分硬水和软水; 氧化物是由氧元素和另外一种元素组成的化合物. 【解答】 解:A、应该是1个水分子中含有2个氢原子和1个氧原子,该选项说法不正确; B、电解水生成氢气和氧气,证明水是由氢、氧两种元素组成的,该选项说法正确; C、向水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生大量浮渣,是硬水,因此利用肥皂水可以区分硬水和软水,该选项说法正确; D、水是由氢元素和氧元素组成的化合物,属于氧化物,该选项说法正确. 故选:A. 二、填空与简答(共17分) 【答案】 +2MgO 3N2 2Fe2+ He 【考点】 化学符号及其周围数字的意义 【解析】 (1)化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后. (2)分子的表示方法:正确书写物质的化学式,表示多个该分子,就在其化学式前加上相应的数字. 第13页 共16页 ◎ 第14页 共16页 (3)离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字. (4)氦气属于稀有气体单质,直接用元素符号表示其化学式. 【解答】 解:(1)由化合价的表示方法,在该元素的上方用正负号和数字表示,正负号在前,数字在后,故氧化镁中镁元素为+2价可表示为:+2MgO. (2)由分子的表示方法,正确书写物质的化学式,表示多个该分子,就在其分子符号前加上相应的数字,则三个氮分子可表示为:3N2. (3)由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略.若表示多个该离子,就在其离子符号前加上相应的数字,故2个亚铁离子可表示为:2Fe2+. (4)氦气属于稀有气体单质,直接用元素符号表示其化学式,其化学式为He. 【答案】 ④⑥,①⑤⑧ ①,②,H2 【考点】 单质和化合物的概念及判别 氧化物的概念与特性 化学式的书写及意义 【解析】 纯净物由一种物质组成,混合物由两种或两种以上的物质组成; 单质是由一种元素组成的纯净物,化合物是由不同种元素组成的纯净物; 氧化物是由氧元素和另外一种元素组成的化合物. 【解答】 解:(1)液氧和汞都是由一种元素组成的纯净物,都属于单质; 冰是水的固体,冰水混合物中含有一种物质水,水是由氢元素和氧元素组成的化合物,属于氧化物,四氧化三铁和五氧化二磷都是由氧元素和另外一种元素组成的化合物,都属于氧化物. (2)①中是水分子,水是由氢元素和氧元素组成的纯净物,属于化合物; ②中的分子是氧分子和氢分子,氢分子和氧分子构成的是混合物; ③中的分子是氢分子,氢分子的化学式是. 【答案】 得 A Mg2+,O2−,MgO 【考点】 元素周期表的特点及其应用 原子结构示意图与离子结构示意图 化学符号及其周围数字的意义 【解析】 原子的最外层电子数小于4个的,反应中容易失去电子,大于4个的,反应中容易得到电子; 原子中,核电荷数=核内质子数=核外电子数=原子序数; 氖原子核外电子数是10个,第一层是2个,第二层是8个,镁离子核外电子数是10个,第一层是2个,第二层是8个. 【解答】 解:(1)16号元素是硫元素,硫原子最外层电子数是6个,在化学反应中f比较容易得电子. (2)14号元素是硅元素, A.硅原子的核电荷数或核外电子数为14,该选项说法正确; B.硅元素属于非金属元素,该选项说法不正确; C.硅元素的质量不是28.09g,该选项说法不正确; D.硅原子的最外层电子数为4,该选项说法不正确. (3)氖原子核外电子数是10个,第一层是2个,第二层是8个,镁离子核外电子数是10个,第一层是2个,第二层是8个,镁离子可以表示为Mg2+,镁元素在化合物中化合价是+2,氧离子可以表示为O2−,氧元素在化合物中化合价是−2,根据化合物中元素化合价代数和为零可知镁元素和氧元素组成的化合物的化学式是MgO. 【答案】 7.5g 2.5g ①② 【考点】 一定溶质质量分数的溶液的配制 托盘天平的使用 【解析】 (1)利用溶质质量=溶液质量×溶质的质量分数,进行分析解答. (2)根据天平的使用方法是左物右码,左盘的质量等于右盘的质量加游码的质量,即药品质量=砝码质量+游码质量,如果位置放反,根据左盘的质量=右盘的质量+游码的质量,列等式进行计算. (3)溶质质量分数变小,则可能是溶质质量偏小或溶剂质量偏大,可以分析出可能造成这两个方面错误的原因进行分析解答. 【解答】 解:(1)溶质质量=溶液质量×溶质的质量分数,配制15%的氯化钠溶液50g,需氯化钠的质量=50g×15%=7.5g. (2)若如图托盘天平中砝码的质量为5g,游码为2.5g,由左盘的质量=右盘的质量+游码的质量可知:砝码质量=药品质量+游码的质量,所以药品质量=砝码质量-游码质量,即药品质量=5.0g−2.5g=2.5g. (3)①称量时砝码和氯化钠放反了,并且使用了游码,会造成实际所取的溶质的质量偏小,则使溶质质量分数偏小. ②量取水时仰视读数,读数比实际液体体积小,会造成实际量取的水的体积偏大,则使溶质质量分数偏小. ③溶解时有少量水溅出,会造成实际量取的水的体积偏小,则使溶质质量分数偏大. ④溶液具有均一性,装瓶时有溶液洒出,溶质质量分数不变. 第13页 共16页 ◎ 第14页 共16页 三、实验与探究(共11分) 【答案】 铁架台 2H2O2======MnO22H2O+O2↑,分解 A,c,c C,E 【考点】 氧气的制取装置 氧气的收集方法 反应类型的判定 书写化学方程式、文字表达式 【解析】 (1)要熟悉各种仪器的名称、用途和使用方法; (2)通常情况下,过氧化氢在二氧化锰的催化作用下,分解生成水和氧气; (3)高锰酸钾受热时能够分解生成锰酸钾、二氧化锰和氧气; 氧气的密度比空气的密度大,不易溶于水; (4)根据制取气体的反应物状态、反应条件、气体的性质可以选择发生装置和收集装置. 【解答】 解:(1)編号为①的仪器名称是铁架台. (2)若实验室用过氧化氢溶液和二氧化锰混合制取氧气,该反应的化学方程式为:2H2O2======MnO22H2O+O2↑,属于分解反应. (3)实验室用高锰酸钾制取氧气时需要加热,应选用A装置做气体发生装置; D装置可用来收集氧气,若用排水集气法,瓶内应先盛满水,氧气从c口进入;若用向上排空气法收集氧气,由于氧气密度比空气大,则空气应从c口排出. (4)氢气的密度比空气小,可以用向下排空气法收集,即用E装置收集,氢气难溶于水,可以用排水法收集,即用C装置收集. 【答案】 解:(1)往盛有5mL 5% H2O2溶液的试管中,伸入带火星的木条,木条不复燃,说明产生的氧气很少,往盛有5mL w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃,说明二氧化锰加快了过氧化氢分解的速度,往盛有5mL w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃,说明氧化铁也加快了过氧化氢分解的速度,并且在反应前后质量不变,所以二氧化锰和氧化铁可以作为过氧化氢分解的催化剂,催化剂所起的作用叫催化作用; (2)作对照实验,必须只有一个变量,有没有催化剂属于变量,所以过氧化氢的质量分数必须相同,过氧化氢溶液的溶质质量分数需要5%;由图表中数据可知过氧化氢制取氧气时二氧化锰作催化剂要比氧化铁作催化剂反映的速度快;由图表中数据可知过氧化氢溶液的浓度越大反应速度越快. 答案: (1)催化作用; (2)5%; (3)相同条件下,MnO2的催化效果比Fe2O3好;在其他条件相同的情况下,H2O2浓度越大,产生氧气的速度越快 【考点】 制取气体的反应原理的探究 催化剂的特点与催化作用 【解析】 (1)根据催化剂所起的作用考虑; (2)根据图表中数据找出反应速度快的溶质质量分数; (3)由图中数据进行对比找出反应速度的影响因素即可. 【解答】 解:(1)往盛有5mL 5% H2O2溶液的试管中,伸入带火星的木条,木条不复燃,说明产生的氧气很少,往盛有5mL w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃,说明二氧化锰加快了过氧化氢分解的速度,往盛有5mL w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃,说明氧化铁也加快了过氧化氢分解的速度,并且在反应前后质量不变,所以二氧化锰和氧化铁可以作为过氧化氢分解的催化剂,催化剂所起的作用叫催化作用; (2)作对照实验,必须只有一个变量,有没有催化剂属于变量,所以过氧化氢的质量分数必须相同,过氧化氢溶液的溶质质量分数需要5%;由图表中数据可知过氧化氢制取氧气时二氧化锰作催化剂要比氧化铁作催化剂反映的速度快;由图表中数据可知过氧化氢溶液的浓度越大反应速度越快. 答案: (1)催化作用; (2)5%; (3)相同条件下,MnO2的催化效果比Fe2O3好;在其他条件相同的情况下,H2O2浓度越大,产生氧气的速度越快 四、计算与应用(共6分) 【答案】 17.7%,虚假 【考点】 元素的质量分数计算 【解析】 本题可根据碳酸氢铵的化学式,借助各原子的相对原子质量,代入质量分数的计算式中来计算N元素的质量分数,若与广告中相同则为真实广告,否则为虚假广告. 【解答】 解:由碳酸氢铵得化学式为NH4HCO3, 则氮元素的质量分数为1414+1×4+1+12+16×3×100%=17.7%, 显然与广告中19.8%不同,则属于虚假广告, 故答案为:17.7%;虚假. 【答案】 2.5 3.4%; 【考点】 第13页 共16页 ◎ 第14页 共16页 根据化学反应方程式的计算 有关溶质质量分数的综合计算 【解析】 (1)根据二氧化锰是过氧化氢分解的催化剂,反应前后质量不变。 (2)利用分解过氧化氢制氧气的化学方程式,根据氧气的质量求出过氧化氢的质量,根据溶质的质量分数计算公式求出过氧化氢溶液中溶质的质量分数。 【解答】 反应结束后,过滤,洗涤并烘干滤渣,称得滤渣的质量就是二氧化锰的质量,是2.5g; 设:生成1.6g气体需要该过氧化氢溶液中溶质的质量为x 2H2O2MnO22H2O+O2↑ 68 32 x 1.6g 根据6832=x1.6g解得x=3.4g 该溶液中溶质的质量分数=3.4g100g×100%=3.4% 第13页 共16页 ◎ 第14页 共16页查看更多