- 2021-04-16 发布 |
- 37.5 KB |
- 26页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2018届一轮复习人教版化学能与热能学案
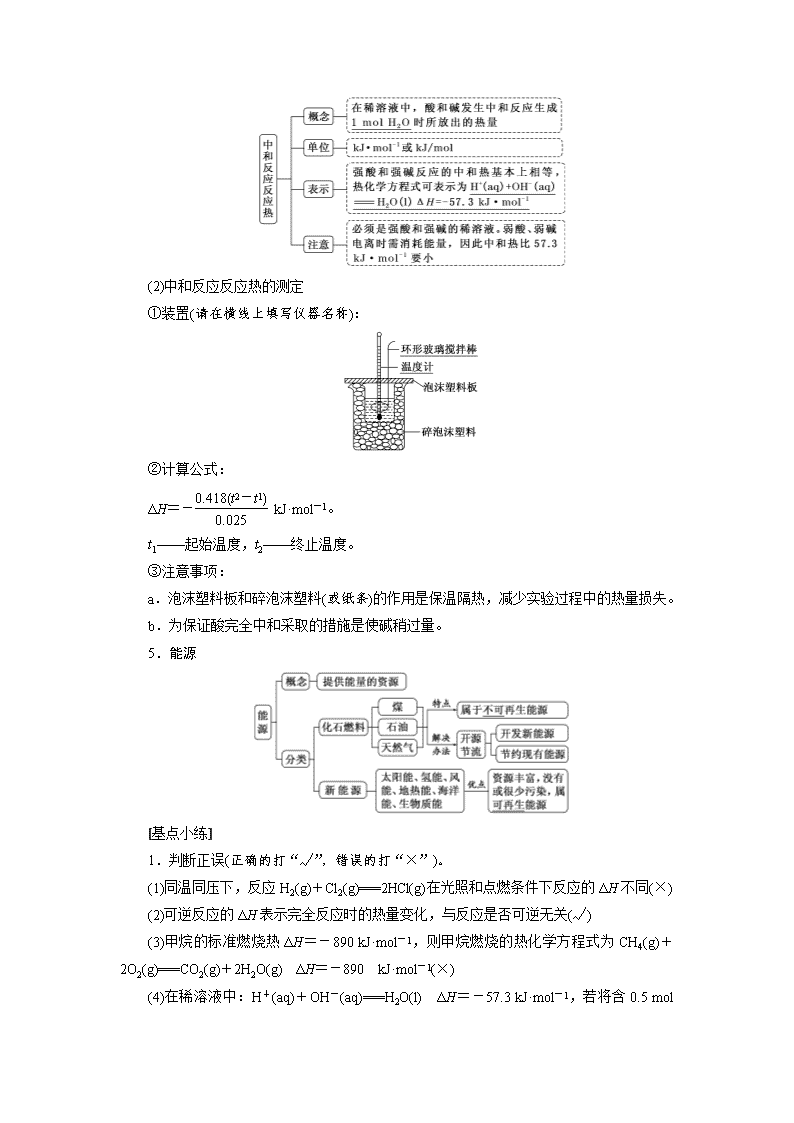
第六章 化学反应与能量 考点一 焓变、反应热 一、了解化学反应中的“两变化”、“两守恒” 1.“两变化”:物质变化和能量变化。 2.“两守恒”:质量守恒和能量守恒。常见的能量转化形式有热能、光能、电能等,通常主要表现为热量的变化。 二、理清五个概念 1.反应热:化学反应过程中吸收或放出的热量,通常叫做反应热 2.焓变 (1)定义:生成物与反应物的焓值差。 (2)焓变与反应热的关系:恒压条件下,化学反应的焓变等于反应热。 (3)符号:ΔH。 (4)单位:kJ·mol-1或kJ/mol。 3.燃烧热 4.中和反应反应热(简称中和热) (1)中和反应反应热的概念及表示方法 (2)中和反应反应热的测定 ①装置(请在横线上填写仪器名称): ②计算公式: ΔH=- kJ·mol-1。 t1——起始温度,t2——终止温度。 ③注意事项: a.泡沫塑料板和碎泡沫塑料(或纸条)的作用是保温隔热,减少实验过程中的热量损失。 b.为保证酸完全中和采取的措施是使碱稍过量。 5.能源 [基点小练] 1.判断正误(正确的打“√”,错误的打“×”)。 (1)同温同压下,反应H2(g)+Cl2(g)===2HCl(g)在光照和点燃条件下反应的ΔH不同(×) (2)可逆反应的ΔH表示完全反应时的热量变化,与反应是否可逆无关(√) (3)甲烷的标准燃烧热ΔH=-890 kJ·mol-1,则甲烷燃烧的热化学方程式为CH4(g)+2O2(g)===CO2(g)+2H2O(g) ΔH=-890 kJ·mol-1(×) (4)在稀溶液中:H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,若将含0.5 mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量为57.3 kJ(×) (5)煤、石油、天然气均为化石能源,是非再生能源(√) 三、两角度明辨吸热反应和放热反应 角度一:反应物和生成物总能量的相对高低 ΔH<0,放热反应 ΔH>0,吸热反应 角度二:断键吸收能量和成键放出能量的相对大小 [基点小练] 2.判断正误(正确的打“√”,错误的打“×”)。 (1)放热反应不需要加热就能反应,吸热反应不加热就不能反应(×) (2)反应HCHO+O2CO2+H2O为吸热反应(×) (3)一个化学反应,当反应物能量大于生成物能量时,反应放热,ΔH为“+”(×) (4)当反应物的键能之和大于生成物的键能之和时,反应放热(×) 题点(一) 基本概念辨析 1.(2017·济南模拟)下列说法中正确的是( ) A.在化学反应过程中,发生物质变化的同时不一定发生能量变化 B.破坏生成物全部化学键所需要的能量大于破坏反应物全部化学键所需要的能量时,该反应为吸热反应 C.生成物的总焓大于反应物的总焓时,反应吸热,ΔH>0 D.ΔH的大小与热化学方程式的化学计量数无关 解析:选C 化学反应中一定有能量变化,A项错误;B项中,由ΔH=断开旧化学键吸收的能量-形成新化学键放出的能量,得ΔH<0,故为放热反应;吸热反应的ΔH>0,C正确;ΔH的大小与热化学方程式的化学计量数成正比关系,D错误。 2.下列说法正确的是( ) A.葡萄糖的燃烧热是2 800 kJ·mol-1,则C6H12O6(s)+3O2(g)===3CO2(g)+3H2O(l)ΔH =-1 400 kJ·mol-1 B.已知101 kPa时,2C(s)+O2(g)===2CO(g) ΔH=-221 kJ·mol-1,则该反应的反应热为221 kJ·mol-1 C.已知稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1,则稀醋酸与稀氢氧化钠溶液反应生成1 mol水时放出57.3 kJ的热量 D.已知HCl和NaOH反应的中和热ΔH=-57.3 kJ·mol-1,则98%的浓硫酸与稀氢氧化钠溶液反应生成1 mol水的中和热为-57.3 kJ·mol-1 解析:选A 燃烧热是指1 mol纯物质完全燃烧放出的热量,故 mol葡萄糖燃烧放出热量1 400 kJ,A正确;B项中反应的反应热应为-221 kJ·mol-1;醋酸为弱电解质,不完全电离,电离时吸热,故稀醋酸与稀NaOH反应生成1 mol水放出的热量小于57.3 kJ;浓硫酸稀释时放热,其与NaOH反应生成1 mol水放出的热量大于57.3 kJ,B、C、D错误。 反应热答题规范 (1)描述反应热时,不论是用“反应热”、“焓变”表示还是用ΔH表示,其后所跟数值都需要带“+”、“-”符号。如某反应的反应热(或焓变)为ΔH=-Q kJ·mol-1或ΔH=+Q kJ·mol-1。 (2)由于中和反应和燃烧均是放热反应,表示中和热和燃烧热时可不带“-”号,但用ΔH表示时,必须带“-”号,如某物质的燃烧热为ΔH=-Q kJ·mol-1或Q kJ·mol-1。 题点(二) 焓变、活化能的图像分析 3.(2016·海南高考)由反应物X转化为Y和Z的能量变化如图所示。下列说法正确的是( ) A.由X→Y反应的ΔH=E5-E2 B.由X→Z反应的ΔH<0 C.降低压强有利于提高Y的产率 D.升高温度有利于提高Z的产率 解析:选BC A项,由X→Y反应的ΔH=E3-E2,错误;B项,由图像可知,反应物的总能量高于生成物的总能量,该反应为放热反应,即由X→Z反应的ΔH<0,正确;C项,根据化学反应2X(g)== =3Y(g),该反应是气体体积增加的可逆反应,降低压强,平衡正向移动,有利于提高Y的产率,正确;D项,由B分析可知,该反应为放热反应,升高温度,平衡逆向移动,Z的产率降低,错误。 4.(2017·河南十校模拟)研究表明N2O与CO在Fe+作用下发生反应的能量变化及反应历程如图所示,下列说法错误的是( ) A.反应总过程ΔH<0 B.Fe+使反应的活化能减小 C.FeO+也是该反应的催化剂 D.Fe++N2O―→FeO++N2、FeO++CO―→Fe++CO2两步反应均为放热反应 解析:选C A项,反应总过程为N2O+CO===N2+CO2,根据图示可知,反应物总能量高于生成物总能量,为放热反应,ΔH<0,正确;B项,根据反应历程,Fe+为催化剂,能够降低反应的活化能,正确;C项,FeO+为中间产物,而不是催化剂,错误;D项,根据图示,Fe++N2O―→FeO++N2、FeO++CO―→Fe++CO2两反应中反应物总能量均高于生成物总能量,均为放热反应,正确。 5.(2015·北京高考)最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下: 下列说法正确的是( ) A.CO和O生成CO2是吸热反应 B.在该过程中,CO断键形成C和O C.CO和O形成了具有极性共价键的CO2 D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程 解析:选C A项,状态Ⅰ总能量为反应物总能量,状态Ⅲ总能量为生成物总能量,由图示知反应物的总能量大于生成物的总能量,该反应为放热反应;B项,从状态Ⅰ、Ⅱ、Ⅲ的图示可以看出,反应中CO并未断裂成C和O,C、O原子间一直有化学键;C项,由图示可以看出,CO和O2生成了CO2,CO2分子中C与O形成极性共价键;D项,状态Ⅰ→状态Ⅲ表示CO与O反应生成CO2的过程,并不是CO与O2的反应过程。 活化能与焓变的关系 (1)催化剂能降低反应的活化能,但不影响焓变的大小。 (2)在无催化剂的情况,E1为正反应的活化能,E2为逆反应的活化能,ΔH=E1-E2。 考点二 热化学方程式 1.概念 表示参加反应的物质的物质的量和反应热的关系的化学方程式。 2.意义 不仅表明了化学反应中的物质变化,也表明了化学反应中的能量变化。例如:H2(g)+O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1,表示在25 ℃和1.01×105 Pa下,1 mol氢气和0.5 mol氧气完全反应生成1 mol液态水时放出285.8 kJ的热量。 3.书写步骤 4.注意事项 (1)热化学方程式不注明反应条件。 (2)热化学方程式不标“↑”“↓”,但必须用s、l、g、aq等标出物质的聚集状态。 (3)热化学方程式的化学计量数只表示物质的量,其ΔH必须与化学方程式及物质的聚集状态相对应。 [基点小练] (1)101 kPa时,1 mol H2完全燃烧生成液态水,放出285.8 kJ的热量,表示H2燃烧热的化学方程式为__________________________________________________________ ________________________________________________________________________。 (2)101 kPa时,1 mol CH4完全燃烧生成液态水和CO2气体,放出890.3 kJ的热量,表示其反应热的化学方程式为___________________________________________________ ________________________________________________________________________。 (3)0.3 mol乙硼烷(分子式B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ的热量,则其热化学方程式为______________________________________。 答案:(1)H2(g)+O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1 (2)CH4(g)+2O2(g)===CO2(g)+2H2O(l) ΔH=-890.3 kJ·mol-1 (3)B2H6(g)+3O2(g)===B2O3(s)+3H2O(l) ΔH=-2 165 kJ·mol-1 题点(一) 热化学方程式的正误判断 1.(2014·海南高考)标准状况下,气态分子断开1 mol化学键的焓变称为键焓。已知H—H、H—O和O===O键的键焓ΔH分别为436 kJ·mol-1、463 kJ·mol-1和495 kJ·mol-1。下列热化学方程式正确的是( ) A.H2O (g)=== H2(g)+O2(g) ΔH= -485 kJ·mol-1 B.H2O (g)===H2(g)+O2(g) ΔH=+485 kJ·mol-1 C.2H2(g)+ O2 (g)===2H2O(g) ΔH = +485 kJ·mol-1 D.2H2(g)+ O2(g)===2H2O(g) ΔH= -485 kJ·mol-1 解析:选D 1 mol的气态水分解产生1 mol的氢气和 mol 的氧气的能量变化是:2×463-436-×495=242.5,因此热化学方程式为H2O(g)===H2(g)+O2(g) ΔH=+242.5 kJ·mol-1,A、B错误。2 mol的气态水分解产生2 mol的氢气和1 mol的氧气的反应热是ΔH=+485 kJ,物质分解吸收的热量与产物燃烧放出的热量数值相等,即热化学方程式是2H2(g)+O2(g)===2H2O(g) ΔH=-485 kJ·mol-1,C错误,D正确。 2.航天燃料从液态变为固态,是一项重要的技术突破。铍是高效率的火箭材料,燃烧时放出巨大的能量,已知1 kg金属铍完全燃烧放出的热量为62 700 kJ。则铍燃烧的热化学方程式正确的是( ) A.Be+O2===BeO ΔH=-564.3 kJ·mol-1 B.Be(s)+O2(g)===BeO(s) ΔH=+564.3 kJ·mol-1 C.Be(s)+O2(g)===BeO(s) ΔH=-564.3 kJ·mol-1 D.Be(s)+O2(g)===BeO(g) ΔH=-564.3 kJ·mol-1 解析:选C 1 kg Be的物质的量为= mol,又因为1 kg铍完全燃烧放出的热量为62 700 kJ,则1 mol铍完全燃烧放出的热量为 kJ=564.3 kJ,Be与氧气反应生成BeO,则其热化学方程式为Be(s)+O2(g)===BeO(s) ΔH=-564.3 kJ·mol-1。 3.下列热化学方程式正确的是( ) A.表示硫的燃烧热的热化学方程式:S(s)+O2(g)===SO3(g) ΔH=-315 kJ·mol-1 B.表示中和热的热化学方程式:NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1 C.表示H2燃烧热的热化学方程式:H2(g)+O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1 D.表示CO燃烧热的热化学方程式:2CO(g)+O2(g)===2CO2(g) ΔH=-566 kJ·mol-1 解析:选B 表示燃烧热的热化学方程式,可燃物质的物质的量为1 mol,反应生成稳定氧化物,A中应生成SO2;C中应生成H2O(l),D中CO的物质的量应为1 mol。 判断热化学方程式的“5审法” 题点(二) 多角度书写热化学方程式 角度一 依据反应事实书写热化学方程式 4.根据信息,写出下列热化学方程式 (1)(2016·天津高考)Si与Cl两元素的单质反应生成1 mol Si的最高价化合物,恢复至室温,放热687 kJ,已知该化合物的熔、沸点分别为-69 ℃和58 ℃。写出该反应的热化学方程式:_____________________________________________________。 (2)(2014·安徽高考)CuCl(s)与O2反应生成CuCl2(s)和一种黑色固体。在25 ℃、101 kPa下,已知该反应每消耗1 mol CuCl(s),放热44.4 kJ,该反应的热化学方程式是_______________________________________________________________________ ________________________________________________________________________。 (3)(2014·全国卷)化合物AX3和单质X2在一定条件下反应可生成化合物AX5。回答下列问题: 已知AX3的熔点和沸点分别为-93.6 ℃和76 ℃,AX5的熔点为167 ℃。室温时AX3与气体X2反应生成1 mol AX5,放出热量123.8 kJ。该反应的热化学方程式为_______________________________________________________________________ ________________________________________________________________________。 答案:(1)Si(s)+2Cl2(g)===SiCl4(l)ΔH=-687 kJ·mol-1 (2)4CuCl(s)+O2(g)===2CuCl2(s)+2CuO(s)ΔH=-177.6 kJ·mol-1 (3)AX3(l)+X2(g)===AX5(s)ΔH=-123.8 kJ·mol-1 角度二 依据图像书写热化学方程式 5.已知化学反应A2(g)+B2(g)===2AB(g)的能量变化如图所示,请写出该反应的热化学方程式:_______________________________________________________________ ________________________________________________________________________。 解析:由图可知,生成物总能量高于反应物总能量,故该反应为吸热反应,ΔH=+(a-b)kJ·mol-1。 答案:A2(g)+B2(g)===2AB(g)ΔH=+(a-b)kJ·mol-1 6.化学反应N2+3H2===2NH3的能量变化如图所示(假设该反应反应完全) 试写出N2(g)和H2(g)反应生成NH3(l)的热化学方程式: ________________________________________________________________________。 解析:反应热等于反应物的键能之和减去生成物的键能之和,所以N2(g)+H2(g)===NH3(g) ΔH=(a-b)kJ·mol-1, 而1 mol的NH3(g)转化为1 mol的NH3(l)放出的热量为c kJ,根据盖斯定律有:N2(g)+H2(g)===NH3(l)ΔH=(a-b-c)kJ·mol-1, 即N2(g)+3H2(g)===2NH3(l)ΔH=2(a-b-c)kJ·mol-1 答案:N2(g)+3H2(g)===2NH3(l) ΔH=2(a-b-c) kJ·mol-1 考点三 盖斯定律 反应热的计算、比较 化学反应与能量变化是历年高考必考的内容之一,有关反应热的计算是化学反应中能量变化的重点,在高考中试题难度适中,重在考查燃烧热、中和热的概念,键能与反应热之间的关系、热化学方程式及盖斯定律的应用,其中考查用盖斯定律计算反应热和热化学方程式的书写在全国卷中再现率极高,并常与化学平衡结合,多在非选择题中出现。 根据公式计算反应热 [典例1] (2016·海南高考)油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应: C57H104O6(s)+80O2(g)===57CO2(g)+52H2O(l) 已知燃烧1 kg该化合物释放出热量3.8×104 kJ。油酸甘油酯的燃烧热ΔH为( ) A.3.8×104 kJ·mol-1 B.-3.8×104 kJ·mol-1 C.3.4×104 kJ·mol-1 D.-3.4×104 kJ·mol-1 [解析] 燃烧热指的是燃烧1 mol 可燃物生成稳定的氧化物所放出的热量。燃烧1 kg油酸甘油酯释放出热量3.8×104 kJ,燃烧1 mol 油酸甘油酯释放出热量为×3.8×104 kJ=3.36×104 kJ≈3.4×104 kJ,则得油酸甘油酯的燃烧热ΔH=-3.4×104 kJ·mol-1。 [答案] D 计算公式:Q=燃烧热×n(可燃物的物质的量),如H2的燃烧热为ΔH=-285.8 kJ·mol-1,燃烧2 mol H2放出的热量为2 mol×285.8 kJ·mol-1=571.6 kJ。计算公式中Q、燃烧热和n三个量,若已知任意两个,可求第三个。 [对点演练] 1.(2015·海南高考)已知丙烷的燃烧热ΔH=-2 215 kJ·mol-1,若一定量的丙烷完全燃烧后生成1.8 g水,则放出的热量约为( ) A.55 kJ B.220 kJ C.550 kJ D.1 108 kJ 解析:选A 1.8 g水为0.1 mol,丙烷的分子式是C3H8,1 mol丙烷完全燃烧会产生4 mol水,丙烷完全燃烧产生1.8 g水,燃烧的丙烷的物质的量为 mol,所以反应放出的热量为×2 215=55.375(kJ)。 根据键能计算反应热 [典例2] (2015·全国卷Ⅱ节选)甲醇既是重要的化工原料,又可作为燃料,利用合成气(主要成分为CO、CO2和H2)在催化剂作用下合成甲醇。发生的主要反应如下: ①CO(g)+2H2(g)CH3OH(g) ΔH1 ②CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH2 ③CO2(g)+H2(g)CO(g)+H2O(g) ΔH3 回答下列问题: 已知反应①中相关的化学键键能数据如下: 化学键 H-H C-O H-O C-H E/(kJ·mol-1) 436 343 1 076 465 413 由此计算ΔH1=________kJ·mol-1;已知ΔH2=-58 kJ·mol-1,则ΔH3=________kJ·mol-1。 [解析] 根据键能与反应热的关系可知,ΔH1=反应物的键能之和-生成物的键能之和=(1 076 kJ·mol-1+2×436 kJ·mol-1)-(413 kJ·mol-1×3+343 kJ·mol-1+465 kJ·mol-1)=-99 kJ·mol-1。根据盖斯定律,由②-①可得:CO2(g)+H2(g)CO(g)+H2O(g),ΔH3=ΔH2-ΔH1=(-58 kJ·mol-1)-(-99 kJ·mol-1)=+41 kJ·mol-1。 [答案] -99 +41 依据键能计算ΔH的方法 (1)计算公式:ΔH=反应物的键能总和-生成物的键能总和。 (2)根据键能计算反应热的关键是正确找出反应物和生成物所含共价键的数目,如H2O分子中含有2个O—H共价键,NH3分子中含有3个N—H共价键,P4分子中含有6 个 P—P共价键等。要注意晶体结构中化学键的情况,常见的有1 mol晶体硅含有2 mol Si—Si键,1 mol石墨晶体中含有1.5 mol C—C键,1 mol金刚石含有2 mol C—C键,1 mol SiO2含有4 mol Si—O键等。 [对点演练] 2.(2015·全国卷Ⅰ节选)已知反应2HI(g)H2(g)+I2(g)的ΔH=+11 kJ·mol-1,1 mol H2(g)、1 mol I2(g)分子中化学键断裂时分别需要吸收436 kJ、151 kJ的能量,则1 mol HI(g)分子中化学键断裂时需吸收的能量为________kJ。 解析:设1 mol HI(g)分子中化学键断裂吸收的能量为x,则2x-436 kJ-151 kJ=+11 kJ,x=299 kJ。 答案:299 3.(2017·江西师大附中模拟)肼(H2NNH2)是一种高能燃料,有关化学反应的能量变化如图所示。已知断裂1 mol化学键所需的能量(kJ):N≡N为942、O===O为500、N—N为154,则断裂1 mol N—H键所需的能量(kJ)是( ) A.194 B.391 C.516 D.658 解析:选B 由图示可知断开1 mol N2H4(g)和1 mol O2中所有化学键需要吸收的总能量为2 752 kJ-534 kJ=2 218 kJ,则断裂1 mol N—H键所需的能量为 kJ=391 kJ。 利用盖斯定律计算反应热 1.盖斯定律 (1)内容:对于一个化学反应,无论是一步完成还是分几步完成,其反应焓变都一样。即化学反应的反应热只与反应体系的始态和终态有关,而与反应的途径无关。 (2)本质:能量守恒定律。 2.计算方法 (1)热化学方程式相加或相减,如 ①C(s)+O2(g)===CO2(g) ΔH1 ②C(s)+O2(g)===CO(g) ΔH2 由①-②可得 CO(g)+O2(g)===CO2(g) ΔH=ΔH1-ΔH2 (2)合理设计反应途径,如 顺时针方向和逆时针方向变化反应热代数和相等。 ΔH=ΔH1+ΔH2。 [典例3] (1)(2016·全国甲卷节选)已知 ①2O2(g)+N2(g)===N2O4(l) ΔH1 ②N2(g)+2H2(g)===N2H4(l) ΔH2 ③O2(g)+2H2(g)===2H2O(g) ΔH3 ④2N2H4(l)+N2O4(l)===3N2(g)+4H2O(g) ΔH4=-1 048.9 kJ·mol-1 上述反应热效应之间的关系式为ΔH4=________,联氨和N2O4可作为火箭推进剂的主要原因为________________________________________________________________ ________________________________________________________________________。 (2)(2016·全国丙卷节选)已知下列反应: SO2(g)+2OH-(aq)===SO(aq)+H2O(l) ΔH1 ClO-(aq)+SO(aq)===SO(aq)+Cl-(aq) ΔH2 CaSO4(s)===Ca2+(aq)+SO(aq) ΔH3 则反应SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)===CaSO4(s)+H2O(l)+Cl-(aq)的ΔH=________。 (3)(2016·四川高考节选)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25 ℃,101 kPa时: CaO(s)+H2SO4(l)===CaSO4(s)+H2O(l) ΔΗ=-271 kJ·mol-1 5CaO(s)+3H3PO4(l)+HF(g)===Ca5(PO4)3F(s)+5H2O(l) ΔH=-937 kJ·mol-1 则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是 ________________________________________________________________________。 [解析] (1)由已知热化学方程式①②③可得: N2O4(l)===2O2(g)+N2(g) -ΔH1 2N2H4(l)===2N2(g)+4H2(g) -2ΔH2 2O2(g)+4H2(g)===4H2O(g) 2ΔH3 根据盖斯定律,将上述三个热化学方程式相加,可得2N2H4(l)+N2O4(l)===3N2(g)+4H2O(g) ΔH4=2ΔH3-2ΔH2-ΔH1。由热化学方程式可知,N2H4和N2O4反应时放出大量的热,且产生大量气体。 (2)将已知三个热化学方程式分别标号为Ⅰ、Ⅱ、Ⅲ,根据盖斯定律,由Ⅰ+Ⅱ-Ⅲ 可得:SO2(g)+Ca2+(aq)+ClO-(aq)+2OH-(aq)===CaSO4(s)+H2O(l)+Cl-(aq),则有ΔH=ΔH1+ΔH2-ΔH3。 (3)把已知热化学方程式依次编号①、②,根据盖斯定律由①×5-②得:Ca5(PO4)3F(s)+5H2SO4(l)===5CaSO4(s)+3H3PO4(l)+HF(g) ΔH=-418 kJ·mol-1。 [答案] (1)2ΔH3-2ΔH2-ΔH1 反应放出大量热,产生大量气体 (2)ΔH1+ΔH2-ΔH3 (3)Ca5(PO4)3F(s)+5H2SO4(l)===5CaSO4(s)+3H3PO4(l)+HF(g) ΔH=-418 kJ·mol-1 利用盖斯定律计算反应热的一般步骤 [对点演练] 4.(2015·重庆高考)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为 S(s)+2KNO3(s)+3C(s)===K2S(s)+N2(g)+3CO2(g) ΔH=x kJ·mol-1 已知:碳的燃烧热ΔH1=a kJ·mol-1 S(s)+2K(s)===K2S(s) ΔH2=b kJ·mol-1 2K(s)+N2(g)+3O2(g)===2KNO3(s) ΔH3=c kJ·mol-1 则x为( ) A.3a+b-c B.c-3a-b C.a+b-c D.c-a-b 解析:选A 碳燃烧的热化学方程式为①C(s)+O2(g)===CO2(g) ΔH1=a kJ·mol-1,将另外两个热化学方程式进行编号,②S(s)+2K(s)===K2S(s) ΔH2=b kJ·mol-1,③2K(s)+N2(g)+3O2(g)===2KNO3(s) ΔH3=c kJ·mol-1,根据盖斯定律,由①×3+②-③得S(s)+2KNO3(s)+3C(s)===K2S(s)+N2(g)+3CO2(g) ΔH=(3a+b-c)kJ·mol-1,则x=3a+b-c,故A正确。 5.(1)(2015·福建高考节选)已知: ①Al2O3(s)+3C(s)===2Al(s)+3CO(g) ΔH1=+1 344.1 kJ·mol-1 ②2AlCl3(g)===2Al(s)+3Cl2(g) ΔH2=+1 169.2 kJ·mol-1 由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为 ________________________________________________________________________。 (2)(2015·江苏高考节选)烟气(主要污染物SO2、NOx)经O3预处理后用CaSO3水悬浮液吸收,可减少烟气中SO2、NOx的含量。O3氧化烟气中SO2、NOx的主要反应的热化学方程式为 ①NO(g)+O3(g)===NO2(g)+O2(g) ΔH1=-200.9 kJ·mol-1 ②NO(g)+O2(g)===NO2(g) ΔH2=-58.2 kJ·mol-1 则反应3NO(g)+O3(g)===3NO2(g)的ΔH=______kJ·mol-1。 (3)(2015·山东高考节选)贮氢合金ThNi5可催化由CO、H2合成CH4的反应。温度为T时,该反应的热化学方程式为___________________________________________________ ________________________________________________________________________。 已知温度为T时:①CH4(g)+2H2O(g)===CO2(g)+4H2(g)ΔH1=+165 kJ·mol-1 ②CO(g)+H2O(g)===CO2(g)+H2(g) ΔH2=-41 kJ·mol-1 解析:(1)把热化学方程式②颠倒过来,反应热的数值不变,符号相反可得③2Al(s)+3Cl2(g)===2AlCl3(g) ΔH3=-ΔH2=-1 169.2 kJ·mol-1。 根据盖斯定律,由①+③可得 Al2O3(s)+3C(s)+3Cl2(g)===2AlCl3(g)+3CO(g) ΔH=ΔH1+ΔH3=+174.9 kJ·mol-1,即为Al2O3、C和Cl2反应生成AlCl3的热化学方程式。 (2)将热化学方程式②乘以2可得③2NO(g)+O2(g)===2NO2(g) ΔH3=2×ΔH2=2×(-58.2 kJ·mol-1)=-116.4 kJ·mol-1。根据盖斯定律,由①+③可得3NO(g)+O3(g)=3NO2(g) ΔH=ΔH1+ΔH3=-317.3 kJ·mol-1。 (3)将热化学方程式①颠倒可得③CO2(g)+4H2(g)===CH4(g)+2H2O(g) ΔH3=-ΔH1=-165 kJ·mol-1。根据盖斯定律,由②+③可得CO(g)+3H2(g)===CH4(g)+H2O(g) ΔH=ΔH2+ΔH3=-206 kJ·mol-1,即为要求的热化学方程式。 答案:(1)Al2O3(s)+3C(s)+3Cl2(g)===2AlCl3(g)+3CO(g) ΔH=+174.9 kJ·mol-1 (2)-317.3 (3)CO(g)+3H2(g)===CH4(g)+H2O(g) ΔH=-206 kJ·mol-1 反应热大小的比较 [典例4] (2014·全国卷Ⅱ)室温下,将1 mol的CuSO4·5H2O(s)溶于水会使溶液温度降低,热效应为ΔH1,将1 mol的CuSO4(s)溶于水会使溶液温度升高,热效应为ΔH2;CuSO4·5H2O受热分解的化学方程式为CuSO4·5H2O(s)CuSO4(s)+5H2O(l),热效应为ΔH3。则下列判断正确的是( ) A.ΔH2>ΔH3 B.ΔH1<ΔH3 C.ΔH1+ΔH3=ΔH2 D.ΔH1+ΔH2>ΔH3 [解析] 方法一:1 mol CuSO4·5H2O(s)溶于水会使溶液温度降低,为吸热反应,故ΔH1>0,1 mol CuSO4(s)溶于水会使溶液温度升高,为放热反应,故 ΔH2<0,1 mol CuSO4·5H2O(s)溶于水可以分为两个过程,先分解成1 mol CuSO4(s)和5 mol水,然后1 mol CuSO4(s)再溶于水, CuSO4·5H2O的分解为吸热反应,即ΔH3>0,根据盖斯定律得到关系式ΔH1=ΔH2+ΔH3,分析得到答案:ΔH1<ΔH3。 方法二:本题还可以用图示法进行比较,方法如下。 画出化学变化过程中的能量变化图后, 依据反应物的总能量与生成物的总能量的高低关系可以很方便地比较ΔH的大小。 如图,从图中关系再确定各选项。 [答案] B 利用物质状态,迅速比较反应热的大小的方法 (1)若反应为放热反应,当反应物状态相同、生成物状态不同时,生成固体放热最多,生成气体放热最少。 (2)若反应为放热反应,当反应物状态不同、生成物状态相同时,固体反应放热最少,气体反应放热最多。 (3)在比较反应热(ΔH)的大小时,应带符号比较。对于放热反应,放出的热量越多,ΔH反而越小。 (4)同一物质,状态不同,反应热也不同。 如A(g)A(l) A(s)。 (5)对于可逆反应,因反应不能进行完全,实际反应过程中放出或吸收的能量要小于热化学方程式中反应热的数值。 [对点演练] 6.下列各组热化学方程式的ΔH前者大于后者的是( ) ①C(s)+O2(g)===CO2(g) ΔH1 C(s)+O2(g)===CO(g) ΔH2 ②S(s)+O2(g)===SO2(g) ΔH3 S(g)+O2(g)===SO2(g) ΔH4 ③H2(g)+O2(g)===H2O(l) ΔH5 2H2(g)+O2(g)===2H2O(l) ΔH6 ④CaCO3(s)===CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)===Ca(OH)2(aq) ΔH8 A.① B.④ C.②③④ D.①②③ 解析:选C ΔH有正、负之分,比较时要连同“+”、“-”在内一起比较,类似数学中的正、负数大小的比较。①中第一个热化学方程式减去第二个热化学方程式可得:CO(g)+O2(g)===CO2(g) ΔH=ΔH1-ΔH2,该反应为放热反应,即ΔH1-ΔH2<0,所以ΔH1<ΔH2;②等量的固态硫变为硫蒸气时吸收热量,故在与O2反应产生同样的SO2时,气态硫放出的热量多,即ΔH3>ΔH4;③发生同样的燃烧反应,物质的量越多,放出的热量越多,故ΔH5>ΔH6;④碳酸钙分解吸收热量,ΔH7>0,CaO与H2O反应放出热量,ΔH8<0,ΔH7>ΔH8。 [课堂巩固练] 1.(2017·镇江模拟)2SO2(g)+O2(g)2SO3(g)反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是( ) A.该反应为吸热反应 B.升高温度,不影响活化分子百分数 C.使用催化剂使该反应的反应热发生改变 D.E1-E2=ΔH 解析: 选D 由图像知反应物的能量高于生成物的能量,为放热反应,A错误;升高温度,活化分子百分数增大,B错误;催化剂对反应的始态和终态无影响,只改变活化能,则对反应的焓变无影响,C错误。 2.下列有关能量的判断和表示方法正确的是( ) A.由C(s,石墨)===C(s,金刚石) ΔH=+1.9 kJ,可知:石墨比金刚石更稳定 B.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 C.由H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ,可知:含1 mol CH3COOH的溶液与含1 mol NaOH的溶液混合,放出热量等于57.3 kJ D.2 g H2完全燃烧生成液态水放出285.8 kJ热量,则氢气燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(l) ΔH=-285.8 kJ 解析:选A 石墨转化为金刚石的过程是吸热反应,金刚石能量高,石墨比金刚石稳定,A正确;等质量的硫蒸气和硫固体分别完全燃烧,固体硫变为蒸气需要吸收热量,前者放出热量更多,B错误;含1 mol CH3COOH的溶液与含1 mol NaOH的溶液混合,醋酸为弱酸,溶于水电离需要吸热,放出热量小于57.3 kJ,C错误;2 g H2的物质的量为1 mol,此反应为放热反应,ΔH<0,故氢气燃烧的热化学方程式为2H2(g)+O2(g)===2H2O(l) ΔH=2×(-285.8 kJ·mol-1)=-571.6 kJ·mol-1,D错误。 3.(2017·兰州模拟)已知: 2H2(g)+O2(g)===2H2O(l)ΔH=-571.6 kJ·mol-1 2CH3OH(l)+3O2(g)===2CO2(g)+4H2O(l)ΔH=-1 452 kJ·mol-1 H+(aq)+OH-(aq)===H2O(l)ΔH=-57.3 kJ·mol-1 下列说法正确的是( ) A.H2(g)的燃烧热为142.9 kJ·mol-1 B.同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 C.H2SO4(aq)+Ba(OH)2(aq)===BaSO4(s)+H2O(l) ΔH=-57.3 kJ·mol-1 D.3H2(g)+CO2(g)===CH3OH(l)+H2O(l)ΔH=+131.4 kJ·mol-1 解析:选B 根据燃烧热的定义可知,H2(g)的燃烧热为285.8 kJ·mol-1,A项错误;2 mol(即4 g) H2(g)完全燃烧放出571.6 kJ的热量,2 mol(即64 g)CH3OH(l)完全燃烧放出1 452 kJ的热量,单位质量的H2(g)放出的热量多,B项正确;中和反应是放热反应,硫酸和氢氧化钡反应生成硫酸钡沉淀的过程也是放热的,所以反应ΔH<-57.3 kJ·mol-1,C项错误;将题干中的热化学方程式依次编号为①②③,根据盖斯定律,由,可得热化学方程式:3H2(g)+CO2(g)===CH3OH(l)+H2O(l) ΔH=-131.4 kJ·mol-1,D项错误。 4.一定条件下,充分燃烧一定量的丁烷放出热量161.9 kJ,经测定完全吸收生成的CO2需消耗5 mol·L-1的KOH溶液100 mL,恰好生成正盐,则此条件下热化学方程式: C4H10(g)+O2(g)===4CO2(g)+5H2O(g)的ΔH为( ) A.+2 590.4 kJ·mol-1 B.-2 590.4 kJ·mol-1 C.+1 295.2 kJ·mol-1 D.-1 295.2 kJ·mol-1 解析:选B n(KOH)=c×V=0.1 L×5 mol·L-1=0.5 mol,2KOH+CO2===K2CO3+H2O,根据钾离子守恒,得n(K2CO3)=0.5 mol×=0.25 mol,根据碳原子守恒可知,n(C4H10)=0.25 mol×= mol,故1 mol丁烷完全燃烧放出的热量为161.9 kJ×16=2 590.4 kJ,即ΔH=-2 590.4 kJ·mol-1。 5.(2017·天津五校联考)已知: ①CH3OH(g)+3/2O2(g)===CO2(g)+2H2O(g)ΔH=-a kJ·mol-1 ②CH4(g)+2O2(g)===CO2(g)+2H2O(g)ΔH=-b kJ·mol-1 ③CH4(g)+2O2(g)===CO2(g)+2H2O(l)ΔH=-c kJ·mol-1 则下列叙述中正确的是( ) A.由上述热化学方程式可知b>c B.甲烷的燃烧热为b kJ·mol-1 C.2CH3OH(g)===2CH4(g)+O2(g)ΔH=2(b-a)kJ·mol-1 D.当甲醇和甲烷物质的量之比为1∶2,完全燃烧生成CO2和H2O(l)时,放出的热量为Q kJ,则该混合物中甲醇的物质的量为Q/(a+2b)mol 解析:选C 等物质的量时,CH4燃烧生成液态水放出的热量更多,故c>b,A项错误;甲烷的燃烧热是指1 mol CH4完全燃烧生成CO2气体和液态H2O时放出的热量,反应②中生成的是气态H2O,故b kJ·mol-1不是甲烷的燃烧热,B项错误;①×2-②×2可得2CH3OH(g)===2CH4(g)+O2(g) ΔH=2(b-a)kJ·mol-1,C项正确;③-②+①得CH3OH(g)+O2(g)===CO2(g)+2H2O(l) ΔH=-(a+c-b)kJ·mol-1④,若设甲醇的物质的量为x,则CH4的物质的量为2x,根据④和③有(a+c-b)kJ·mol-1×x+2x kJ·mol-1×c=Q kJ,x= mol,即混合物中甲醇的物质的量为 mol,D项错误。 6.参考下列图表和有关要求回答问题: (1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2 和NO过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是________(填“增大”“减小”或“不变”,下同),ΔH的变化是________。请写出NO2和CO反应的热化学方程式:__________________________。 (2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是: ①CH3OH(g)+H2O(g)===CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1 ②CH3OH(g)+O2(g)===CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1 又知③H2O(g)===H2O(l) ΔH=-44 kJ·mol-1 则甲醇燃烧生成液态水的热化学方程式: ________________________________________________________________________。 (3)下表是部分化学键的键能数据: 化学键 P—P P—O O===O P===O 键能/(kJ·mol-1) a b c x 已知1 mol白磷(P4)完全燃烧放热为d kJ,白磷及其完全燃烧的产物结构如图Ⅱ所示,则表中x=________ kJ·mol-1(用含有a、b、c、d的代数式表示)。 解析:(1)观察图像,E1应为反应的活化能,加入催化剂反应的活化能降低,但是ΔH不变;1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO的反应热即E1和E2之差,因此该反应的热化学方程式为NO2(g)+CO(g)===CO2(g)+NO(g) ΔH=-234 kJ·mol-1。 (2)根据盖斯定律,由3×②-①×2+③×2得:CH3OH(g)+O2(g)===CO2(g)+2H2O(l) ΔH=3×(-192.9 kJ·mol-1)-2×49.0 kJ·mol-1+(-44 kJ·mol-1)×2=-764 kJ·mol-1。 (3)反应热=反应物键能总和-生成物键能总和,即6a+5c-(4x+12b)=-d,可得x=。 答案:(1)减小 不变 NO2(g)+CO(g)===CO2(g)+NO(g) ΔH=-234 kJ·mol-1 (2)CH3OH(g)+O2(g)===CO2(g)+2H2O(l)ΔH=-764.7 kJ·mol-1 (3) [课下提能练] 1.(2016·江苏高考)通过以下反应均可获取H2。下列有关说法正确的是( ) ①太阳光催化分解水制氢:2H2O(l)===2H2(g)+O2(g)ΔH1=+571.6 kJ·mol-1 ②焦炭与水反应制氢:C(s)+H2O(g)===CO(g)+H2(g)ΔH2=+131.3 kJ·mol-1 ③甲烷与水反应制氢:CH4(g)+H2O(g)===CO(g)+3H2(g)ΔH3=+206.1 kJ·mol-1 A.反应①中电能转化为化学能 B.反应②为放热反应 C.反应③使用催化剂,ΔH3减小 D.反应CH4(g)===C(s)+2H2(g)的ΔH=+74.8 kJ·mol-1 解析:选D 反应①是太阳能转化为化学能,A不正确;反应②中ΔH2>0,是吸热反应,B不正确;反应③使用催化剂不能改变反应的焓变,ΔH3不变,C不正确;D项中,由盖斯定律,反应③-②可得CH4(g)===C(s)+2H2(g) ΔH=+74.8 kJ·mol-1,正确。 2.(2017·佛山高三质检)下列热化学方程式书写正确的是(ΔH的绝对值均正确)( ) A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g)ΔH=-1 367.0 kJ·mol-1(燃烧热) B.NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l)ΔH=+57.3 kJ·mol-1(中和热) C.S(s)+O2(g)===SO2(g)ΔH=-296.8 kJ·mol-1(反应热) D.2NO2===O2+2NOΔH=+116.2 kJ·mol-1(反应热) 解析:选C 燃烧热要求可燃物的物质的量必须为1 mol,得到的氧化物必须是稳定的氧化物,即H2O的状态必须为液态,A项错误;中和反应是放热反应,ΔH应小于0,B项错误;热化学方程式要注明物质的聚集状态,D项错误。 3.(2017·南京模拟)根据碘与氢气反应的热化学方程式: ①I2(g)+H2(g)2HI(g) ΔH=-9.48 kJ·mol-1 ②I2(s)+H2(g)2HI(g) ΔH=+26.48 kJ·mol-1 下列判断正确的是( ) A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ C.反应①的产物比反应②的产物稳定 D.反应②的反应物总能量比反应①的反应物总能量低 解析:选D I2(g)+H2(g)2HI(g)是可逆反应,I2(g)不可能全部转化为HI,反应放出的热量小于9.48 kJ,A错误;根据盖斯定律,由②-①得:I2(s)I2(g) ΔH=+35.96 kJ·mol-1,B错误;反应①和反应②的产物都是HI(g),稳定性相同,C错误;对于同一物质,固态物质的能量比气态物质能量低,因此反应②的反应物总能量比反应①的反应物总能量低,D正确。 4.下列依据热化学方程式得出的结论正确的是( ) A.已知NaOH(aq)+HCl(aq)===NaCl(aq)+H2O(l) ΔH=-57.3 kJ·mol-1,则含40.0 g NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量 B.已知2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ·mol-1 C.已知2C(s)+2O2(g)===2CO2(g) ΔH=a 2C(s)+O2(g)===2CO(g) ΔH=b,则a>b D.已知P(白磷,s)===P(红磷,s) ΔH<0,则白磷比红磷稳定 解析:选A 中和热是指稀的强酸和强碱溶液发生中和反应生成1 mol水时所放出的热量,醋酸是弱酸,其电离过程吸热,40.0 g即1 mol NaOH的稀溶液与稀醋酸完全中和,放出小于57.3 kJ的热量,A正确;氢气的燃烧热必须是生成液态水的过程所放出的热量,液态水变为气态水是吸热的,氢气的燃烧热大于241.8 kJ·mol-1,B错误;焦炭完全燃烧放出的热量高于不完全燃烧放出的热量,因焓变是负值,即a查看更多