- 2021-04-15 发布 |
- 37.5 KB |
- 8页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
中考化学压轴题训练之实验探究题
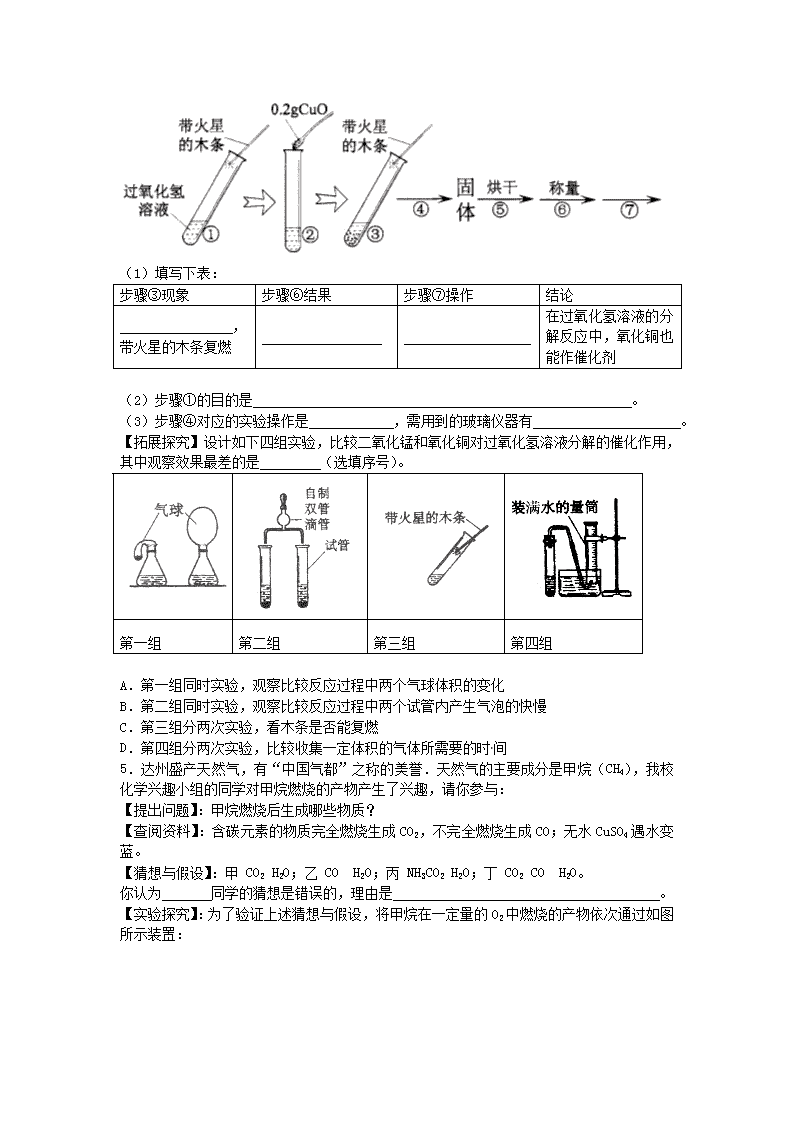
中考化学压轴题训练之实验探究题 1.为进一步研究高锰酸钾的分解产物,某兴趣小组同学查阅资料,并取一定质量的高锰酸钾加热使之完全分解,然后分别进行了以下三个实验。 【实验内容】: 编号 实验内容 实验现象 实验结论 1 取反应后固体剩余物0.2g加入5mL 6%的H2O2溶液中 剧烈反应,放出大量热量,产生大量气体 固体剩余物中的MnO2对H2O2分解有催化作用 2 取0.2gMnO2加入5mL a (H2O2溶液的质量分数)的H2O2溶液中 平稳反应,放出热量,持续产生气体 MnO2对H2O2分解有催化作用 3 取反应后固体剩余物1.0g加入足量水中,充分溶解,过滤 固体完全溶解,滤纸上无黑色固体残余物 固体剩余物中无 b 【实验分析】 (1)完成上表中的填空内容:a _________________ b ______________; (2)实验2的目的是 __________________________________________________; (3)同学们经过讨论,认为实验1的结论不正确,理由是 __________________; 【查阅资料】 Ⅰ、KMnO4受热分解时,在某条件下可能发生以下两个反应: ①6KMnO42K2MnO4+K2Mn4O8+4O2↑ ②KMnO4KMnO2+O2↑ Ⅱ、相对分子质量:(KMnO4:158 O2:32) (4)16gKMnO4中氧元素的质量为 ____;加热使之完全分解,若完全发生反应①,生成O2的质量为 ______;若同时发生反应①②,生成O2的质量范围是 _________ 。(保留二位小数。提示:依据质量守恒定律观察) 2. 张丽同学欲通过实验证明“二氧化锰是过氧化氢分解的催化剂”这一命题。她设计并完成了下表所示的探究实验: 实验操作 实验现象 实验结论或总结 结论 总结 实验一 取5mL5%的过氧化氢溶液于试管中,伸入带火星的木条 有气泡产生,木条不复燃 过氧化氢分解产生氧气,但反应速率 _______。 反应的化学方程式为: 。 二氧化锰是过氧化氢分解的催化剂 实验二 向盛水的试管中加入二氧化锰,伸入带火星的木条 没有明显现象 实验三 二氧化锰能加快过氧化氢的分解 请你帮张丽同学填写上表中未填完的空格。 (1)在张丽的探究实验中,“实验一”和“实验二”起的作用是 ____________。 (2)小英同学认为仅由上述实验还不能完全得出表内的“总结”,她补充设计了两个方面的探究实验,最终完成了对“命题”的实验证明。 第一方面的实验操作中包含了两次称量,其目的是: __________________________; 第二方面的实验是利用“实验三”反应后试管内的剩余物继续实验。接下来的实验操作是: ______________________________________________________________________________。 3.学校化学兴趣小组的同学知道二氧化锰能作过氧化氢(H2O2)分解的催化剂后,想再探究其他一些物质如氧化铝是否也可作过氧化氢分解的催化剂.请你一起参与他们的探究过程,并填写下列空白. 【提出问题】Al2O3能不能作过氧化氢分解的催化剂呢? 【作出猜想】Al2O3能作过氧化氢分解的催化剂。 【实验验证】 实验步骤 实验现象 实验结论 实验一 有少量气泡 木条不复燃 常温下过氧化氢溶液分解速率很慢. 实验二 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 产生大量的气泡 木条复燃 【得出结论】Al2O3能加快过氧化氢的分解速率,故Al2O3能作过氧化氢分解的催化剂. 【反思提高】经过讨论,有的同学认为只有上述两个证据,不能证明Al2O3能作过氧化氢分解的催化剂,还要补充一个探究实验三: 实验三: 【实验目的】探究 。 【实验步骤】①准确称量Al2O3(少量)的质量; ②完成实验二; ③待反应结束,将实验二试管里的物质进行过滤,洗涤, ,称量; ④对比反应前后Al2O3的质量. 【交流讨论】如果Al2O3在反应前后质量不变,则说明Al2O3可以作过氧化氢分解的催化剂. 【提出新的问题】但小华认为,要证明猜想,上述三个实验还不足够,还需要再增加一个探究实验四: 实验四的目的是探究 。 4.在过氧化氢溶液的分解反应中,二氧化锰能作催化剂。下列有关催化剂的说法正确的是 (选填序号)。 A.在化学反应后其质量减小 B.在化学反应后其化学性质发生了变化 C.能增大生成物的质量 D.能改变化学反应速率 【提出问题】在过氧化氢溶液的分解反应中,除了二氧化锰,是否有其他物质也能作催化剂? 【查阅资料】在过氧化氢溶液的分解反应中,氧化铜也能作催化剂。 【进行实验】用天平称量0.2g氧化铜,取5mL5%过氧化氢溶液于试管中,进行如下实验: (1)填写下表: 步骤③现象 步骤⑥结果 步骤⑦操作 结论 ,带火星的木条复燃 在过氧化氢溶液的分解反应中,氧化铜也能作催化剂 (2)步骤①的目的是 。 (3)步骤④对应的实验操作是 ,需用到的玻璃仪器有 。 【拓展探究】设计如下四组实验,比较二氧化锰和氧化铜对过氧化氢溶液分解的催化作用,其中观察效果最差的是 (选填序号)。 第一组 第二组 第三组 第四组 A.第一组同时实验,观察比较反应过程中两个气球体积的变化 B.第二组同时实验,观察比较反应过程中两个试管内产生气泡的快慢 C.第三组分两次实验,看木条是否能复燃 D.第四组分两次实验,比较收集一定体积的气体所需要的时间 5.达州盛产天然气,有“中国气都”之称的美誉.天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与: 【提出问题】:甲烷燃烧后生成哪些物质? 【查阅资料】:含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。 【猜想与假设】:甲 CO2 H2O;乙 CO H2O;丙 NH3CO2 H2O;丁 CO2 CO H2O。 你认为 同学的猜想是错误的,理由是 。 【实验探究】:为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过如图所示装置: (1)A、B装置的顺序能否颠倒?(填“能“或“否”) 。 (2)实验中用纯净O2而不用空气的原因是 。 (3)实验中观察到A中无水CuSO4变蓝,B、D中澄清石灰水变浑浊,C中红色粉末变成黑色,由此推断 同学猜想成立。 (4)请写出B中澄清石灰水变浑浊、C中红色粉末变成黑色的化学方程式: 、_______________________________________________。 【反思与交流】:为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是 _____________________________________。 6.英国科学家法拉第在《蜡烛的故事》系列讲座中,对蜡烛燃烧所涉及的知识进行了全面介绍.生产蜡烛的主要原料是石蜡和少量的硬脂酸添加剂等有机物,现在让我们一起对蜡烛原料的组成元素进行探究. (1)写出C不完全燃烧的化学方程式: . [提出问题]生产蜡烛的原料中主要有哪些元素? [假设与猜想]主要原料为有机物,猜想: (2)①一定有 元素;②可能还有氢元素和氧元素. [实验设计]据上述三种元素的猜想制订实验方案. 实验一:如图1所示,在蜡烛火焰上方放置一块洁净、干燥的玻璃片,一会儿观察到玻璃片上生成一些细小的水珠. 实验二;如图2所示,在蜡烛火焰上方罩一个内壁附着有澄清石灰水的烧杯,观察现象. [证据与结论](3)实验一,观察到玻璃片上有细小水珠时,说明原料中一定存在(填元素符号) .实验二,观察到烧杯内壁附着的 ,则猜想①成立. [分析与交流](4)实验一和实验二获得的证据均不能证明原料中一定存在________元素,因为 . (5)写出C的两条化学性质 . 7.某校化学兴趣小组将用剩的过氧化氢溶液倒入放有生锈铁钉的废液缸中,发现产生了大量的气泡,经检验此气体为氧气.根据学过的知识初步判断,是生锈铁钉中的某种物质加快了过氧化氢的分解,那么究竟是哪种物质加快了过氧化氢的分解速率?请你参与他们的研究,分享和体验探究实验的快乐. [猜想与假设] 甲同学:铁钉表面的氧化铁加快了H2O2的溶液分解. 乙同学:铁钉里的 加快了H2O2的溶液分解. [设计方案和实验] 完成下列表格 实验方案 实验现象 结论 方案一:向盛有10mL 5% H2O2溶液的试管中 加入2g 氧化铁粉末,将一根带火星的木条放 在试管口,观察现象. 甲同学结论成立. 方案二:向盛有10mL 5% H2O2溶液的试管中加入 粉末,将一根带火星的木条放在试管口,观察现象. 乙同学结论 . (填“成立”或“不成立”) [讨论交流] 丙同学认为“方案一”只能说明Fe2O3加快了H2O2溶液的分解,并不能说Fe2O3就一定是催化剂.你是否支持丙同学的观点? ,如果要证明氧化铁是催化剂,就要设计一个实验来证明,这个实验的设计原理是 . (提示:下面小题若答对将奖励4分.) [反思与评价] 丁同学仔细观察“方案二”中一直没有现象的试管,过了一段时间后发现试管中也产生了气体,丁同学对此现象进行深入思考和分析,得出可能的原因,你能想出其中的原吗? 。 8.天然气的主要成分是甲烷(CH4),我校化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,请你参与 【提出问题】甲烷燃烧后生成哪些物质? 【查阅资料】含碳元素的物质完全燃烧生成CO2,不完全燃烧生成CO;无水CuSO4遇水变蓝。 【猜想与假设】 甲 CO2 、H2O ; 乙 CO、H2O; 丙 NH3、CO2 、H2O; 丁 CO2 、CO、H2O 。 你认为 同学的猜想是错误的,理由是 ________。 【实验探究】为了验证上述猜想与假设,将甲烷在一定量的O2中燃烧的产物依次通过下列装置: (1)若实验中观察到A中无水CuSO4变蓝,B、E中澄清石灰水变浑浊,D中红色粉末变成黑色,由此推断 同学猜想成立,请写出甲烷在此时燃烧的化学方程式 。 (2)A、B装置的顺序不能颠倒,其理由是 ,C装置的作用是 ; 【反思与交流】为避免有毒的CO污染环境,所以含碳元素的物质燃烧必须满足的条件是 ________________________________________________。 9 .在探究课上,老师给同学们一包黑色粉末,该粉末是由铁粉和氧化铜粉末中的一种或两种组成.为了确定该粉末的成分,同学们进行如下探究: 请回答下列问题: 【猜想假设】(1)黑色粉末是铁粉 (2)黑色粉末是氧化铜粉末 (3)黑色粉末是铁粉和氧化铜粉末 【设计方案】取少量黑色粉末,放入硬质玻璃管中,通入一氧化碳气体,片刻后加热充分反应(实验装置如图所示) 请填写下表空白:(不考虑铁粉和氧化铜粉末可能发生反应) 实验中可能出现的现象 结论 猜想(1)成立 黑色粉末全部变红,澄清的石灰水变浑浊 猜想(2) (填成立或不成立) 猜想(3)成立 【实验结论】经过分析实验现象,确认猜想(3)成立. 【反思评价】 (1)实验完毕后,先停止加热,继续通入一氧化碳直至玻璃管冷却至室温.继续通入一氧化碳的目的是 . (2)从环保角度上看,上述设置有不足之处,改进措施是 . (3)猜想(2)玻璃管中发生反应的化学方程式是 ________________. 1. (1)a:6% b:MnO2 (2)和实验1进行对比,确定MnO2的催化作用 (3)实验3证实固体剩余物中没有二氧化锰,可能是分解后产物中其他物质起催化作用 (4)6.48g 2.16g 2.16g~3.24g 2. 实验一【结论】慢;化学方程式:2H2O22H2O+ O2↑ 实验二【结论】二氧化锰不能催化分解水 。 实验三 【实验操作】:向盛有过氧化氢溶液的试管中加入二氧化锰,伸入带火星的木条 【实验现象】:有气泡产生,木条复燃。 (1)【作用】对比作用 (2)【目的】证明二氧化锰的质量没有改变 【实验操作】向试管剩余物中再加入过氧化氢溶液 3.【实验验证】 实验步骤 实验现象 实验结论 实验一 将带火星的木条伸入装有过氧化氢溶液的试管中 实验二 Al2O3能加快过氧化氢的分解速率 实验三: 【实验目的】Al2O3在反应前后质量是否改变。 【实验步骤】干燥. 【提出新的问题】Al2O3的化学性质在反应前后是否改变. 4.D 【进行实验】 (1)有大量气泡产生 固体质量仍为0.2g 将固体加入盛有5mL5%过氧化氢溶液的试管中,并把带火星的木条伸入试管,观察现象 (2)与步骤③对比,检验加入氧化铜前后过氧化氢溶液的分解速率有无变化 (3)过滤 烧杯、玻璃棒、漏斗 【拓展探究】C 5.【猜想与假设】丙 化学反应前后元素的种类不变而反应前不含氮元素,生成物中不可能生成氨气 【实验探究】(1)否 (2)空气中含有CO2和H2O(干扰对产物的鉴别) (3)丁 (4)CO2+Ca(OH)2=CaCO3↓+H2O Fe2O3+3CO高温 = 2Fe+3CO2 【反思与交流】氧气充足 6.(1)2C+O22CO; (2)碳; (3)H;澄清石灰水变浑浊; (4)O;蜡烛燃烧时与空气中氧气反应,反应物提供了氧元素; (5)可燃性(氧化性)、还原性. 7. 【猜想与假设】铁; 【设计方案和实验】有大量气泡产生,带火星木条复燃;铁;不成立; 【讨论交流】支持;设计实验验证Fe2O3在反应前后质量和化学性质是否改变; 【反思与评价】可能是铁被过氧化氢溶液氧化成氧化铁,后来氧化铁催化过氧化氢溶液分解或可能是铁钉中碳被过氧化氢溶液氧化,其产物催化过氧化氢溶液分解. 8.丙 化学反应前后元素的种类不变(或质量守恒定律) (1)丁 4CH4+7O2点燃2CO2+2CO+8H2O (2)澄清石灰水能挥发出水蒸气,会影响水的鉴别 除去二氧化碳,以免其对一氧化碳的鉴别造成干扰 充足的氧气,使燃料充分燃烧 9.【设计方案】 实验中可能出现的现象 结论 黑色粉末不变红,澄清的石灰水不变浑浊 猜想(1)成立 黑色粉末全部变红,澄清的石灰水变浑浊 猜想(2)成立(填成立或不成立) 黑色粉末部分变红,澄清的石灰水变浑浊 猜想(3)成立 【反思评价】(1)防止生成的铜再次被氧化(合理说法均可); (2)在b处放一只燃着的酒精灯(或安装尾气处理装置或在b处导管处绑一个小气球等); (3)CO+CuOCu+CO2.查看更多