- 2021-04-14 发布 |
- 37.5 KB |
- 6页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
鲁教版九年级化学第五单元测试题含答案
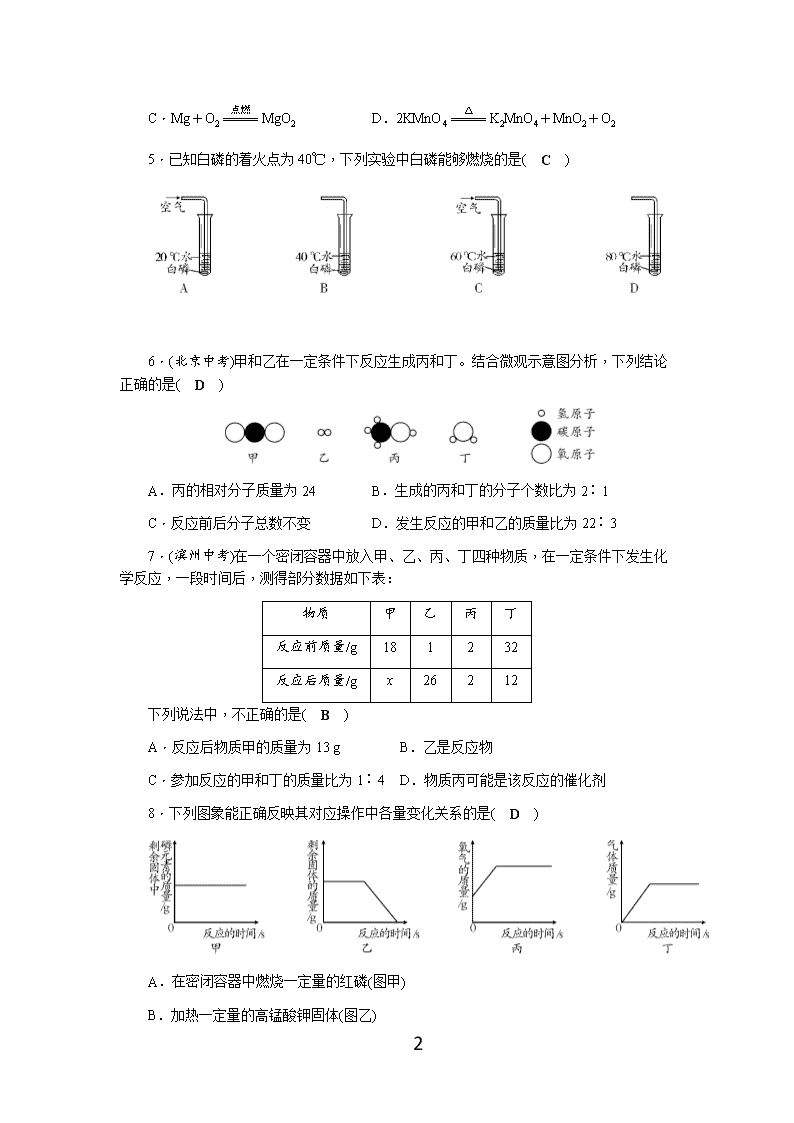
鲁教版九年级化学第五单元测试题含答案 (时间:60分钟 满分:75分) 可能用到的相对原子质量:H—1 C—12 O—16 S—32 第Ⅰ卷 (选择题 24分) 一、选择题(本题共8小题,每小题3分,共24分。每小题只有一个选项符合题意) 1.下列关于质量守恒定律说法正确的是( D ) A.参加反应的氢气和氧气的体积,一定等于生成水的体积 B.100 g冰融化得到100 g水,符合质量守恒定律 C.高锰酸钾加热后固体质量减少,说明这一反应不符合质量守恒定律 D.镁条燃烧后,生成物质量比镁条的质量大,该反应符合质量守恒定律 2.(南充中考)小明同学从S+O2SO2中获得以下信息:①该反应中反应物是硫和氧气;②该反应发生的条件是点燃;③反应前后元素种类和原子个数保持不变;④反应前后分子总数保持不变;⑤参加反应的硫和氧气的质量比为2∶1。其中正确的信息是( B ) A.①②④⑤ B.①②③ C.④⑤ D.①②③⑤ 3.下图所示的四位同学正在讨论某一化学方程式表示的意义,他们所描述的化学方程式是( C ) A.C+O2CO2 B.CH4+2O2CO2+2H2O C.2CO+O22CO2 D.2H2+O22H2O 4.下列化学方程式书写完全正确的是( A ) A.C+O2CO2 B.4Fe+3O22Fe2O3 6 C.Mg+O2MgO2 D.2KMnO4K2MnO4+MnO2+O2 5.已知白磷的着火点为40℃,下列实验中白磷能够燃烧的是( C ) 6.(北京中考)甲和乙在一定条件下反应生成丙和丁。结合微观示意图分析,下列结论正确的是( D ) A.丙的相对分子质量为24 B.生成的丙和丁的分子个数比为2∶1 C.反应前后分子总数不变 D.发生反应的甲和乙的质量比为22∶3 7.(滨州中考)在一个密闭容器中放入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,一段时间后,测得部分数据如下表: 物质 甲 乙 丙 丁 反应前质量/g 18 1 2 32 反应后质量/g x 26 2 12 下列说法中,不正确的是( B ) A.反应后物质甲的质量为13 g B.乙是反应物 C.参加反应的甲和丁的质量比为1∶4 D.物质丙可能是该反应的催化剂 8.下列图象能正确反映其对应操作中各量变化关系的是( D ) A.在密闭容器中燃烧一定量的红磷(图甲) B.加热一定量的高锰酸钾固体(图乙) 6 C.在少量二氧化锰中加入双氧水(图丙) D.加热一定量的氯酸钾和二氧化锰的混合物(图丁) 第Ⅱ卷 (非选择题 51分) 二、填空题(本题共6小题,化学方程式每个2分,其余每空1分,共27分) 9.(4分)某学生书写出以下化学方程式: ①HgO2Hg+O2↑ ②P2+O2P2O5 ③C+O2CO2↑ ④Mg+O2===MgO2 ⑤3Fe+2O2↑===Fe3O4 ⑥H2+O2H2O↓ 你帮助检查一下,将其中有如下错误的化学方程式的序号填入相应的横线上。 (1)化学式写错的是 ②④ ; (2)未配平的是 ①⑥ ; (3)“↑”“↓”符号使用不当的是 ③⑤⑥ ; (4)反应条件写错或漏写的是①④⑤ 。 10.(6分)写出下列反应的化学方程式。 (1)镁条在空气中燃烧生成氧化镁 2Mg+O22MgO 。 (2)氢气在空气中燃烧: 2H2+O22H2O 。 (3)实验室加热高锰酸钾制取氧气: 2KMnO4K2MnO4+MnO2+O2↑ 。 11.(4分)配平下列化学方程式。 (1) 4 NH3+ 3 O2 2 N2+ 6 H2O (2) 1 C2H6O+ 3 O2 2 CO2+ 3 H2O 12.(3分)如图所示是某密闭容器中物质变化过程的微观示意图: 6 (1)A、B、C中表示混合物的是 A 。 (2)上述变化Ⅰ、Ⅱ和Ⅲ中,属于化学变化的是 Ⅰ ,该化学变化中一定不变的粒子是 碳原子和氧原子 (填粒子名称)。 13.(5分)把A、B、C、D四种纯净物放在一密闭容器中反应,反应前后各物质的质量如下表: A B C D 反应前质量/g 28 6 2 4 反应后质量/g 2 6 12 未知 (1)该反应生成物是 CD ,B可能是 催化剂 ,反应后D的质量是 20 g。 (2)该反应属于哪种基本反应类型: 分解反应 。 (3)物质A是 化合物 (填“单质”或“化合物”)。 14.(5分)将16g硫在定量的氧气中燃烧,有如下实验数据:(S+O2SO2) 第一次实验 第二次实验 第三次实验 给定氧气的质量/g 15 16 20 生成二氧化硫的质量/g 30 32 32 (1)在三次实验中,第 二 次恰好完全反应; (2)第 一 次实验中硫有剩余,剩余 1 g; (3)第 三 次实验中氧气有剩余,剩余 4 g。 三、实验与探究题(本题共2小题,化学方程式每个2分,其余每空1分,共17分) 15.(6分)质量守恒定律的定量研究对化学科学发展具有重大意义。 (1)我国从2011年5月1日起,酒驾入刑。“酒精检测仪”可检查司机是否酒后驾车,其反应原理为C2H5OH+4CrO3+6H2SO4===2Cr2(SO4)3+2CO2↑+9X,反应中红色的CrO3转变为绿色的Cr2(SO4)3,其中X的化学式为 H2O 。 (2)如图为某化学反应的微观模拟图,“”和“●”分别表示两种不同元素的原子: 由“”聚集成的物质 可能 (填“可能”或“不可能”)是氧化物, 6 参加反应的两种反应物的分子个数比为 2∶1 ,此反应的基本反应类型为 化合反应 。 (3)已知m1 g镁条放在空气中完全燃烧,生成m2 g氧化镁(不考虑其他反应),m1 <__(填“>”“<”或“=”)m2。小西在做该实验时,观察到耀眼的白光,冒出大量白烟,称量无误时,发现m1 >m2,其原因是 镁条燃烧产生的氧化镁部分以白烟的形式逸散到空气中去了 。 16.(11分)小明和小芳在学习了“质量守恒定律”后,到实验室想亲自探究其他化学反应是否也遵循质量守恒定律,小明和小芳分别做了A、B所示的实验。 (1)分别写出A、B实验中发生反应的化学方程式: A. Fe+CuSO4===FeSO4+Cu ; B. Na2CO3+2HCl===2NaCl+H2O+CO2↑ 。 (2)小明在实验A中观察到的现象:① 铁钉上有红色物质生成,溶液由蓝色变为浅绿色;② 天平仍保持平衡 ;小芳在实验B中观察到的现象:③ 有大量气泡产生 ;④天平失去平衡,指针偏右 。 (3)小明和小芳根据各自不同的实验现象得出不同的结论。①小明认为:在化学反应中,生成物的总质量等于反应物的总质量;②小芳认为:在化学反应中,生成物的总质量与反应物的总质量不相等。 (4)你认为 小明 的结论正确,导致另一个实验结论错误的原因是 反应生成的气体逸散到空气中去了 。由此可知,验证质量守恒定律成功的关键是 化学反应在密闭的体系中进行或无内外气体交换 。 四、计算题(本题共1小题,共7分) 17.(南充中考)某化学兴趣小组欲测定一瓶过氧化氢溶液中溶质的质量分数,实验操作及相关数据如图所示: (1)生成氧气的质量为 1.6 g。 (2)这瓶过氧化氢溶液中溶质的质量分数是多少?(写出计算过程) 6 解:(1)根据质量守恒定律,反应生成氧气的质量:68 g+2 g-68.4 g=1.6 g; (2)设68 g过氧化氢溶液中含有过氧化氢的质量为x。 2H2O22H2O+O2↑ 68 32 x 1.6 g = 解得x=3.4 g 过氧化氢溶液溶质的质量分数为×100%=5% 6查看更多