- 2021-04-13 发布 |
- 37.5 KB |
- 9页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
化学卷·2018届福建省惠安惠南中学高二5月月考(2017
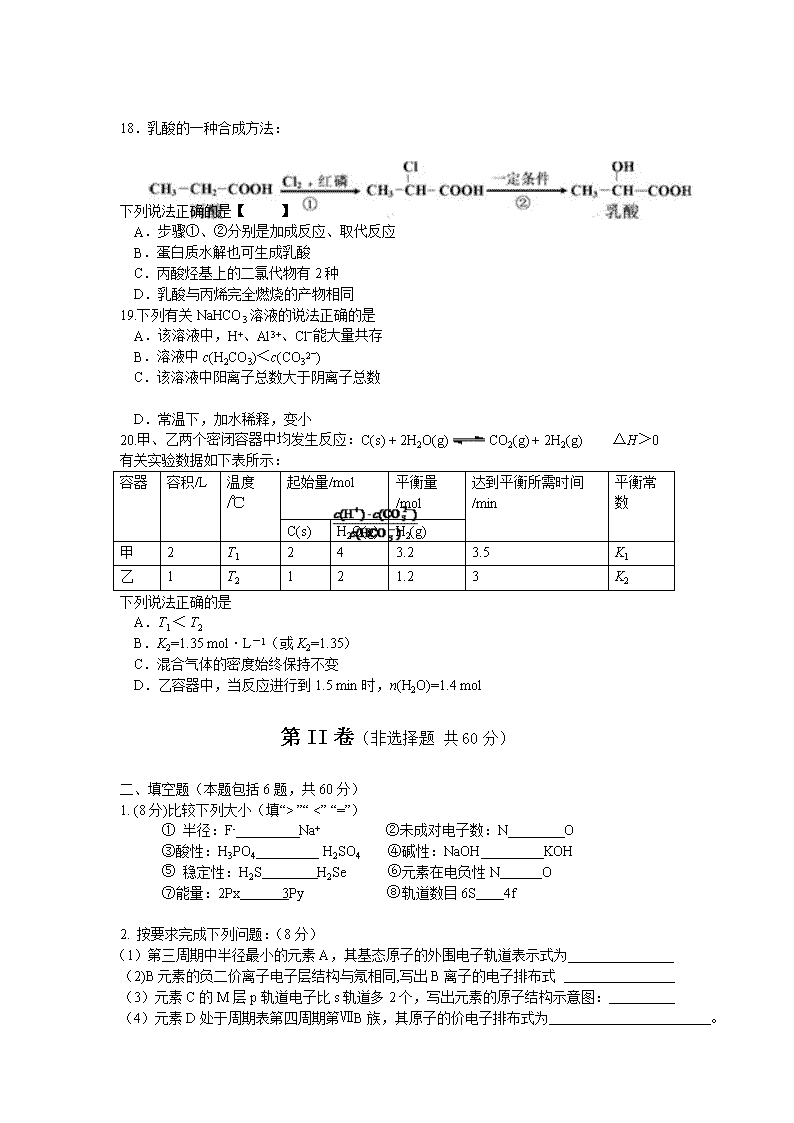
泉州台商投资区惠南中学2017年5月月考试卷 高二化学 命题人:骆培蓉 考试时间:100分钟 满分:100分 2017.5.28 班级 座号 姓名 第Ⅰ卷(选择题 共40分) 一、选择题(本题共20小题,每小题2分,共40分,每题只有一个正确选项) 1、在物质结构研究的历史上,首先提出原子中有原子核的科学家是【 】 A.卢瑟福 B.玻尔 C.汤姆生 D.普朗克 2. 下列关于氢原子电子云图的说法中正确的是【 】 A.黑点密度大,电子数目大 B.黑点密度大,单位体积内电子出现的概率大 C.电子云图是对电子运动无规律性的描述 D.一个小黑点表示一个电子 3. 下列说法中正确的是【 】 A.3p2表示3p能级有两个轨道 B.M能层中的原子轨道数目为3 C.1s22s12p1表示的是激发态原子的电子排布 D.处于同一轨道上的电子可以有多个,它的运动状态完全相同 4.原子轨道按能量由低到高的顺序排列,正确的一组是 【 】 A.2p、3d、4s B.2p、3s、3p C. 2s、3s、2p D. 4s、3p、4p 5.某原子核外共有6个电子,分布在K与L电子层上,在下列L层分布中正确的是 【 】 A. B. C. D. 6.下列化学用语的书写,正确的是 【 】 A.Br-的电子排布式[Ar] 3d104s24p6 B.硫原子的结构示意图: C.溴化钠的电子式: D.N原子的轨道表示式: 7.下列原子中的未成对电子数最多的是 【 】 A.氮(N) B.硒(Se) C.铬(Cr) D.锰(Mn) 8.在下列所示的微粒中,原子半径最大的是 【 】 A.1S22S22P2 B.1S22S22P5 C.1S22S22P63S1 D.1S22S22P63S23P2 9.下列原子或离子的基态电子排布式正确的是【 】 A.Ni:[Ar]3d8 B.Cu:[Ar]3d94s2 C.S2-:[Ne]2s23p6 D.Si:[Ne]3s23p2 10.若某基态原子的外围电子排布为4d25s2,则下列说法正确的是【 】 A.该元素位于周期表第5周期第IIB族 B.该元素原子核外有4个电子层 C.该元素原子M层上共有8个电子 D.该元素原子最外层共有2个电子 11.具有如下电子层结构的原子,其相应元素一定属于同一主族的是 【 】 A.3p轨道上有2个未成对电子的原子和4p轨道上有2个未成对电子的原子 B.3p轨道上只有1个空轨道的原子和4p轨道上只有1个空轨道的原子 C.最外层电子排布为3s2的原子和最外层电子排布为4s2的原子 D.最外层电子排布为ls2的原子和最外层电子排布为2s2的原子 122,4,6 .W、X、Y、Z均为短周期主族元素,原子序数依次增加,X与Y形成的化合物能与水反应生成酸且X、Y同主族,两元素核电荷数之和与W、Z的原子序数之和相等,则下列说法正确的是【 】 A.Z元素的含氧酸是最强酸 B.原子半径:X > Z C.气态氢化物热稳定性:W >X D.W与Y可以存在于同一离子化合物中 13.按电子排布,可把周期表里的元素划分成5个区,以下元素属于S区的是【 】 A.Fe B.Mg C.S D.Cr 14. 下表列出了某短周期元素R的各级电离能数据(用I1、I2……表示,单位为kJ/mol)。 I1 I2 I3 I4 …… R 740 1500 7700 10500 …… 下列关于元素R的判断中一定正确的是【 】 A.R的最高正价为+3价 B.R元素位于元素周期表中第ⅡA族 C.R元素的原子最外层共有4个电子 D.R元素基态原子的电子排布式为1s22s2 15.下列各组元素中,电负性依次减小的是 【 】 A.K、Na、Al B.O、S、P C.As、P、N D.O、Si、F 16.X、Y为两种元素的原子,X的阴离子与Y的阳离子具有相同的电子层结构,由此可知 【 】 A.X的原子半径大于Y的原子半径 B.X的电负性大于Y的电负性 C.X的氧化性大于Y的氧化性 D.X的第一电离能大于Y的第一电离能 17.茅台酒中存在少量具有凤梨香味的物质X,其结构如右下图所示。下列说法正确的是 A.X难溶于乙醇 B.酒中的少量丁酸能抑制X的水解 C.分子式为C4H8O2且官能团与X相同的物质有5种 D.X完全燃烧后生成CO2和H2O的物质的量比为1∶2 18.乳酸的一种合成方法: 下列说法正确的是【 】 A.步骤①、②分别是加成反应、取代反应 B.蛋白质水解也可生成乳酸 C.丙酸烃基上的二氯代物有2种 D.乳酸与丙烯完全燃烧的产物相同 19.下列有关NaHCO3溶液的说法正确的是 A.该溶液中,H+、Al3+、Cl‾能大量共存 B.溶液中c(H2CO3)<c(CO32‾) C.该溶液中阳离子总数大于阴离子总数 D.常温下,加水稀释,变小 20.甲、乙两个密闭容器中均发生反应:C(s) + 2H2O(g) CO2(g) + 2H2(g) △H>0 有关实验数据如下表所示: 容器 容积/L 温度/℃ 起始量/mol 平衡量/mol 达到平衡所需时间/min 平衡常数 C(s) H2O(g) H2(g) 甲 2 T1 2 4 3.2 3.5 K1 乙 1 T2 1 2 1.2 3 K2 下列说法正确的是 A.T1 < T2 B.K2=1.35 mol·L-1(或K2=1.35) C.混合气体的密度始终保持不变 D.乙容器中,当反应进行到1.5 min时,n(H2O)=1.4 mol 第II卷(非选择题 共60分) 二、填空题(本题包括6题,共60分) 1. (8分)比较下列大小(填“> ”“ <” “=”) ① 半径:F- Na+ ②未成对电子数:N O ③酸性:H3PO4 H2SO4 ④碱性:NaOH KOH ⑤ 稳定性:H2S H2Se ⑥元素在电负性N O ⑦能量:2Px 3Py ⑧轨道数目6S 4f 2. 按要求完成下列问题:(8分) (1)第三周期中半径最小的元素A,其基态原子的外围电子轨道表示式为 (2)B元素的负二价离子电子层结构与氖相同,写出B离子的电子排布式 (3)元素C的M层p轨道电子比s轨道多2个,写出元素的原子结构示意图: (4)元素D处于周期表第四周期第ⅦB族,其原子的价电子排布式为 。 (5)某元素E的激发态原子的电子排布式为1s22s22p63s23p34s1,则该元素基态原子的电子排布式为 ; (6)元素F在基态原子核外有8个原子轨道占满了电子,则该原子电子排布式是: (7)G元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子,G的元素符号为________,其基态原子的电子排布式为_______________________。 3. (9分)根据下列五种元素的第一至第四电离能数据(单位:kJ·mol-1),回答下列各题: 元素代号 I1 I2 I3 lI4 Q 2080 4000 6100 9400 R 500 4600 6900 9500 S 740 1500 7700 10500 T 580 1800 2700 11600 U 420 3100 4400 5900 (1)在周期表中,最可能处于同一族的是________。 A.Q和R B.S和T C.T和U D.R和T E.R和U (2)下列离子的氧化性最弱的是________。 A.S2+ B.R2+ C.T3+ D.U+ (3)下列元素中,化学性质和物理性质最像Q元素的是________。 A.硼 B.铍 C.氦 D.氢 (4)每种元素都出现相邻两个电离能的数据相差较大的情况,这一事实从一个侧面说明: _______ ________________________________________________________________________。 (5)如果R、S、T是同周期的三种主族元素,则它们的原子序数由小到大的顺序是_______,其中元素________的第一电离能异常高的原因是________________________________________。 4. (9分)W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。 (1)W位于元素周期表第________周期第_____ _族。W的气态氢化物稳定性比H2O(g)________(填“强”或“弱”)。 (2)Y基态原子核外电子排布式是_______ _ ,Y原子半径比X的___ (填“大”或“小) (3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是 ________________________________________________________________________。 (4)已知下列数据:Fe(s)+O2(g)===FeO(s) ΔH=-272 kJ·mol-1 2X(s)+O2(g)===X2O3(s) ΔH=-1 676 kJ·mol-1 X的单质和FeO反应的热化学方程式是_________________________________________。 5. (12分)某研究小组采用矿浆电解法从复杂锑铅矿(主要成分为Sb2S3、PbS、FeS)提取金属锑,实现了锑、铅的一步分离。其工艺流程图如下: 已知:①Sb3+ + 6Cl‾ SbCl63‾ ② 物质 Sb2S3 PbS FeS PbCl2 PbCO3 Ksp 2×10‾93 1×10‾28 6×10‾18 1.6×10‾5 7.4×10‾14 (1)加入NH4Cl可以提高电解时SbCl3在阳极区的溶解度,理由是 。 (2)Sb2S3在阳极区因硫元素被氧化而溶解,写出电极反应式 ;Sb2S3也可以被电解生成的Fe3+溶解,反应的离子方程式为 。 (3)阳极渣中含铅化合物的化学式为 。 (4)步骤Ⅱ反应选择在40~ 50℃进行,温度不宜过高的原因是 (5)单质硫在煤油中的溶解度曲线如图。利用煤油为溶剂将滤渣中的碳酸铅和单质硫分离,步骤Ⅲ的操作方法是: 。 (6)步骤Ⅳ,先加入NaClO3试剂将Fe2+转化为Fe2O3·nH2O除去,则氧化剂和还原剂的物质的量之比为 。 6.(14分)有机物F是一种香料,其合成路线如图所示: (1)A的名称为 ,试剂X的结构简式为 ,步骤Ⅵ的反应类型为 。 (2)步骤Ⅰ的反应试剂和条件分别为 、 。 (3)步骤Ⅱ反应的化学方程式为 。 (4)满足下列条件的E的同分异构体有 种,其中核磁共振氢谱峰面积比为 6︰2︰2︰1︰1的分子的结构简式为 。 ①苯环上只有两个取代基 ②能与FeCl3溶液发生显色反应 ③能发生水解反应和银镜反应 (5)依据题中信息,完成以 为原料制取 的合成路线图。 合成路线图示例如下: SK 试 卷 分 析 S型错误(技能型错误) K型错误(知识型错误) 错误类型 涉及题序 失分 错误内容 涉及题序 失分 审题错误 推理错误 计算错误 书写错误 惠泉州台商投资区惠南中学2017年5月月考试卷 高二化学 题号 1 2 3 4 5 6 7 8 9 10 答案 题号 11 12 13 14 15 16 17 18 19 20 答案 第II卷(非选择题 共60分) 二、填空题(本题包括6题,共60分) 1.① ② ③ ④ ⑤ ⑥ ⑦ ⑧ 2.⑴ ⑵ ⑶ ⑷ ⑸ ⑹ ⑺ , 3.⑴ ⑵ ⑶ ⑷ ⑸ , , 4.⑴ , , ⑵ , ⑶ ⑷ 5.⑴ ⑵ , ⑶ ⑷ ⑸ ⑹ 6. ⑴ , , ⑵ , ⑶ ⑷ , ⑸ 1.① < ② 〉 ③ < ④ < ⑤ > ⑥ < ⑦ = ⑧ < 2.⑴ ⑵ 1s22s22p6 ⑶ ⑷ 3d54s2 ⑸ 1s22s22p63s23p4 ⑹ 1s22s22p63s23p2 ⑺ Se , 1s22s22p63s23p63d104s24p4 3.⑴ E ⑵ D ⑶ C ⑷ 电子分层排布,且各能层能量不同 ⑸ R<S<T,S, S元素的第一电离能失去的是s能级的电子,s能级为全满稳定结构、能量降低. 4.⑴ 二;ⅤA , 弱 ⑵ 1s22s22p63s23p63d9 , 小 ⑶ 2H2SO4(浓)+Cu ==== CuSO4+SO2↑+2H2O, ⑷ 3FeO(s)+2Al(s)=Al2O3(s)+3Fe(s)?△H=-859.7KJ/mol. 5. (1)提高氯离子浓度,使Sb3+ + 6Cl-SbCl63-正向移动 (2)Sb2S3 + 12Cl--6e- = 3S + 2SbCl63-或Sb2S3-6e- = 3S + 2Sb3+ 6Fe3+ + Sb2S3 + 12Cl- = 6Fe2+ + 3S + 2SbCl63-或6Fe3+ + Sb2S3 = 3S + 2Sb3+ + 6Fe2+ (3)PbCl2 (4)防止NH4HCO3分解 (5)用热煤油溶解,趁热过滤;将滤液冷却,过滤 (说明:“用热煤油溶解,趁热过滤”2分,“将滤液冷却,过滤”1分) (6)1︰6 6. (1)甲苯 CH3CHClCOOH 取代反应或酯化反应 (2)Cl2、光照 (3)C6H5-CH2Cl + NaOH C6H5-CH2OH + NaCl (4)15; (5) 查看更多