- 2021-04-13 发布 |
- 37.5 KB |
- 18页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
高考化学离子反应试题汇编
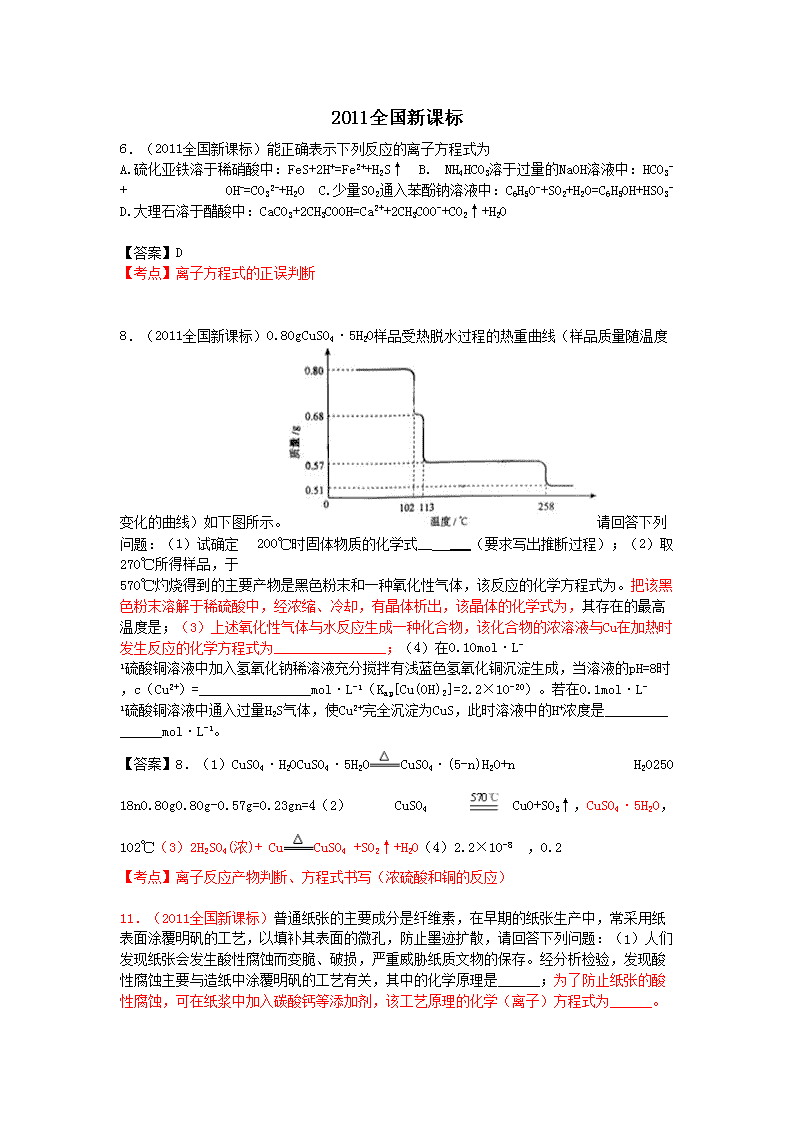
2011-2015全国卷汇编---离子反应(索引) 2011-2015全国卷汇编---离子反应(题目) 考点 题号 离子方程式的正误判断 2011全国新课标:6 2013全国新课标II:4 离子方程式的书写 2011全国新课标:11(1)、11(2)② 2012全国新课标:8(3)(4) 2013全国新课标I:9(2) 2013全国新课标II:9(1)、11(2)② 2014全国新课标I:9(3)、11(2) 2014全国新课标II:9(3)、11 2015全国新课标I:36(2) 2015全国新课标Ⅱ:13、26、28 离子反应方程书写 2011全国新课标:8(3) 2013全国新课标I:10(1)、12(4) 2015全国新课标I:27(1) 离子反应及其发生的条件(包括除杂、离子 检验、产物判断、现象分析) 2011全国新课标:8(2)、13 2012全国新课标:1、8(2) 2013全国新课标I:9(4)、11(2) 2013全国新课标II:9(1)(3) 2014全国新课标I:2、11(4) 2014全国新课标II:3、7 2015全国新课标I:10 2015全国新课标I:27(3)、36(3) 2015全国新课标Ⅱ:26、28 电解质化学式的书写 2013全国新课标I:9(6)、11(5) 电离方程式的书写 2014全国新课标I:9(1) 2011全国新课标 6.(2011全国新课标)能正确表示下列反应的离子方程式为 A.硫化亚铁溶于稀硝酸中:FeS+2H+=Fe2++H2S↑ B. NH4HCO3溶于过量的NaOH溶液中:HCO3- + OH-=CO32-+H2O C.少量SO2通入苯酚钠溶液中:C6H5O-+SO2+H2O=C6H5OH+HSO3- D.大理石溶于醋酸中:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O 【答案】D 【考点】离子方程式的正误判断 8.(2011全国新课标)0.80gCuSO4·5H2O样品受热脱水过程的热重曲线(样品质量随温度 变化的曲线)如下图所示。 请回答下列问题:(1)试确定 200℃时固体物质的化学式__ ___(要求写出推断过程);(2)取 270℃所得样品,于 570℃灼烧得到的主要产物是黑色粉末和一种氧化性气体,该反应的化学方程式为。把该黑 色粉末溶解于稀硫酸中,经浓缩、冷却,有晶体析出,该晶体的化学式为,其存在的最高 温度是;(3)上述氧化性气体与水反应生成一种化合物,该化合物的浓溶液与Cu在加热时 发生反应的化学方程式为________________;(4)在0.10mol·L- 1硫酸铜溶液中加入氢氧化钠稀溶液充分搅拌有浅蓝色氢氧化铜沉淀生成,当溶液的pH=8时 ,c(Cu2+)=________________mol·L-1(Kap[Cu(OH)2]=2.2×10-20)。若在0.1mol·L- 1硫酸铜溶液中通入过量H2S气体,使Cu2+完全沉淀为CuS,此时溶液中的H+浓度是_________ ______mol·L-1。 【答案】8.(1)CuSO4·H2OCuSO4·5H2O CuSO4·(5-n)H2O+n H2O250 18n0.80g0.80g-0.57g=0.23gn=4(2) CuSO4 CuO+SO3↑,CuSO4·5H2O, 102℃(3)2H2SO4(浓)+ Cu CuSO4 +SO2↑+H2O(4)2.2×10-8 ,0.2 【考点】离子反应产物判断、方程式书写(浓硫酸和铜的反应) 11.(2011全国新课标)普通纸张的主要成分是纤维素,在早期的纸张生产中,常采用纸 表面涂覆明矾的工艺,以填补其表面的微孔,防止墨迹扩散,请回答下列问题:(1)人们 发现纸张会发生酸性腐蚀而变脆、破损,严重威胁纸质文物的保存。经分析检验,发现酸 性腐蚀主要与造纸中涂覆明矾的工艺有关,其中的化学原理是______;为了防止纸张的酸 性腐蚀,可在纸浆中加入碳酸钙等添加剂,该工艺原理的化学(离子)方程式为______。 (2)为了保护这些纸质文物,有人建议采取下列措施:①喷洒碱性溶液,如稀氢氧化钠溶 液或氨水等,这样操作产生的主要问题是______。②喷洒Zn(C2H5)2。Zn(C2H5)2可以与水反 应生成氧化锌和乙烷。用化学(离子)方程式表示该方法生成氧化锌及防治酸性腐蚀的原 理______。(3)现代造纸工艺常用钛白粉(TiO2)替代明矾。钛白粉的一种工业制法是以钛 铁矿(主要成分FeTiO3)为原料按下列过程进行的,请完成下列化学方程式:①□FeTiO3+ □C+□Cl2 □TiCl4+□FeCl3+□CO②□TiCl4+□O2 □TiO3+□Cl2 【答案】(1)明矾水解产生酸性环境,在酸性条件下,纤维素水解,使高分子链断裂;CaCO 3+2H+=Ca2++CO2↑+H2O(2)①过量的碱同样可以导致纤维素的水解,造成书籍污损。②Zn(C2H 5)2+H2O=ZnO+ 2 C2H6↑,ZnO+2H+=Zn2++H2O (3)①2FeTiO3+ 6C+7Cl2 2TiCl4+2FeCl3+6CO②TiCl4+O2 TiO3+2Cl2 【考点】离子方程式的书写 13.(2011全国新课标)香豆素是一种天然香料,存在于黑香豆、兰花等植物中。工业上 常用水杨醛与乙酸酐在催化剂存在下加热反应制得: 以下是由甲苯为原料生产香豆素的一种合成路线(部分反应条件及副产物已略去) 已知以下信息:①A中有五种不同化学环境的氢;②B可与FeCl3溶液发生显色反应;③同一 个碳原子上连有两个羧基通常不稳定,易脱水形成羰基。请回答下列问题:(1)香豆素的分 子式为_______;(2)由甲苯生成A的反应类型为___________;A的化学名称为__________; (3)由B生成C的化学反应方程式为___________;(4)B的同分异构体中含有苯环的还有_____ _种,其中在核磁共振氢谱中只出现四组峰的有_______种;(5)D的同分异构体中含有苯环 的还有______中,其中:①既能发生银境反应,又能发生水解反应的是________(写结构 简式)②能够与饱和碳酸氢钠溶液反应放出CO2的是_________(写结构简式) 【答案】13.(1)C9H6O2(2)取代反应,2-氯甲苯(邻氯甲苯)(3) (4)4,2(5)4, , 【考点】离子反应及其发生的条件 2012全国新课标 1.(2012全国新课标)下列叙述中正确的是 A.液溴易挥发,在存放液溴的试剂瓶中应加水封B.能使润湿的淀粉KI试纸变成蓝色的物 质一定是Cl2 C.某溶液加入CCl4,CCl4层显紫色,证明原溶液中存在I- D.某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ 【答案】A 【考点】离子反应及其发生的条件(现象分析) 8.(2012全国新课标)铁是应用最广泛的金属,铁的卤化物、氧化物以及高价铁的含氧酸 盐均为重要化合物。(1)要确定铁的某氯化物FeClx的化学式。可用离子交换和滴定的方 法。实验中称取 0.54g的FeClx样品,溶解后先进行阳离子交换预防处理,再通过含有饱和OH- 的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40mol·L- 1的盐酸滴定,滴至终点时消耗盐酸25.0mL。计算该样品中氯的物质的量,并求出FeClx中X 值(2)现有一含有FeCl2和FeCl3的混合样品,采用上述方法测得n(Fe): n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为____。在实验室中,FeCl2可用铁粉和__ __反应制备,FeCl3可用铁粉和_______反应制备(3)FeCl3与氢碘酸反应时可生成棕色物 质,该反应的离子方程式为___(4)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理 剂和高容量电池材料。FeCl3与KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式 为______与MnO2-Zn电池类似,K2FeO4- Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电极反应式为________,该电 池总反应的离子方程式为_____。 【答案】(1)n(Cl)= 0.0250L×0.40mol·L-1=0.010mol0.54g-0.010mol×35.5g·mol -1= 0.19gn(Fe)= 0.19g/ 56g·mol-1=0.0034moln(Fe): n(Cl)=0.0034:0.010≈1:3,x=3(2)0.10 盐酸 氯气(3)2Fe3++2I-=2Fe2++I2 (或2Fe3++3I-=2Fe2++I3-)(4)2Fe(OH)3+3ClO-+4OH-=2FeO42-+5H2O+3Cl-(5)FeO42-+3e- +4H2O= Fe(OH)3+5OH-;2FeO42-+8H2O+3Zn= 2Fe(OH)3+ 3Zn(OH)3+4OH- 【考点】离子反应及其发生的条件、离子方程式的书写、原电池反应离子方程式的书写 2013全国新课标Ⅰ 9.(2013全国高考)锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极 材料有钴酸锂(LiCoO2)、导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反 应为6C+xLi++xe- = LixC6。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。 回答下列问题:(1)LiCoO2中,Co元素的化合价为。(2)写出“正极碱浸”中发生反应 的离子方程式。(3)“酸浸”一般在80℃下进行,写出该步骤中发生的所有氧化还原反应 的化学方程式;可用盐酸代替H2SO4和H2O2的混合液,但缺点是。(4)写出“沉钴”过程中 发生反应的化学方程式。(5)充放电过程中,发生LiCoO2与Li1- xCoO2之间的转化,写出放电时电池反应方程式。(6)上述工艺中,“放电处理”有利于 锂在正极的回收,其原因是。在整个回收工艺中,可回收到的金属化合物有(填化学式) 。 【答案】(1)+3(2)2Al + 2OH- + 6H2O = 2Al(OH)- 4 + 3H2↑(3)2LiCoO2 + 3H2SO4 + H2O2 Li2SO4 + 2CoSO4 + O2↑+ 4H2O2H2O2 2H2O + O2↑ ;有氯气生成,污染较大。(4) CoSO4 + 2NH4HCO3 = CoCO3↓+ (NH4)2SO4 +CO2↑+ H2O(5) Li1-xCoO2 + LixC6 = LiCoO2 + 6C(6)Li+从负极中脱出,经由电解质向正极移动并进入正极材料中 Al(OH)3、CoCO3、Li2SO4【考点】离子方程式的书写、离子反应及其发生的条件、电解池的 离子运动、电解质化学式的书写 11.(2013全国高考)草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和 稀土生产。一种制备草酸(含2个结晶水)的工艺流程如下: 回答下列问题:(1)CO和NaOH在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程 式分别为、。(2)该制备工艺中有两次过滤操作,过滤操作①的滤液是,滤渣是;过滤操 作②的滤液是和,滤渣是。 (3)工艺过程中③和④的目的是。(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸 。该方案的缺点是产品不纯,其中含有的杂质主要是。(5)结晶水合草酸成品的纯度用高 锰酸钾法测定。称量草酸成品0.250g溶于水中,用0.0500 mol•L- 1的酸性KMnO4溶液滴定,至粉红色不消褪,消耗KMnO4溶液15.00mL,反应的离子方程式为; 列式计算该成品的纯度。 【答案】(1)CO + NaOH HCOONa 2HCOONa Na2C2O4 + H2↑(2)NaOH溶液 CaC2O4H2C2O4溶液 H2SO4溶液 CaSO4(3)分别循环利用氢氧化钠和硫酸(降低成本),减小污染。(4)Na2SO4(5)5C2O 2- 4 + 2MnO- 4 + 16H+ = 2Mn2+ + 8H2O + 10CO2↑ 【考点】离子反应及其发生的条件(产物判断)、离子方程式的书写 4.(2013全国II卷)能正确表示下列反应的离子方程式 A.浓盐酸与铁屑反应:2Fe + 6H+ = 2Fe3+ + 3H2↑ B.钠与CuSO4溶液反应:2Na + Cu2+ = Cu↓+ 2Na+ C.NaHCO3溶液与稀H2SO4反应:CO32-+ 2H+ = H2O + CO2↑ D.向FeCl3溶液中加入Mg(OH)2:3Mg(OH)2 + 2Fe3+ = 2Fe(OH)3 + 3Mg2+ 【答案】D 【考点】离子方程式的正误判断 10.(2013全国高考)二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。由合成气( 组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:甲醇合 成反应:(i)CO(g) + 2H2(g) = CH3OH(g) △H1 = -90.1kJ•mol- 1(ii)CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H2 = -49.0kJ•mol- 1水煤气变换反应:(iii)CO(g) + H2O(g) = CO2(g) + H2 (g) △H3 = - 41.1kJ•mol-1二甲醚合成反应:(iV)2 CH3OH(g) = CH3OCH3(g) + H2O(g) △H4 = -24.5kJ•mol- 1回答下列问题:(1)Al2O3是合成气直接制备二甲醚反应催化剂的主要成分之一。工业上 从铝土矿制备较高纯度Al2O3的主要工艺流程是(以化学方程式表示)。(2)分析二甲醚 合成反应(iV)对于CO转化率的影响。(3)由H2和CO直接制备二甲醚(另一产物为水蒸气 )的热化学方程式为。根据化学反应原理,分析增加压强对直接制备二甲醚反应的影响。 (4)有研究者在催化剂(含Cu—Zn—Al— O和Al2O3)、压强为5.0MPa的条件下,由H2和CO直接制备二甲醚,结果如下图所示。其中CO 转化率随温度升高而降低的原因是。 (5)二甲醚直接燃料电池具有启动快、效率高等优点,其能量密度等于甲醇直接燃料电池 (5.93kW•h•kg- 1)。若电解质为酸性,二甲醚直接燃料电池的负极反应为,一个二甲醚分子经过电化学氧 化,可以产生个电子的能量;该电池的理论输出电压为1.20V,能量密度E = (列式计算。能量密度=电池输出电能/燃料质量,1 kW•h = 3.6×106J)。 【答案】10.(1)Al2O3(铝土矿) + 2NaOH + 3H2O = 2NaAl(OH)4NaAl(OH)4 + CO2 = Al(OH)3↓ + NaHCO3,2Al(OH)3 Al2O3+ 3H2O(2)消耗甲醇,促进甲醇合成反应(i)平衡右移,CO转化率增大;生成的H2O,通过 水煤气变换反应(iii)消耗部分CO。(3)2CO(g) + 4H2(g) = CH3OCH3 + H2O(g) △H= -204.7kJ•mol- 1该反应分子数减少,压强升高使平衡右移,CO和H2转化率增大,CH3OCH3产率增加。压强升 高使CO和H2浓度增加,反应速率增大。(4)反应放热,温度升高,平衡左移。(5)CH3OC H3 + 3H2O = 2CO2 + 12H+ + 12e- 12 【分析】离子反应方程书写 12.(2013全国高考)硅是重要的半导体材料,构成了现代电子工业的基础。请回答下列 问题:(1)基态Si原子中,电子占据的最高能层符号为,该能层具有的原子轨道数为、电 子数为。(2)硅主要以硅酸盐、等化合物的形式存在于地壳中。(3)单质硅存在与金刚 石结构类似的晶体,其中原子与原子之间以相结合,其晶胞中共有8个原子,其中在面心位 置贡献个原子。(4)单质硅可通过甲硅烷(SiH4)分解反应来制备。工业上采用Mg2Si和N H4Cl在液氨介质中反应制得SiH4,该反应的化学方程式为。(5)碳和硅的有关化学键键能 如下所示,简要分析和解释下列有关事实: 化学键 C—C C—H C—O Si—Si Si—H Si—O 键能/(kJ•mol-1 356 413 336 226 318 452 ①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是。②SiH 4的稳定性小于CH4,更易生成氧化物,原因是。(6)在硅酸盐中,SiO44-四面体(如下图 (a))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(b )为一种无限长单链结构的多硅酸根,其中Si原子的杂化形式为,Si与O的原子数之比为, 化学式为。 【答案】12.(1)M 9 4(2)二氧化硅(3)共价键 3(4)Mg2Si + 4NH4Cl = SiH4 + 4NH3 + 2MgCl2(5)①C—C键和C— H键较强,所形成的烷烃稳定。而硅烷中Si—Si键和Si— H键的键能较低,易断裂,导致长链硅烷难以生成。②C—H键的键能大于C—O键,C— H键比C—O键稳定。而Si—H键的键能却远小于Si—O键,所以Si— H键不稳定而倾向于形成稳定性更强的Si—O键。(6)sp3 1∶3 [SiO3]2n- n(或SiO2- 3) 【分析】离子反应方程书写 2013全国新课标Ⅱ 9.(2013全国II卷)氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧 化锌(含有Fe(II)、Mn(II)、Ni(II)等杂质)的流程如下: 提示:在本实验条件下,Ni(II)不能被氧化;高锰酸钾的还原产物是MnO2。回答下列问题 :(1)反应②中除掉的杂质离子是,发生反应的离子方程式为;在加高锰酸钾溶液前,若 pH较低,对除杂的影响是。(2)反应③的反应类型为,过滤得到的滤渣中,除了过量的锌 外还有。(3)反应④形成的沉淀要用水洗,检查沉淀是否洗涤干净的方法是。(4)反应 ④中产物的成分可能是ZnCO3·xZn(OH)2。取干燥后的滤饼11.2g,锻烧后可得到产品8.1g ,则x等于。 【答案】(1)Fe2+和Mn2+ MnO4-+ 3Fe2+ + 7H2O = 3Fe(OH)3↓+ MnO2↓+ 5H+ 2 MnO4-+ 3Mn2+ + 2H2O = 5MnO2↓+ 4H+ 铁离子和锰离子不能生成沉淀,从而无法除去铁和锰杂质(2)置换反应 镍(3)取少量水洗夜于试管中,滴入1~2滴稀硝酸,再滴入硝酸钡溶液,若无白色沉淀生 成,则说明沉淀已经洗涤干净(4)1 【考点】离子反应及其发生的条件(除杂)、离子方程式的书写、离子反应及其发生的条 件(杂质离子的检验)11.(2013全国II卷)锌锰电池(俗称干电池)在生活中的用量很 大。两种锌锰电池的构造如图(a)所示。 回答下列问题:(1)普通锌锰电池放电时发生的主要反应为: Zn + 2NH4Cl + 2MnO2 = Zn(NH3)2Cl2 + 2MnOOH①该电池中,负极材料主要是,电解质的主要成分是,正极发生的主要反应是。② 与普通锌锰电池相比,碱性锌锰电池的优点及其理由是。(2)图(b)表示回收利用废旧 普通锌锰电池工艺(不考虑废旧电池中实际存在的少量其他金属)。 ①图(b)中产物的化学式分别为A,B。②操作a中得到熔块的主要成分是K2MnO4。操作b中 ,绿色的K2MnO4溶液反应生成紫色溶液和一种黑褐色固体,该反应的离子方程式为。③采 用惰性电极电解K2MnO4溶液也能得到化合物D,则阴极处得到的主要物质是 (填化学式)。 【答案】11.(1)①Zn NH4Cl MnO2+NH4++e-=2MnOOH+NH3②碱性电池不易发生电解质的泄漏,因为消耗的负极改装在电池 的内部;碱性电池使用寿命较长,因为金属材料在碱性电解质中比在酸性电解质中的稳定 性提高。(答对一条即可)(2)①ZnCl2 NH4Cl②2MnO42-+2CO2=2MnO4-+MnO2↓2CO32- ③H2【考点】离子方程式的书写 2014全国新课标Ⅰ 2.(2014全国高考I卷)化学与社会、生活密切相关。对下列现象或事实的解释正确的是 选项 现象或事实 解释 A 用热的烧碱溶液洗去油污 Na2CO3可直接和油污反应 B 漂白粉在空气中久置变质 漂白粉中的CaCl2 与空气中的CO2反应生成CaCO3 C 施肥时,草木灰(有效成分为K2 CO3)不能与NH4Cl混合使用 K2CO3与NH4Cl反应生成氨气会降低肥效 D FeCl3溶液可用于铜质印刷线路 板制作 FeCl3能从含有Cu2+的溶液中置换出铜 【答案】2.C 【考点】离子反应及其发生的条件 7.(2014全国高考I卷)利用右图所示装置进行下列实验,能得出相应实验结论的是 选项 ① ② ③ 实验结论 A 稀硫酸 Na2S AgNO3与AgCl的 浊液 Ksp(AgCl)>Ksp(Ag2S) B 浓硫酸 蔗糖 溴水 浓硫酸具有脱水性、氧化性 C 稀盐酸 Na2SO3 Ba(NO3)2溶液 SO2与可溶性钡盐均可以生成 白色沉淀 D 浓硝酸 Na2CO3 Na2SiO3溶液 酸性:硝酸>碳酸>硅酸 【答案】7.B 【考点】离子反应及其发生的条件(现象分析) 9.(2014全国高考I卷)次磷酸(H3PO2)是一种精细化工产品,具有较强还原性,回答下列 问题:(1)H3PO2是一元中强酸,写出其电离方程式:。(2)H3PO2及NaH2PO2)均可将溶液 中的银离子还原为银单质,从而可用于化学镀银。①(H3PO2)中,磷元素的化合价为。②利 用(H3PO2)进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4︰1,则氧化产物为: (填化学式)③NaH2PO2是正盐还是酸式盐?其溶液显性(填弱酸性、中性、或者弱碱性)(3 )(H3PO2)的工业制法是:将白磷(P4)与氢氧化钡溶液反应生成PH3气体和Ba(H2PO2),后者再 与硫酸反应,写出白磷与氢氧化钡溶液反应的化学方程式:。(4)(H3PO2)也可以通过电 解的方法制备。工作原理如图所示(阳膜和阴膜分别只允许阳离子、阴离子通过): ①写出阳极的电极反应式。②分析产品室可得到H3PO2的原因。③早期采用“三室电渗析法 ”制备H3PO2,将“四室电渗析法”中阳极室的稀硫酸用H3PO2稀溶液代替,并撤去阳极室与 产品室之间的阳膜,从而合并了阳极室与产品室,其缺点是杂质。该杂质产生的原因是: 。 【答案】9.(1)H3PO2 H++H2PO2-(2)①+1 ②H3PO4 ③正盐 弱碱性(3)2P4+3Ba(OH)2+6H2O=3Ba(H2PO2)2+3PH3↑(4)①2H2O-4e-=O2↑+4H+;② 阳极室的 穿过阳膜扩散至产品室,原料室的 穿过阴膜扩散至产品室、二者反应生成③PO43-;H3PO3或H2PO2被氧化【考点】电离方程式 的书写、氧化还原反应方程书写、离子反应方程书写 11.(2014全国高考I卷)磷矿石主要以磷酸钙〔Ca3(PO4)2·H2O〕和磷灰石〔Ca3(OH)(PO4) 3〕等形式存在。图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用 过量硫酸分解制备磷酸。图(b)是热法磷酸生产过各中由磷灰石制单质磷的流程。 部分物质的相关性质如下: 熔点/℃ 沸点/℃ 备注 白磷 44 280.5 PH3 -133.8 -87.8 难溶于水,具有还原性 SiF4 -90 -86 易水解 回答下列问题:(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的℅ 。(2)以磷灰石为原料,湿法磷酸过程中Ca 3F(PO4)3反应的化学方程式为: 。现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得85℅的商品磷酸吨。(3)如图 (b)所示,热法生产磷酸的第一步是将二氧化硅、过量焦炭与磷灰石混合,高温反应生成白 磷。炉渣的主要成分是:(填化学式)冷凝塔1的主要沉积物是:冷凝塔2的主要沉积物是: (4)尾气中主要含有,还含有少量PH3、H2S和HF等,将尾气先通入纯碱溶液,可除去再通 入次氯酸钠溶液,可除去(均填化学式)(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高 ,但优点是: 。 【答案】11.(1)69 (2)Ca 3F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑ 0.49(3)CaSiO3;液态白磷;固态白磷(4)SiF4、CO;SiF4、HF、H2S;PH3(5) 产品纯度高(浓度大) 【考点】离子反应方程的书写、离子反应及其发生的条件(除杂) 3.(2014全国新课标)下列反应中,反应后固体物质增重的是 A.氢气通过灼热的CuO粉末 B.二氧化碳通过Na2O2粉末 C.铝与Fe2O3发生铝热反应 D.将锌粒投入Cu(NO3)2溶液 【考点】离子反应及其发生条件(产物分析) 2014全国新课标Ⅱ 9.(2014全国新课标)铅及其化合物可用于蓄电池,耐酸设备及X射线防护材料等。回答 下列问题:(1)铅是碳的同族元素,比碳多4个电子层,铅在周期表的位置为周期,第族 :PbO2的酸性比CO2的酸性(填“强”或“弱”)。<(2)PbO2与浓盐酸共热生成黄绿色气 体,反应的化学方程式为。(3)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程 式为:PbO2也可以通过石墨为电极,Pb(NO3) 2和Cu(NO3) 2的混合溶液为电解液电解制取。阳极发生的电极反应式,阴极观察到的现象是:若电解液 中不加入Cu(NO3)2,阴极发生的电极反应式,这样做的主要缺点是。(4)PbO2在加热过程 发生分解的失重曲线如下图所示,已知失重曲线上的a点为样品失重4.0%( )的残留固体,若a点固体表示为PbO2或mPbO2•nPbO2,列式计算x值和m:n值。 【答案】9.(1)六 ⅣA 弱(2)PbO2+4HCl(浓)PbCl2+Cl2↑+2H2O(3)PbO+ClO-= PbO2+Cl- Pb2++2H2O - 2e- = PbO2↓+4H+石墨上包上铜镀层 Pb2++2e- =Pb↓ 不能有效利用Pb2+(4)x=2 - =1.4 = = 【考点】氧化还原反应方程书写、离子反应方程书写、离子方程式的书写 11.(2014全国新课标)将海水淡化和与浓海水资源化结合起来是综合利用海水的重要途 径之一。一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺提取其他产 品。回答下列问题:(1)下列改进和优化海水综合利用工艺的设想和做法可行的是(填序 号)。①用混凝法获取淡水 ②提高部分产品的质量③优化提取产品的品种 ④改进钾.溴.镁的提取工艺(2)采用“空气吹出法”从浓海水中吹出Br2,并用纯碱吸 收。碱吸收溴的主要反应是:Br2+Na2CO3+H2O NaBr+NaBrO3+6NaHCO3,吸收1mol Br2时转移的电子为mol。(3)海水提镁的一段工艺流程如下图: 浓海水的主要成分如下: 离子 Na+ Mg2+ Cl- SO42- 浓度/(g·L-1) 63.7 28.8 144.6 46.4 该工艺过程中,脱硫阶段主要反应的离子方程式为,产品2的化学式为,1L浓海水最多可得 到产品2的质量为g。(4)采用石墨阳极.不锈钢阴极电解熔融的氯化镁,发生反应的化学 方程式为;电解时,若有少量水存在会造成产品镁的消耗,写出有关反应的化学方程式。 【答案】11.(1)②③④(2) (3)Ca2++SO42-= CaSO4↓ Mg(OH)2 69.6 (4)MgCl2 Mg+Cl2↑ Mg+2H2O Mg(OH)2+H2↑ 【考点】离子方程式的书写、离子反应及其发生的条件(产物判断) 2015全国新课标Ⅰ 10.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是() 【答案】D 【考点】ABD选项:离子反应及其发生的条件(现象分析、产物判断) 27.硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和 Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的 工艺流程如图所示: 回答下列问题: (1)写出Mg2B2O5·H2O与硫酸反应的化学方程式_____________。为提高浸出 速率,除适当增加硫酸浓度浓度外,还可采取的措施有_________(写出两条) 。 (2)利用_______的磁性,可将其从“浸渣”中分离。“浸渣”中还剩余的物 质是______(化学式)。 (3)“净化除杂”需先加H2O2溶液,作用是_______。然后在调节溶液的pH约 为5,目的是_________。 (4)“粗硼酸”中的主要杂质是________(填名称)。 (5)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂 ,其电子式为_______。 (6)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制 备单质硼,用化学方程式表示制备过程___________。 【答案】⑴Mg2B2O5·H2O+2H2SO4 2MgSO4+2H3BO3;减小铁硼矿粉粒径、提高反应温度。⑵Fe3O4;SiO2和CaSO4;⑶将Fe2+氧化 为Fe3+;使Al3+与Fe3+形成氢氧化物而除去。⑷(七水)硫酸镁⑸ ⑹2H3BO3 B2O3+3HO B2O3+3Mg 3MgO+2B 36.[化学——选修2:化学与技术](15分) 氯化亚铜(CuCl)广泛应用于化工、印染、电镀等行业。CuCl难溶于醇和水,可溶于氯离子 浓度较大的体系,在潮湿空气中易水解氧化。以海绵铜(主要成分是Cu和少量CuO)为原料 ,采用硝酸铵氧化分解技术生产CuCl的工艺过程如下: 回答下列问题: (1)步骤①中得到的氧化产物是_________,溶解温度应控制在60— 70度,原因是__________。 (2)写出步骤③中主要反应的离子方程式___________。 (3)步骤⑤包括用pH=2的酸洗、水洗两步操作,酸洗采用的酸是_________(写名称)。 (4)上述工艺中,步骤⑥不能省略,理由是_____________. (5)步骤②、④、⑤、⑧都要进行固液分离。工业上常用的固液分离设备有__________( 填字母) A、分馏塔 B、离心机 C、反应釜 D、框式压滤机 (6)准确称取所制备的氯化亚铜阳平mg,将其置于若两的FeCl3溶液中,待样品完全溶解 后,加入适量稀硫酸,用amol/L的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液bmL,反应中Cr 2O72-被还原为Cr3+,样品中CuCl的质量分数为__________。 【答案】 (1)CuSO4或Cu2+ 温度低溶解速度慢、温度过高铵盐分解(2)2Cu2++SO32-+2Cl- +H2O=2CuCl↓+SO42- +2H+(3)硫酸(4)醇洗有利加快去除CuCl表面水分,防止其水解氧化(5)BD(6) 【考点】离子方程式的书写、离子反应及其发生的条件(除杂) 2015全国新课标Ⅱ 13.用右图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是 【答案】D 【考点】离子反应及其发生的条件(现象分析) 26.(14分)酸性锌锰干电池是一种一次电池,外壳为金属锌,中间是碳棒,其周围是有碳 粉,二氧化锰,氯化锌和氯化铵等组成的填充物,该电池在放电过程产生MnOOH,回 收处理该废电池可以得到多种化工原料,有关数据下图所示: 溶解度/(g/100g水) 温度/℃ 化合物 0 20 40 60 80 100 NH4Cl 29.3 37.2 45.8 55.3 65.6 77.3 ZnCl2 343 395 452 488 541 614 化合物 Zn(OH)2 Fe(OH)2 Fe(OH)3 Ksp近似值 10-17 10-17 10-39 回答下列问题: (1)该电池的正极反应式为,电池反应的离子方程式为: (2)维持电流强度为0.5A,电池工作五分钟,理论消耗Zng。(已经F=96500C/mol) (3)废电池糊状填充物加水处理后,过滤,滤液中主要有氯化锌和氯化铵,两者可以 选项 ①中物质 ②中物质 预测②中的现象 A. 稀盐酸 碳酸钠与氢氧化钠的混合溶液 立即产生气泡 B. 浓硝酸 用砂纸打磨过的铝条 产生红棕色气体 C. 氯化铝溶液 浓氢氧化钠溶液 产生大量白色沉淀 D. 草酸溶液 高锰酸钾酸性溶液 溶液逐渐褪色 通过 分离回收,滤渣的主要成分是二氧化锰、和,欲从中得到较纯的二氧化锰,最简 便的方法是,其原理是。 (4)用废电池的锌皮制作七水合硫酸锌,需去除少量杂质铁,其方法是:加入新硫酸 和双氧水,溶解,铁变为加碱调节PH为,铁刚好完全沉淀。继续加碱调节PH为 ,锌开始沉淀。若上述过程不加双氧水的后果是,原因是 。 【答案】 【考点】离子方程式的书写、离子反应及其发生的条件(除杂、产物判断) 28. (15 分)二氧化氯(ClO2,黄绿色易溶于水的气体)是高效、低毒的消毒剂,回答下列问題: (1 )工业上可用KC1O3与Na2SO3在H2SO4存在下制得ClO2,该反应氧化剂与还原剂物质的量之 比为• (2)实验室用NH4Cl、盐酸、NaClO2(亚氯酸钠)为原料,通过以下过程制备ClO2: ①电解时发生反应的化学方程式为. ②溶液X中大量存在的阴离子有• ③除去ClO2中的NH3可选用的试剂是(填标号), a.水b.碱石灰C.浓硫酸d.饱和食盐水 (3)用下图装置可以测定混合气中ClO2的含量: (6)在锥形瓶中加入足量的碘化钾,用50 mL水溶解后,再加入 3 mL稀硫酸: (7)在玻璃液封装置中加入水.使液面没过玻璃液封管的管口; (8)将一定量的混合气体通入锥形瓶中吸收; IV. 将玻璃液封装置中的水倒入锥形瓶中: V. 用0.1000 mol·L- 1硫代硫酸钠标准溶液滴定锥形瓶中的溶液(I2+2S2O32-2I-+S4O62- ),指示剂显示终点时共用去20.00 mL硫代硫酸钠溶液。在此过程中: ①锥形瓶内ClO2与碘化钾反应的离子方程式为• ②玻璃液封装置的作用是• ③V中加入的指示剂通常为__________,滴定至终点的现象是 ④测得混合气中ClO2的质量为g. (4)用ClO2处理过的饮用水会含有一定最的亚氯酸盐。若要除去超标的亚氯酸盐,下 列物庾最适宜的是(填标号)• a.明矾b.碘化钾c.盐酸d.硫酸亚铁 【答案】 【考点】离子反应及其发生的条件(除杂)、离子方程式的书写查看更多