- 2021-04-12 发布 |
- 37.5 KB |
- 8页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
河南省商丘市第一高级中学2018-2019学年高一第二学期期末考试化学试卷
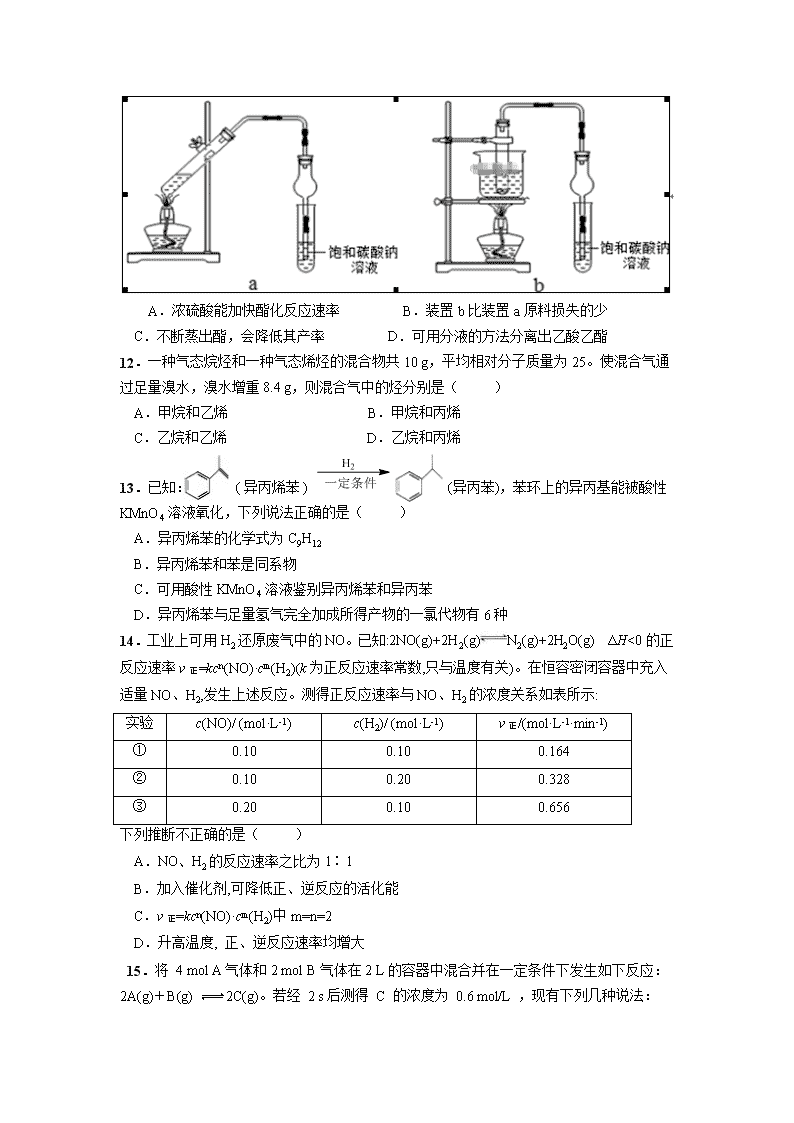
化学试卷 说明: 试卷满分100分,考试时间90分钟。答案请写到答题卷的相应位置。 可能用到的原子量:H-1 C-12 N-14 O-16 S-32 Cu-64 Br-80 第Ⅰ卷 选择题(共48分) 一、选择题:(每小题只有一个选项符合题意,共16小题,每小题3分) 1.下列表示反应中相关微粒的化学用语正确的是( ) A.中子数为18的氯原子: B.N2的结构式:N=N C.Na+的结构示意图: D.H2O的电子式: 2. NA表示阿伏加德罗常数的值,下列说法正确的是( ) A.常温下,在18 g 18O2中含有NA个氧原子 B.标准状况下,22.4 L二氯甲烷的分子数约为NA C.1 mol乙烷中含有C—H的键数为7×6.02×1023 D.1 mol —OH所含的电子数目为7 NA 3.下列变化中,属于物理变化的是( ) ①石油的分馏 ②煤的干馏 ③石油的裂化 ④铝热反应 ⑤由乙烯变为聚乙烯 ⑥氧气转变为臭氧 ⑦乙烯催熟果实 ⑧苯使溴水褪色 ⑨海水蒸馏法制取淡水 A.①②③④ B.①②⑤⑦ C.①②⑨ D.①⑧⑨ 4.在给定条件下,下列选项所示的物质间转化均能实现的是( ) A.Cl2(g)FeCl2(s) B.N2(g)NH3(g)Na2CO3(s) C.S(s)SO3(g)H2SO4(aq) D.MgCl2(aq)Mg(OH)2(s)MgO (s) 5.铟(49In)与铷(37Rb)同周期,下列说法不正确的是( ) A.In是第五周期第ⅢA族元素 B.11549In的中子数与电子数的差值为17 C.碱性:In(OH)3 > RbOH D.原子半径:In > Al 6.X、Y、Z均为短周期主族元素,它们原子的最外层电子数之和为10,X与Z同族,Y最外层电子数等于X次外层电子数,且Y原子半径大于Z。下列叙述正确的是( ) A.热稳定性:X的氢化物大于Z的氢化物 B.X与Z可形成离子化合物ZX C.熔点:X的氧化物比Y的氧化物高 D.Y的单质与Z的单质均能溶于浓硝酸 7.下列说法或表示方法中正确的是( ) A.等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量多 B.由C (金刚石)→C (石墨) △H = -1.9 kJ/mol 可知,金刚石比石墨稳定 C.稀溶液中:H+(aq)+ OH-(aq) = H2O(l) △H = -57.3 kJ/mol。若将含0.5 mol H2SO4的浓溶液与含l mol NaOH的溶液混合,放出的热量大于57.3 kJ D.在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式为:2H2(g) + O2(g) =2H2O(l) △H = +285.8 kJ/mol 8.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为: S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) △H= x kJ/mol 已知:①C(s)+O2(g)=CO2(g) △H= a kJ/mol ②K2S(s)=S(s)+2K(s) △H= b kJ/mol ③2K(s)+N2(g)+3O2(g)=2KNO3(s) △H= c kJ/mol 下列说法正确的是( ) A. x>0, a<0 B.b<0 ,c<0 C.x=3a-b-c D.1 mol 碳(s)在空气中不完全燃烧生成CO的焓变小于a kJ/mol 9.把镁条、铝条平行插入一定浓度的NaOH溶液中,用导线连接成原电池,此电池工作时,下列叙述中正确的是( ) A.原电池工作过程中溶液pH不变 B.Mg比Al活泼,Mg失去电子被氧化为Mg2+ C.负极反应式为Al-3e-+4OH-=AlO2-+2H2O D.Al是电池正极,开始工作时溶液中会立即有白色沉淀析出 10. 微生物燃料电池是指在微生物的作用下将化学能转化为电能的装置。某微生物燃料电池的工作原理如图所示,下列说法正确的是( ) A.电子从b流出,经外电路流向a B.若该电池电路中有0.4 mol电子发生转移,则有0.5 mol H+通过质子交换膜 C.如果将反应物直接燃烧,能量的利用率不会变化 D. HS-在硫氧化菌作用下转化为SO42- 的反应为:HS-+4H2O-8e-= SO42-+9H+ 11.乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计以下两套装置用乙醇、乙酸和浓硫酸分别制备乙酸乙酯(沸点77.2℃)。下列说法不正确的是( ) A.浓硫酸能加快酯化反应速率 B.装置b比装置a原料损失的少 C.不断蒸出酯,会降低其产率 D.可用分液的方法分离出乙酸乙酯 12.一种气态烷烃和一种气态烯烃的混合物共10 g,平均相对分子质量为25。使混合气通过足量溴水,溴水增重8.4 g,则混合气中的烃分别是( ) A.甲烷和乙烯 B.甲烷和丙烯 C.乙烷和乙烯 D.乙烷和丙烯 13.已知: ( 异丙烯苯 ) (异丙苯),苯环上的异丙基能被酸性KMnO4 溶液氧化,下列说法正确的是( ) A.异丙烯苯的化学式为C9H12 B.异丙烯苯和苯是同系物 C.可用酸性 KMnO4 溶液鉴别异丙烯苯和异丙苯 D.异丙烯苯与足量氢气完全加成所得产物的一氯代物有6种 14.工业上可用H2还原废气中的NO。已知:2NO(g)+2H2(g)N2(g)+2H2O(g) ΔH<0的正反应速率v正=kcn(NO)·cm(H2)(k为正反应速率常数,只与温度有关)。在恒容密闭容器中充入适量NO、H2,发生上述反应。测得正反应速率与NO、H2的浓度关系如表所示: 实验 c(NO)/ (mol·L-1) c(H2)/ (mol·L-1) v正/(mol·L-1·min-1) ① 0.10 0.10 0.164 ② 0.10 0.20 0.328 ③ 0.20 0.10 0.656 下列推断不正确的是( ) A.NO、H2的反应速率之比为1∶1 B.加入催化剂,可降低正、逆反应的活化能 C.v正=kcn(NO)·cm(H2)中m=n=2 D.升高温度, 正、逆反应速率均增大 15.将 4 mol A气体和2 mol B气体在2 L的容器中混合并在一定条件下发生如下反应: 2A(g)+B(g) 2C(g)。若经 2 s后测得 C 的浓度为 0.6 mol/L ,现有下列几种说法: ①用物质 A 表示的反应的平均速率为 0.3 mol/(L·s) ②用物质 B 表示的反应的平均速率为 0.6 mol/(L·s) ③2 s 时,物质 B 的浓度为 0.7 mol/L ④2 s 时,物质 A 的转化率为70% 其中正确的是( ) A.①③ B.①④ C.②③ D.③④ 16.对水样中溶质M的分解速率影响因素进行研究。在相同温度下,M的物质的量浓度(mol/L)随时间(min)变化的有关实验数据见下表。 时间 水样 0 5 10 15 20 25 I (pH=2) 0.40 0.28 0.19 0.13 0.10 0.09 II(pH=4) 0.40 0.31 0.24 0.20 0.18 0.16 Ⅲ(pH=4) 0.20 0.15 0.12 0.09 0.07 0.05 IV(pH=4,含 Cu2+) 0.20 0.09 0.05 0.03 0.01 0 下列说法不正确的是( ) A. 由于Cu2+存在,IV 中M的分解速率比I快 B. 其它条件相同时,水样pH越小,M的分解速率越快 C. 在0~25 min内,Ⅲ中M的分解百分率比II大 D. 在0~20 min内,I中M的平均分解速率为0.015 mol/(L·min) 第Ⅱ卷 非选择题(共52分) 二. 填空题:(每空2分) 17.右表为元素周期表的一部分。 (1)Z元素在周期表中的位置为________。 (2)表中元素原子半径最大的是(写元素符号)________。 (3)下列事实能说明Y元素的非金属性比S元素的非金属性强的是_______。 a.Y单质与H2S溶液反应,溶液变浑浊 b.在氧化还原反应中,1 mol Y单质比1 mol S得电子多 c.Y和S两元素的简单氢化物受热分解,前者的分解温度高 (4)X与Z两元素的单质反应生成1 mol X的最高价化合物,恢复至室温,放热687 kJ,已知该化合物的熔、沸点分别为-69℃和58 ℃,写出该反应的热化学方程式_______。 (5)铜与一定浓度的硝酸和硫酸的混合酸反应,生成的盐只有硫酸铜,同时生成的两种气体均由上表中两种元素组成,气体的相对分子质量都小于50。为防止污染,将产生的气体完全转化为最高价含氧酸盐,消耗1 L 2.2 mol/L 的NaOH溶液和1 mol O2,则两种气体的分子式及物质的量分别为_______。生成硫酸铜物质的量为_______。 18.在下列转化关系中,烃A为石油的裂解气里含量较高的气体(碳元素的质量分数为0.857)。B分子中含有三元环,分子式为C2H4O;1 mol D与足量Zn反应生成22.4L H2(标准状况);E为六元环化合物。请回答下列问题: (1)写出A 的结构简式_______。 (2)①的反应类型为_______。 (3)D物质中含氧原子团的名称为_______。 写出HOCH2CH2OH与金属钠反应的化学方程式_______。 (4)写出反应②的化学方程式_______。 19.I.(1)已知C(s)+O2(g)=CO2(g) △H= -393 kJ/mol 2CO(g)+O2(g)=2CO2(g) △H= -566 kJ/mol 2H2(g)+O2(g)=2H2O(g) △H= -484 kJ/mol 将水蒸气喷到灼热的炭上可实现炭的气化(制得CO、H2),写出该反应的热化学方程式_______。 (2)工业上利用CO和水蒸气在一定条件下发生反应制取氢气: CO(g)+ H2O(g)⇌ CO2(g)+ H2(g) △H= -41.0 kJ/mol 该反应过程中,反应物分子中化学键断裂时所吸收的总能量 (填“大于”、“小于”或“等于”)生成物分子中化学键形成时所释放的总能量。 II.教材中用酸性KMnO4溶液和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10 CO2↑+8H2O。某实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化): 序号 A溶液 B溶液 ① 20 mL 0.1 mol/L H2C2O4溶液 30 mL 0.01 mol/L KMnO4溶液 ② 20 mL 0.2 mol/L H2C2O4溶液 30 mL 0.01 mol/L KMnO4溶液 (3)该实验探究的是_______因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是①_______②(填“>”、“<”或“=”)。 (4)若实验①在2 min末收集了896 mL CO2(标准状况下),则用MnO4-表示该时间内的化学反应速率为v (MnO4-)=_______。 (5)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定_______来比较化学反应速率。 反应速率 时间 O t1 t2 图二 (6)该实验小组同学发现反应速率如图二所示,其中t1~t2时间内 速率变快的主要原因可能是:①该反应放热;②_______。 20.某化学小组同学为探究海水提溴原理,模拟空气吹出法设计了如下图所示的实验装置。(假设浓缩海水中的主要成分为 NaCl 和 NaBr,其他杂质不参与反应) (1)写出使用 KMnO4 和浓盐酸反应制备 Cl2 的离子方程式:_______,该反应中氧化剂和还原剂的物质的量之比为_______。 (2)从浓缩海水中提取溴的实验步骤如下: ①关闭活塞b 、d ,打开活塞 a 、c , 向 A 中缓慢通入 Cl2至反应结束; ②关闭活塞 a、 c,打开活塞b、 d , 向 A 中鼓入足量热空气; ③关闭b ,打开a ,再通过 A 向 B 中 通入足量的Cl2; ④取 B 中所得液体进行蒸馏,收集液溴。 请按正确的顺序填入步骤的序号:_______。 (3)判断以上步骤①中反应已经结束的实验现象:_______。 (4)试剂 X 最好选用_______(填字母,下同),尾气处理最好选用_______。 a、蒸馏水 b、饱和食盐水 c、氢氧化钠溶液 d、饱和 Na2SO3 溶液 (5)为从工业溴中提纯溴,他们查阅了有关资料,然后设计了如下的实验装置: 仪器 B 的名称是_______。欲要达到提纯溴的目的,操作的关键是检查实验装置的气密性,还有_______。 高一化学参考答案 一.选择题(每题3分,共48分) 题号 1 2 3 4 5 6 7 8 答案 D A D D C A C C 题号 9 10 11 12 13 14 15 16 答案 C D C A D C A A 二.填空题(共52分,每空2分) 17. (1)第三周期ⅦA族 (2)Si (3)ac (4)Si(s)+2Cl2(g)===SiCl4(l) ΔH=-687 kJ•mol-1 (5) NO:0.9 mol,NO2:1.3 mol 2 mol 18.(1)CH2=CH2; (2)氧化反应 (3)羧基; (4) 19. I. (1) C(s)+ H2O(g)= CO(g)+ H2(g) △H=+132 kJ/mol (2) 小于 II.(3)草酸浓度;<; (4)0.08mol/(L•min) (5)产生相同体积CO2所需要的时间(或KMnO4溶液完全褪色的时间); (6)产物Mn2+(或MnSO4)是反应的催化剂; 20. (1) 2MnO4-+10Cl-+16H+=2Mn2++5 Cl2↑+8H2O 1:5 (2) ①②③④ (3)当观察到 A 中液面上方出现黄绿色 (4) d c (5) 直形冷凝管 注意观察温度计 a,b 的读数,控制好热水浴的温度,及时收集 59.1℃的馏分查看更多