- 2021-05-25 发布 |
- 37.5 KB |
- 5页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020届一轮复习苏教版水溶液中的离子平衡的综合应用学案
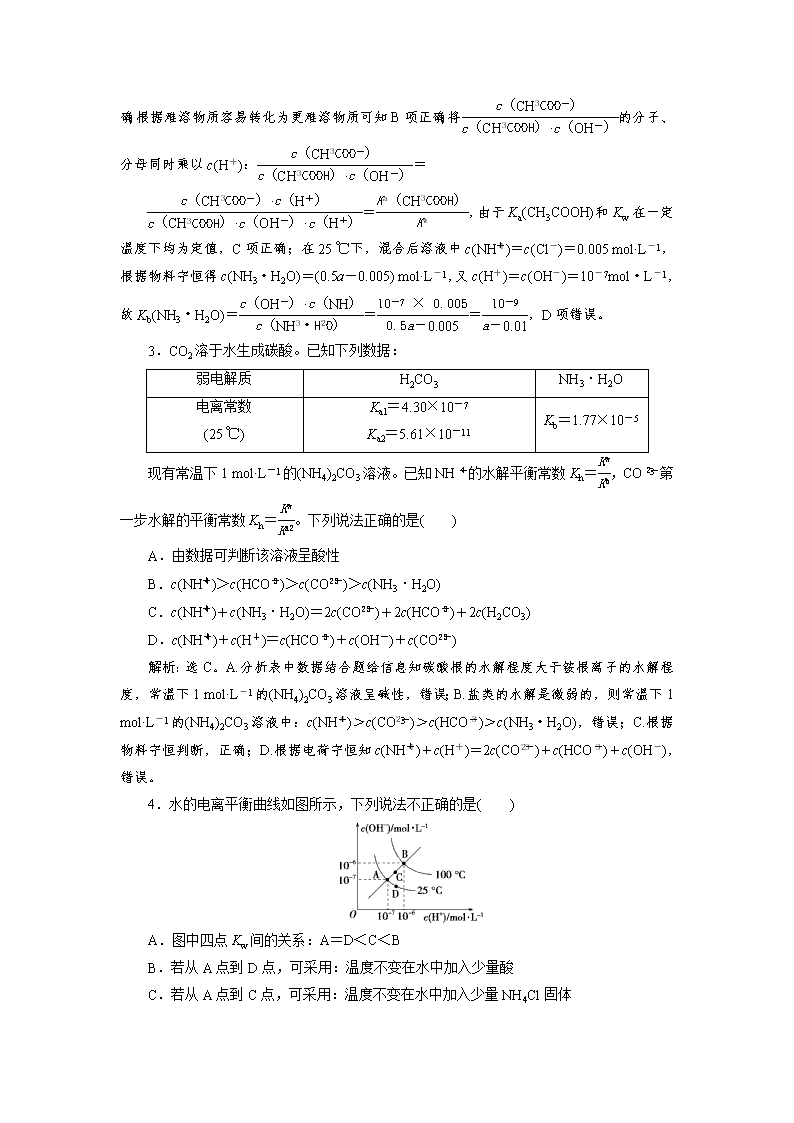
水溶液中的离子平衡的综合应用 [备考分析] 水溶液中的离子平衡包括弱电解质的电离平衡、盐类的水解平衡以及难溶电解质的溶解平衡三大部分内容,其中的概念、规律体系、中和滴定实验以及四大平衡常数非常重要,是高考重点设题的部分,这部分内容的考试热点有: (1)强、弱电解质的比较。(2)勒夏特列原理在“三大”平衡中的应用。(3)水的离子积常数、电离常数的应用与计算。(4)溶液酸碱性的判断。(5)pH的简单计算及应用(包括pH的变化规律、盐溶液pH的大小比较)。(6)微观粒子数的大小比较与计算(三大守恒的应用)。(7)溶度积常数的计算及应用(包括沉淀的生成、溶解及转化规律)。 水溶液中的离子平衡的考查题型既涉及选择题,又涉及非选择题;既有正误判断,也有大小比较、守恒关系、计算,还有图像分析、反应过程分析等等。 [命题解读] 该部分内容的知识网络可以用下图概括: 角度一 弱电解质的电离平衡 弱电解质的电离平衡是很重要的基本理论知识,通过此类试题可以体现命题者对基本概念和基本理论的重视。此类试题的综合性较强,主要考查影响电离平衡的因素(内因和外因)、电离平衡常数、电离度以及pH的相关计算、图像分析等。 角度二 水的电离和溶液的酸碱性 水的电离和溶液的酸碱性判断是高考常考的知识点。这类试题难度不大,主要考查溶液的酸碱性判断、Kw和pH的简单计算,其中Kw只与温度有关是计算和判断pH的关键。 角度三 盐类的水解及应用 盐类的水解是重要的基本理论知识,该类试题综合性较强,注意考查影响盐类水解的本质及规律、水解平衡常数和盐类水解的应用,其中盐类水解的本质及规律、水解平衡常数的巧妙运用尤为重要。 角度四 溶液中粒子浓度的关系 粒子浓度的关系是重要的基本理论知识,此类试题体现了命题者对基本理论知识的重视。该类试题综合性强,主要考查单一电解质溶液、混合时不发生反应的电解质溶液、混合时反应的电解质溶液中粒子浓度大小关系及等量关系,其中弱电解质的电离、盐类的水解、“三大守恒”关系往往可以帮助解决粒子浓度关系问题。 角度五 酸碱中和反应综合运用 酸碱中和反应是重要的基本理论知识,此类试题综合性较强,考查面较广,主要考查酸碱中和滴定、弱电解质的电离、盐类的水解、粒子浓度大小关系比较等基本理论知识,其中结合图像进行滴定终点的判断、综合分析和电离平衡常数的计算等是考查重点。 角度六 难溶电解质的沉淀溶解平衡 该类试题主要考查外界因素对沉淀溶解平衡的影响、沉淀转化、结合图像进行有关溶度积Ksp的计算,注意Ksp只与温度有关,完全沉淀一般隐含了离子浓度为1×10-5 mol/L。 [突破训练] 1.化学平衡常数(K)、弱酸的电离平衡常数(Ka)、难溶物的溶度积常数(Ksp)是判断物质性质或变化的重要的平衡常数。下列关于这些常数的说法中,正确的是( ) A.平衡常数的大小与温度、浓度、压强、催化剂等有关 B.当温度升高时,弱酸的电离平衡常数Ka变小 C.Ksp(AgCl)>Ksp(AgI),由此可以判断AgCl(s) + I-(aq)===AgI(s)+ Cl-(aq)能够发生 D.Ka(HCN)查看更多
相关文章
- 当前文档收益归属上传用户
- 下载本文档