- 2021-05-19 发布 |
- 37.5 KB |
- 5页

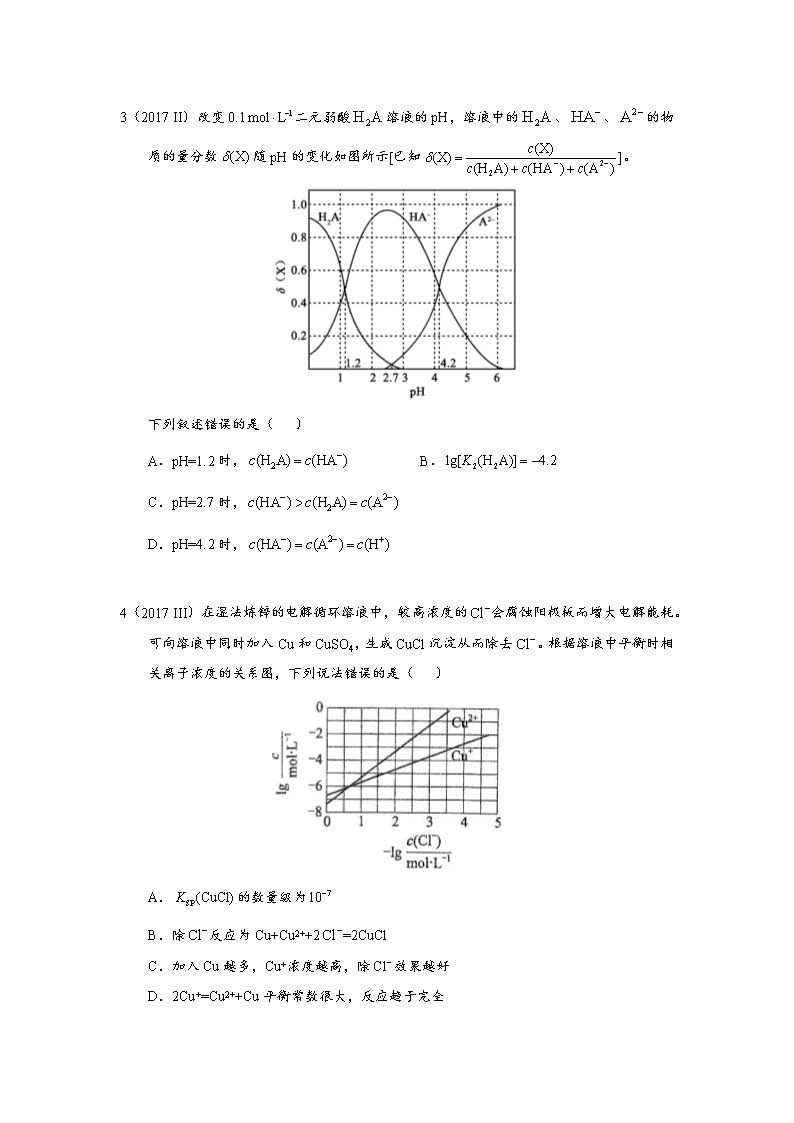
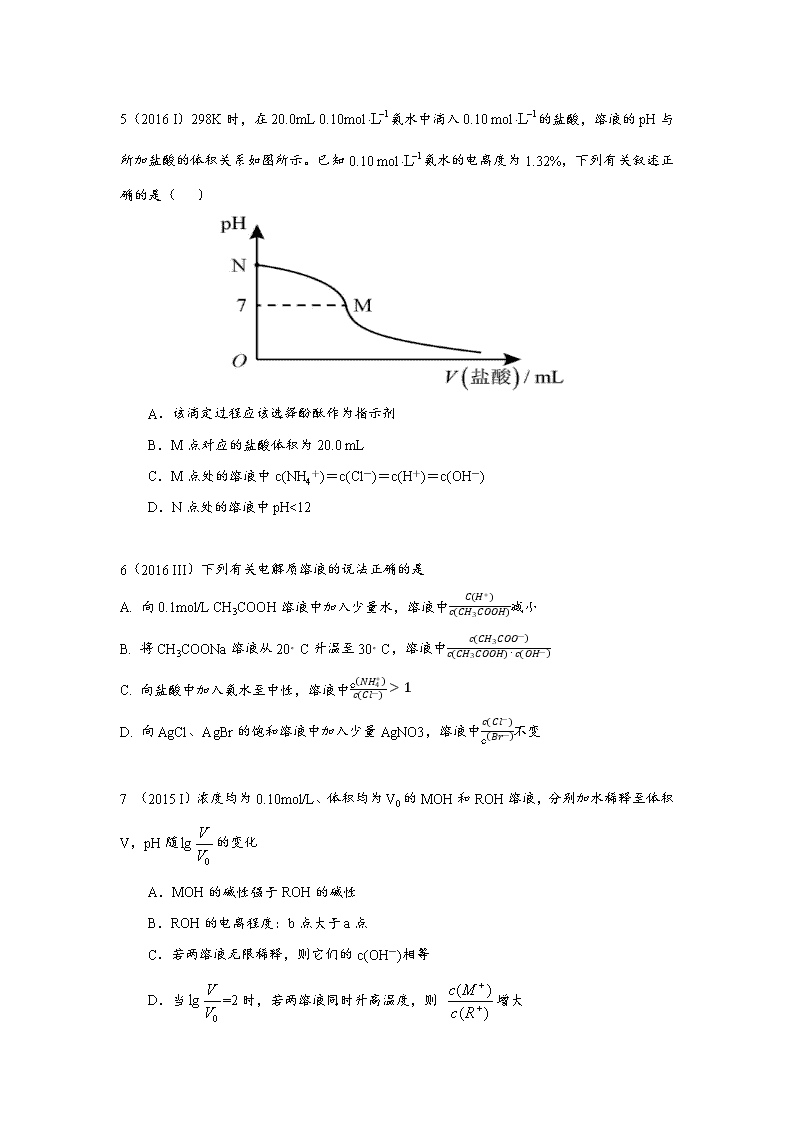
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
水溶液中的离子平衡高考题
水溶液中的离子平衡(全国卷) 1(2018 III)用0.100 mol·L-1 AgNO3滴定50.0 mL 0.0500 mol·L-1 Cl-溶液的滴定曲线如图所示。下列有关描述错误的是 A.根据曲线数据计算可知Ksp(AgCl)的数量级为10-10 B.曲线上各点的溶液满足关系式c(Ag+)·c(Cl-)=Ksp(AgCl) C.相同实验条件下,若改为0.0400 mol·L-1 Cl-,反应终点c移到a D.相同实验条件下,若改为0.0500 mol·L-1 Br-,反应终点c向b方向移动 2(2017 I)常温下将NaOH溶液滴加到己二酸(H2X)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是( ) A.Ka2(H2X)的数量级为10–6 B.曲线N表示pH与的变化关系 C.NaHX溶液中 D.当混合溶液呈中性时, 3(2017 II)改变0.1二元弱酸溶液的pH,溶液中的、、的物质的量分数随pH的变化如图所示[已知]。 下列叙述错误的是( ) A.pH=1.2时, B. C.pH=2.7时, D.pH=4.2时, 4(2017 III)在湿法炼锌的电解循环溶液中,较高浓度的会腐蚀阳极板而增大电解能耗。可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去。根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( ) A.的数量级为 B.除反应为Cu+Cu2++2=2CuCl C.加入Cu越多,Cu+浓度越高,除效果越好 D.2Cu+=Cu2++Cu平衡常数很大,反应趋于完全 5(2016 I)298K时,在20.0mL 0.10mol氨水中滴入0.10 mol的盐酸,溶液的pH与所加盐酸的体积关系如图所示。已知0.10 mol氨水的电离度为1.32%,下列有关叙述正确的是( ) A.该滴定过程应该选择酚酞作为指示剂 B.M点对应的盐酸体积为20.0 mL C.M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) D.N点处的溶液中pH<12 6(2016 III)下列有关电解质溶液的说法正确的是 A. 向0.1mol/L CH3COOH溶液中加入少量水,溶液中C(H+)c(CH3COOH)减小 B. 将CH3COONa溶液从20。C升温至30。C,溶液中c(CH3COO-)c(CH3COOH)∙c(OH-) C. 向盐酸中加入氨水至中性,溶液中c(NH4+)c(Cl-)>1 D. 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中c(Cl-)c(Br-)不变 7 (2015 I)浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随的变化 A.MOH的碱性强于ROH的碱性 B.ROH的电离程度:b点大于a点 C.若两溶液无限稀释,则它们的c(OH-)相等 D.当=2时,若两溶液同时升高温度,则 增大 8(2014 I)溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是( ) A. 溴酸银的溶解是放热过程 B.温度升高时溴酸银溶解速度加快 C.60℃时溴酸银的Ksp约等于6×10-4 D.若硝酸钾中含有少量溴酸银,可用重结晶方法提纯 9 (2014 I)下列有关仪器的使用方法或实验操作正确的是( ) A. 洗净的锥形瓶和容量瓶可以放进烘箱中烘干 B. 酸式滴定管装标准液前,必须先用该溶液润洗 C. 酸碱滴定实验中,用待滴定溶液润洗锥形瓶以减少实验误差 D. 用容量瓶配溶液时,若加水超过刻度线,立即用滴定管吸出多余液体。 10 (2014 II)一定温度下,下列溶液的离子浓度关系式正确的是 A. pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5mol·L-1 B. pH=a的氨水溶液,稀释10倍后,其pH=b,则a=b+1 C. pH=2的H2C2O4溶液与pH=12的NaOH溶液任意比例混合: cNa++cH+=cOH-+c(HC2O4-) D. pH相同的①CH3COONa ②NaHCO3 ③NaClO三种溶液的c(Na+):①>②>③ 11(2013 I)已知Ksp(AgCl)=1.56×10-10,Ksp(AgBr)=7.7×10-13,Ksp(Ag2CrO4)=9.0×10-12。某溶液中含有Cl-、Br-、CrO42-,浓度为0.010mol/L,向该溶液中滴加如0.010mol/L的AgNO3溶液时,三种阴离子产生沉淀的先后顺序为() A. Cl-、Br-、CrO42- B. CrO42-、Br-、Cl- C. Br-、Cl-、CrO42- D. Br-、CrO42-、Cl- 12(2013 II)室温时,MOH2s⇌M2+aq+2OH-aq Ksp=a0cM2+=b mol/L时,溶液的pH等于() A. 12lg(ba) B. 12lg(ab) C. 14 + 12lg(ab) D. 14 + 12lg(ba) 2012 2011 2009查看更多