- 2021-05-19 发布 |
- 37.5 KB |
- 25页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020届一轮复习人教版化学能与热能学案
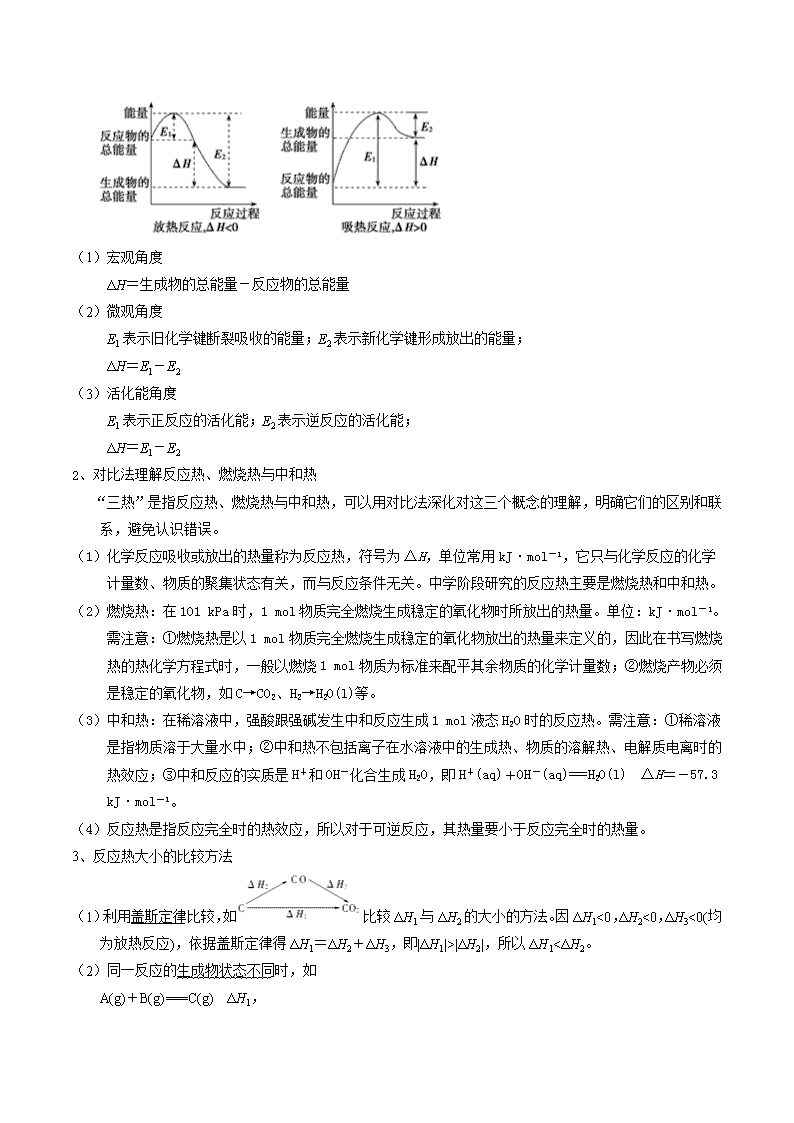
2020届一轮复习人教版 化学能与热能 学案 题型介绍: 该题型为高考中必考题型,通常以选择题或填空题的形式出现,考查反应热、燃烧热、中和热的概念,反应热的计算及盖斯定律的应用,热化学方程式的书写及判断,中和热的测定等。盖斯定律的应用和热化学方程式的书写为考查的重点,对于燃烧热和中和热的概念及计算仍将是高考考查的重点,常以具体的事实为背景进行设计题目,突出对概念的理解和应用,以图表为背景,考查化学反应中能量变化,以及涉及到盖斯定律或键能的简单计算逐渐成为高考出题新热点。 高考选题: 【2018新课标1卷】采用N2O5为硝化剂是一种新型的绿色硝化技术,在含能材料、医药等工业中得到广泛应用。回答下列问题 (2)已知:2N2O5(g)=2N2O4(g)+O2(g) ΔH1=−4.4 kJ·mol−1 2NO2(g)=N2O4(g) ΔH 2=−55.3 kJ·mol−1 则反应N2O5(g)=2NO2(g)+ O2(g)的ΔH=_______ kJ·mol−1。 【答案】 53.1 解题技巧: 1、从三个角度理解反应热 (1)宏观角度 ΔH=生成物的总能量-反应物的总能量 (2)微观角度 E1表示旧化学键断裂吸收的能量;E2表示新化学键形成放出的能量; ΔH=E1-E2 (3)活化能角度 E1表示正反应的活化能;E2表示逆反应的活化能; ΔH=E1-E2 2、对比法理解反应热、燃烧热与中和热 “三热”是指反应热、燃烧热与中和热,可以用对比法深化对这三个概念的理解,明确它们的区别和联系,避免认识错误。 (1)化学反应吸收或放出的热量称为反应热,符号为ΔH,单位常用kJ·mol-1,它只与化学反应的化学计量数、物质的聚集状态有关,而与反应条件无关。中学阶段研究的反应热主要是燃烧热和中和热。 (2)燃烧热:在101 kPa时,1 mol物质完全燃烧生成稳定的氧化物时所放出的热量。单位:kJ·mol-1。需注意:①燃烧热是以1 mol物质完全燃烧生成稳定的氧化物放出的热量来定义的,因此在书写燃烧热的热化学方程式时,一般以燃烧1 mol物质为标准来配平其余物质的化学计量数;②燃烧产物必须是稳定的氧化物,如C→CO2、H2→H2O(l)等。 (3)中和热:在稀溶液中,强酸跟强碱发生中和反应生成1 mol液态H2O时的反应热。需注意:①稀溶液是指物质溶于大量水中;②中和热不包括离子在水溶液中的生成热、物质的溶解热、电解质电离时的热效应;③中和反应的实质是H+和OH-化合生成H2O,即H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ·mol-1。 (4)反应热是指反应完全时的热效应,所以对于可逆反应,其热量要小于反应完全时的热量。 3、反应热大小的比较方法 (1)利用盖斯定律比较,如比较ΔH1与ΔH2的大小的方法。因ΔH1<0,ΔH2<0,ΔH3<0(均为放热反应),依据盖斯定律得ΔH1=ΔH2+ΔH3,即|ΔH1|>|ΔH2|,所以ΔH1<ΔH2。 (2)同一反应的生成物状态不同时,如 A(g)+B(g)===C(g) ΔH1, A(g)+B(g)===C(l) ΔH2, 则ΔH1>ΔH2。 (3)同一反应的反应物状态不同时,如 A(s)+B(g)===C(g) ΔH1, A(g)+B(g)===C(g) ΔH2, 则ΔH1>ΔH2。 (4)两个有联系的反应相比较时,如 C(s)+O2(g)===CO2(g) ΔH1①, C(s)+O2(g)===CO(g) ΔH2②。 比较方法:利用反应①(包括ΔH1)乘以某计量数减去反应②(包括ΔH2)乘以某计量数,即得出ΔH3=ΔH1×某计量数-ΔH2×某计量数,根据ΔH3大于0或小于0进行比较。 总之,比较反应热的大小时要注意: ①反应中各物质的聚集状态; ②ΔH有正负之分,比较时要连同“+”、“-”一起比较,类似数学中的正、负数大小的比较; ③若只比较放出或吸收热量的多少,则只比较数值的大小,不考虑正、负号。 4、反应热的有关计算 (1)根据热化学方程式计算:反应热与反应物的物质的量成正比。 (2)根据盖斯定律求算 应用盖斯定律进行简单计算时,关键在于设计反应过程,同时注意: ①参照新的热化学方程式(目标热化学方程式),结合原热化学方程式(一般2~3个)进行合理“变形”,如热化学方程式颠倒、乘除以某一个数,然后将它们相加、减,得到目标热化学方程式,求出目标热化学方程式的ΔH与原热化学方程式之间ΔH的换算关系。 ②当热化学方程式乘、除以某一个数时,ΔH也应相应地乘、除以某一个数;方程式进行加减运算时,ΔH也同样要进行加减运算,且要带“+”“-”符号,即把ΔH看作一个整体进行运算。 ③将一个热化学方程式颠倒书写时,ΔH的符号也随之改变,但数值不变。 ④在设计反应过程中,会遇到同一物质的三态(固、液、气)的相互转化,状态由固→液→气变化时,会吸热;反之会放热。 (3)根据物质燃烧放热的数值计算:Q(放)=n(可燃物)×|ΔH| (4)根据能量或键能计算 ΔH=生成物的总能量-反应物的总能量 ΔH=反应物的总键能之和-生成物的总键能之和 5、热化学方程式的书写 (1)注明反应条件:反应热与测定条件(温度、压强等)有关。绝大多数反应是在25 ℃、101 kPa下进行的,可不注明。 (2)注明物质状态:常用s、l、g、aq分别表示固体、液体、气体、溶液。 (3)注意符号单位:ΔH应包括“+”或“-”、数字和单位(kJ·mol-1)。 (4)注意守恒关系:①原子守恒和得失电子守恒;②能量守恒。(ΔH与化学计量数相对应) (5)区别于普通方程式:一般不注“↑”、“↓”以及“点燃”、“加热”等。 (6)注意热化学方程式的化学计量数 热化学方程式中各物质化学式前面的化学计量数仅表示该物质的物质的量,可以是整数,也可以是分数。且化学计量数必须与ΔH相对应,如果化学计量数加倍,则ΔH也要加倍。 高频考点一:热化学方程式的书写及正误判断 【典例】【江西铅山县一中2019届上学期期中】下列热化学方程式书写正确的是(ΔH的绝对值均正确)( ) A.C2H5OH(l)+3O2(g)2CO2(g)+3H2O(g) ΔH=−1 367.0 kJ/mol(燃烧热) B.NaOH(aq)+HCl(aq)NaCl(aq)+H2O(l) ΔH=+57.3 kJ/mol(中和热) C.S(s)+O2(g)SO2(g) ΔH=−296.8 kJ/mol(反应热) D.2NO2O2+2NO ΔH=+116.2 kJ/mol(反应热) 【答案】C 【 考点揭秘】盖斯定律在应用的过程中一定要注意思维模型,切勿毫无目的的将方程式乱加乱减,最终得不到结果。一般的思维模型是: 先确定待求的化学反应方程式 找出待求方程式中各物质在已知方程式中的位置 根据待求方程式中各物质的计量数和位置对已知方程式进行处理,得到变形后的新方程式 将新得到的方程式进行加减(反应热也需要相应的加减) 写出待求的热化学方程式 1.【2018北京卷】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。 下列说法不正确的是 ( ) A.生成CH3COOH总反应的原子利用率为100% B.CH4→CH3COOH过程中,有C―H键发生断裂 C.①→②放出能量并形成了C―C键 D.该催化剂可有效提高反应物的平衡转化率 【答案】D 【解析】分析:A项,生成CH3COOH的总反应为CH4+CO2CH3COOH,原子利用率为100%;B项,CH4选择性活化变为①过程中,有1个C-H键发生断裂;C项,根据图示,①的总能量高于②的总能量,①→②放出能量并形成C-C键;D项,催化剂只影响化学反应速率,不影响化学平衡,不能提高平衡转化率。 点睛:本题考查原子利用率、化学反应的实质、化学反应中的能量变化、催化剂对化学反应的影响,解题的关键是准确分析示意图中的信息。注意催化剂能降低反应的活化能,加快反应速率,催化剂不能改变ΔH、不能使化学平衡发生移动。 2.【2016年高考海南卷】油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应: C57H104O6(s)+80O2(g)=57CO2(g)+52H2O(l)已知燃烧1kg该化合物释放出热量3.8×104kJ。油酸甘油酯的燃烧热△H为 ( ) A.3.8×104kJ·mol-1 B.-3.8×104kJ·mol-1 C.3.4×104kJ·mol-1 D.-3.4×104kJ·mol-1 【答案】D 【解析】 试题分析:燃烧热指的是燃烧1mol可燃物生成稳定的氧化物所放出的热量。燃烧1kg油酸甘油酯释放出热量3.8×104kJ,则燃烧1mol油酸甘油酯释放出热量为3.4×104kJ,则得油酸甘油酯的燃烧热△H=-3.4×104kJ·mol-1 考点:考查燃烧热及化学反应中的能量 【名师点睛】考纲明确要求:了解化学能与热能的相互转化。了解吸热反应、放热反应、反应热等概念。根据考纲的这一要求将化学反应中的物质变化和能量变化综合起来考查将成为一种热门的题型,同时注意到由于能源日益匮乏,因此有关燃烧热、中和热、盖斯定律等问题必将成为今后命题的重点。新课程背景下的高考热化学方程式试题大多是一些思路型题型,题目变化较多,但思路变化却较少,主干知识依然是重点考查的内容。此类试题比较贴近当前的教学实际,虽然形式上有各种各样的变化,但只要学会了基础题型的解题思路和应对策略,缜密分析、逐层递解,再经过一些变化演绎,就可以准确解答相关题型。此外,通过此类题型的解题策略探究还有利于培养 3.【2016年高考海南卷】由反应物X转化为Y和Z的能量变化如图所示。下列说法正确的是 ( ) A.由反应的ΔH=E5−E2 B.由反应的ΔH<0 C.降低压强有利于提高Y的产率 D.升高温度有利于提高Z的产率 【答案】BC 考点:考查化学反应中的能量变化,化学图象的分析与判断 【名师点睛】对于化学图像问题,可按以下的方法进行分析: ①认清坐标系,搞清纵、横坐标所代表的意义,并与化学反应原理挂钩。②紧扣反应特征,搞清反应方向是吸热还是放热,体积增大还是减小,有无固体、纯液体物质参加反应。③看清起点、拐点、终点,看清曲线的变化趋势等等。本题考查化学反应与能量变化,主要结合物质反应与能量变化图,考查学生对化学反应热的理解。对于AB两项判断反应是放热反应还是吸热反应,可以从三个角度判断:一是比较反应物和生成物的总能量相对大小,生成物总能量比反应物总能量高的反应是吸热反应;二是比较反应物和生成物的总键能;三是从常见的分类去判断。 4.【2016年高考江苏卷】通过以下反应均可获取H2。下列有关说法正确的是 ( ) ①太阳光催化分解水制氢:2H2O(l)=2H2(g)+ O2(g) ΔH1=571.6kJ·mol–1 ②焦炭与水反应制氢:C(s)+ H2O(g) =CO(g)+ H2(g)ΔH2=131.3kJ·mol–1 ③甲烷与水反应制氢:CH4(g)+ H2O(g)=CO(g)+3H2(g)ΔH3=206.1kJ·mol–1 A.反应①中电能转化为化学能 B.反应②为放热反应 C.反应③使用催化剂,ΔH3减小 D.反应CH4(g)=C(s)+2H2(g)的ΔH=74.8kJ·mol–1 【答案】D 【考点定位】本题主要是考查化学反应与能量转化的有关判断以及反应热计算等 【名师点晴】应用盖斯定律进行反应热的简单计算的关键在于设计反应过程,同时还需要注意:①参照新的热化学方程式(目标热化学方程式),结合原热化学方程式(一般2~3个)进行合理“变形”,如热化学方程式颠倒、乘除以某一个数,然后将它们相加、减,得到目标热化学方程式,求出目标热化学方程式的ΔH与原热化学方程式之间ΔH的换算关系。②当热化学方程式乘、除以某一个数时,ΔH也应相应地乘、除以某一个数;方程式进行加减运算时,ΔH也同样要进行加减运算,且要带“+”“-”符号,即把ΔH看作一个整体进行运算。③将一个热化学方程式颠倒书写时,ΔH的符号也随之改变,但数值不变。④在设计反应过程中,会遇到同一物质的三态(固、液、气)的相互转化,状态由固→液→气变化时,会吸热;反之会放热。答题时注意灵活应用。 5.【2016年高考天津卷】氢能是发展中的新能源,它的利用包括氢的制备、储存和应用三个环节。回答下列问题: (2)氢气可用于制备H2O2。已知: H2(g)+A(l)=B(l) ΔH1 O2(g)+B(l)=A(l)+H2O2(l) ΔH2 其中A、B为有机物,两反应均为自发反应,则H2(g)+ O2(g)= H2O2(l)的ΔH____0(填“>”、“<”或“=”)。 【答案】(2)< 【解析】 试题分析: (2)①H2(g)+A(l)=B(l) ΔH1,②O2(g)+B(l)=A(l)+H2O2(l) ΔH2,两反应的ΔS<0,根据ΔG=ΔH-TΔS,因为均为两反应自发反应,因此ΔH均小于0,将①+②得:H2(g)+ O2(g)= H2O2(l)的ΔH=ΔH1+ΔH1<0,故答案为:<; 【考点定位】考查化学反应中的能量变化、电解原理及其应用 【名师点晴】本题考查的知识点较多,以氢气利用为线索考查了化学反应中的能量变化、电解原理及其应用、化学平衡的移动及其影响因素等相关知识。在书写燃料电池电极反应时,要注意掌握一般的书写方法:①电极反应是一种离子反应,遵循书写离子反应的所有规则;②将两极反应的电子得失数配平后,相加得到总反应,总反应减去一极反应即得到另一极反应;③负极失电子所得氧化产物和正极得电子所得还原产物,与溶液的酸碱性有关(如+4价的C在酸性溶液中以CO2形式存在,在碱性溶液中以CO32-形式存在);④溶液中不存在O2-:在酸性溶液中它与H+结合成H2O、在碱性或中性溶液中它与水结合成OH-。本题的易错点和难点是c(Na2FeO4)低于最高值的原因分析。分析时,要注意从题目中寻找线索并结合反应的特征分析。 6.【2016年高考新课标Ⅱ卷】联氨(又称联肼,N2H4,无色液体)是一种应用广泛的化工原料,可用作火箭燃料,回答下列问题: (1)联氨分子的电子式为_________,其中氮的化合价为______。 (2)实验室可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为_____ ______。 (3)①2O2(g)+N2(g)=N2O4(l) △H1 ②N2(g)+2H2(g)=N2H4(l) △H2 ③O2(g)+2H2(g)=2H2O(g) △H3 ④2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) △H4=-1048.9kJ/mol 上述反应热效应之间的关系式为△H4=________________,联氨和N2O4可作为火箭推进剂的主要原因为_________________________________________________。 【答案】26、(1) ;-2 (2)NaClO+2NH3=N2H4+NaCl+H2O (3)△H4=2△H3-2△H2-△H1 ;反应放热量大、产生大量气体 (2)次氯酸钠溶液与氨反应制备联氨,Cl元素的化合价由+1价降低到-1价,N元素的化合价由-3价升高到-2价,根据得失电子守恒和原子守恒配平,反应的化学方程式为NaClO+2NH3=N2H4+NaCl+H2O。 (3)根据盖斯定律,2×③-2×②-①即得2 N2H4(l) + N2O4(l)= 3N2(g)+ 4H2O(g) 的△H4,所以反应热效应之间的关系式为△H4=2△H3-2△H2-△H1。联胺有强还原性,N2O4有强氧化性,两者在一起易发生氧化还原反应,反应放热量大、产生大量气体,所以联氨和N2O4可作为火箭推进剂。 【考点定位】考查电子式,化合价,盖斯定律的应用,弱电解质的电离,化学计算等知识。 【名师点睛】本题以多知识点综合题的形式考查化学基本用语,涉及电子式和化合价,盖斯定律的应用,弱电解质的电离平衡,简单化学计算等知识。对于弱电解质电离平衡常数的计算要注意几点:①准确书写电离平衡常数的表达式;②若没有直接的数据代入,要根据题意做一些变形,得到平衡常数之间的关系式也可解答。 7.【2017新课标3卷】(3)已知:As(s)+H2(g)+2O2(g)=H3AsO4(s) ΔH1 H2(g)+O2(g)=H2O(l) ΔH2 2As(s)+O2(g) =As2O5(s) ΔH3 则反应As2O5(s) +3H2O(l)= 2H3AsO4(s)的ΔH =_________。 【答案】(3)2△H1-3△H2-△H3 8.【2016年高考新课标Ⅲ卷】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题: (4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。 ①从化学平衡原理分析,Ca(ClO)2相比NaClO具有的有点是_______。 ②已知下列反应: SO2(g)+2OH− (aq) ===SO32− (aq)+H2O(l) ΔH1 ClO− (aq)+SO32− (aq) ===SO42− (aq)+Cl− (aq) ΔH2 CaSO4(s) ===Ca2+(aq)+SO42−(aq) ΔH3 则反应SO2(g)+ Ca2+(aq)+ ClO− (aq) +2OH− (aq) === CaSO4(s) +H2O(l) +Cl− (aq)的ΔH=______。 【答案】 (4)①生成的硫酸钙微溶,降低硫酸根离子浓度,促使平衡向正反应方向进行②△H1+△H2-△H3 【解析】 试题分析:(4)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。 ①由于生成的硫酸钙微溶,降低硫酸根离子浓度,促使平衡向正反应方向进行,所以Ca(ClO)2效果好。 ②已知:①SO2(g)+2OH− (aq) ===SO32− (aq)+H2O(l) ΔH1 ②ClO− (aq)+SO32− (aq) ===SO42− (aq)+Cl− (aq) ΔH2 ③CaSO4(s) ===Ca2+(aq)+SO42−(aq) ΔH3 则根据盖斯定律可知①+②-③即得到反应SO2(g)+ Ca2+(aq)+ ClO− (aq) +2OH− (aq) === CaSO4(s) +H2O(l) +Cl− (aq)的ΔH=△H1+△H2-△H3。 考点:考查盖斯定律 9.【2017新课标2卷】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。回答下列问题: (1)正丁烷(C4H10)脱氢制1-丁烯(C4H8)的热化学方程式如下: ①C4H10(g)= C4H8(g)+H2(g) ΔH1 已知:②C4H10(g)+O2(g)= C4H8(g)+H2O(g) ΔH2=−119 kJ·mol−1 ③H2(g)+ O2(g)= H2O(g) ΔH3=−242 kJ·mol−1 反应①的ΔH1为________kJ·mol−1。 【答案】(1)+123 10.【2017江苏卷】通过以下反应可获得新型能源二甲醚(CH3OCH3 )。下列说法不正确的是 ( ) ① C(s) + H2O(g)CO(g) + H2 (g) ΔH1 = a kJ·mol−1 ②CO(g) + H2O(g)CO2 (g) + H2 (g) ΔH 2 = b kJ·mol−1 ③CO2 (g) + 3H2 (g)CH3OH(g) + H2O(g) ΔH 3 = c kJ·mol−1 ④2CH3OH(g)CH3OCH3 (g) + H2O(g) ΔH 4 = d kJ·mol−1 A.反应①、②为反应③提供原料气 B.反应③也是CO2资源化利用的方法之一 C.反应CH3OH(g)CH3OCH3 (g) +H2O(l)的ΔH =kJ·mol−1 D.反应 2CO(g) + 4H2 (g) CH3OCH3 (g) + H2O(g)的ΔH = ( 2b + 2c + d ) kJ·mol−1 【答案】C 【解析】A.反应①、②的生成物CO2和H2是反应③的反应物,A正确;B.反应③可将二氧化碳转化为甲醇,变废为宝,B正确;C.4个反应中,水全是气态,没有给出水由气态变为液态的焓变,所以C错误;D.把反应②③④三个反应按(②+③)2+④可得该反应及对应的焓变,D正确。 【名师点睛】本题以合成新能源二甲醚为背景,考查学生对简单化工流程的反应原理、能量的转化关系、化学反应焓变的概念、盖斯定律的运用等知识的掌握和理解程度,同时关注了节能减排、工业三废资源化处理、开发利用新能源等社会热点问题。 11.【2018新课标2卷】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题: (1)CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g)。 已知:C(s)+2H2(g)=CH4(g) ΔH=-75 kJ·mol−1 C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol−1 C(s)+1/2O2(g)=CO(g) ΔH=-111 kJ·mol−1 该催化重整反应的ΔH==______ kJ·mol−1。 【答案】 247 12.【2018北京卷】近年来,研究人员提出利用含硫物质热化学循环实现太阳能的转化与存储。过程如下: (1)反应Ⅰ:2H2SO4(l)2SO2(g)+2H2O(g)+O2(g) ΔH1=+551 kJ·mol-1 反应Ⅲ:S(s)+O2(g)SO2(g) ΔH3=-297 kJ·mol-1 反应Ⅱ的热化学方程式:________________。 【答案】(2)H2O(l)=H2(g)+O2(g) ΔH=+286 kJ/mol H2S(g)=H2(g)+S(s) ΔH=+20 kJ/mol 系统(II) 13.【2018天津卷】CO2是一种廉价的碳资源,其综合利用具有重要意义。回答下列问题: (2)CO2与CH4经催化重整,制得合成气: CH4(g)+ CO2(g) 2CO (g)+ 2H2(g) ①已知上述反应中相关的化学键键能数据如下: 化学键 C—H C=O H—H CO(CO) 键能/kJ·mol−1 413 745 436 1075 则该反应的ΔH=_________。 【答案】 +120 kJ·mol-1 【解析】(2)①化学反应的焓变应该等于反应物键能减去生成物的键能,所以焓变为(4×413+2×745)-(2×1075+2×436)= +120 kJ·mol-1。 14.【2018江苏卷】NOx(主要指NO和NO2)是大气主要污染物之一。有效去除大气中的NOx是环境保护的重要课题。 (1)用水吸收NOx的相关热化学方程式如下: 2NO2(g)+H2O(l)HNO3(aq)+HNO2(aq) ΔH=−116.1 kJ·mol−1 3HNO2(aq)HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol−1 反应3NO2(g)+H2O(l)2HNO3(aq)+NO(g)的ΔH=___________kJ·mol−1。 【答案】(1)−136.2 【解析】1)将两个热化学方程式编号, 2NO2(g)+H2O(l)=HNO3(aq)+HNO2(aq) ΔH=−116.1 kJ·mol−1(①式) 3HNO2(aq)=HNO3(aq)+2NO(g)+H2O(l) ΔH=75.9 kJ·mol−1(②式) 应用盖斯定律,将(①式3+②式)2得,反应3NO2(g)+H2O(l)=2HNO3(aq)+NO(g)ΔH=[(−116.1 kJ·mol−1)3+75.9 kJ·mol−1]2=-136.2kJ·mol−1。 夯实基础: 1.【哈尔滨呼兰区一中2019届高三12月月考】下列说法正确的是 ( ) A.1 mol强酸和1 mol强碱完全反应所放出的热量称为中和热 B.热化学方程式中表明的热量是指每摩尔反应物反应时吸收或放出的热量 C.热化学方程式中的化学计量数表示物质的量,因此可用分数表示 D.1 mol碳燃烧所放出的热量为燃烧热 【答案】C 2.【湖南衡阳市八中2019届高三第四次月考】有关热化学方程式书写与对应表述均正确的是 ( ) A.稀硫酸与 0.1 mol/L NaOH 溶液反应:H+(aq)+OH-(aq)= H2O(l) △H = +57.3 kJ·mol-1 B.已知 2C(s)+O2(g)=2CO(g) △H= -221 kJ·mol-1, 则可知 C 的燃烧热为 110.5 kJ·mol-1 C.0℃、30MPa 下,将 0.5mol N2 和 1.5molH2 置于密闭的容器中充分反应生成 NH3(g),放热 19.3kJ, 其热化学方程式为:N2(g) + 3H2(g) 2NH3(g) △H= -38.6kJ·mol-1 D.密闭容器中,0. 3mol 硫粉与 0.2mol 铁粉混合加热生成硫化亚铁 0.2mol 时,放出 19.12 kJ 热量, 则 Fe(s)+S(s)=FeS(s)△H= - 95.6 kJ·mol-1 【答案】D 3.【山东恒台一中2019届高三上学期诊断】CH4-CO2催化重整不仅可以得到合成气CO和H2,还对温室气体的减排具有重要意义。 已知:C(s)+2H2(g)=CH4(g) △H1 K1 C(s)+O2(g) =CO2(g) △H2 K2 ;C(s)+O2(g) =CO(g) △H3 K3;CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H K(其中△H为焓变,K为平衡常数)下列说法正确的是 ( ) A.△H=2△H3-2△H2-△H1 B.K=2K3-K2-K1 C.若平衡时c(CH4):c(CO2):c(CO):c(H2)=1:1:1:1,则K一定等于1(mol/L)2 D.减小压强可增大CH4(g)和CO2(g)的平衡转化率 【答案】D 【解析】A.①C(s)+2H2(g)=CH4(g) △H1 ②C(s)+O2(g) =CO2(g) △H2 ③C(s)+O2(g) =CO(g) △H3 将方程式2×③-①-②可得CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=2△H3-△H1-△H2,A错误;B.根据化学平衡常数的含义可得K1=;K2=;K3=;K=,B错误;C.若平衡时c(CH4):c(CO2):c(CO):c(H2)=1:1:1:1,假设每种物质的浓度都是x,则K==,若x=1,则K=1,若x=2,则K=4,所以K不一定为1(mol/L)2,C错误;D.由于反应CH4(g)+CO2(g)=2CO(g)+2H2(g)的正反应为气体体积增大的反应,所以根据平衡移动原理,减小压强,化学平衡正向移动,从而可增大CH4(g)和CO2(g)的平衡转化率,D正确;故合理选项是D。 4.【北京海淀区2019届高三上学期期末】以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下: 相关反应的热化学方程式为: 反应I:SO2(g) + I2(g) + 2H2O(l) === 2HI(aq) + H2SO4(aq) ΔH1 =﹣213 kJ·mol-1 反应II:H2SO4(aq) === SO2(g) + H2O(l) + O2(g) ΔH2 = +327 kJ·mol-1 反应III:2HI(aq) === H2(g) + I2(g) ΔH3 = +172 kJ·mol-1 下列说法不正确的是: ( ) A.该过程实现了太阳能到化学能的转化 B.SO2和I2对总反应起到了催化剂的作用 C.总反应的热化学方程式为:2H2O(l) === 2H2 (g)+O2(g) ΔH = +286 kJ·mol-1 D.该过程降低了水分解制氢反应的活化能,但总反应的ΔH不变 【答案】C 5.【福建永安市三中2018届高三9月月考】由化学能产生的能量是目前人类使用的主要能源。请回答下列问题: (1)N2和O2在一定条件下反应生成NO2的热化学方程式为: 1/2N2(g)+O2(g)====NO2(g) ΔH=+34 kJ·mol-1。该反应为________(“放热”“吸热”)反应。 (2)化学反应中的能量变化源自于化学反应中化学键变化时产生的能量变化。下表为一些化学键的键能: 化学键 键能( kJ·mol-1) 化学键 键能( kJ·mol-1) N≡N 942 H—O 460 N—H 391 O==O 499 H—H 437 ①写出N2和H2反应合成氨的热化学方程式________________________。 ② 已知:1 mol H2O(g)转化为1 mol H2O(l)时放出44.0 kJ的热量。计算1 g H2完全燃烧时放出的热量______________。H2O(g)的稳定性___________(“大于”“小于”)H2O(l)。 (3)写出NH3(g)在O2(g)中完全燃烧生成NO2(g)和H2O(g)的热化学方程式________________。 【答案】吸热 N2(g)+3H2(g)⇌2NH3(g) △H=-93kJ•mol-1 138.75 kJ 小于4NH3(g)+7O2(g)==4NO2(g)+6H2O(g) ΔH=-1 079 kJ·mol-1 (3)根据①1/2N2(g)+O2(g)====NO2(g) ΔH=+34 kJ·mol-1、②N2(g)+3H2(g)⇌2NH3(g) △H=-93kJ•mol-1;③2H2(g)+O2(g)═2H2O(g)△H=-467KJ/mol,根据盖斯定律可得[①×2-②]×2+3×③:4NH3(g)+7O2(g)==4NO2(g)+6H2O(g) ΔH=-1079kJ·mol-1;正确答案:4NH3(g)+7O2(g)==4NO2(g)+6H2O(g) ΔH=-1079 kJ·mol-1。 能力拓展: 6.【浙江金丽衢十二校2019届高三第二次联考】已知:H2(g)+Cl2(g)2HCl(g)的反应能量变化示意图如下。下列说法不正确的是 ( ) A.键的断裂过程是吸热过程,键的形成过程是放热过程 B.“假想的中间物质”的总能量高于起始态H2和Cl2的总能量 C.反应的△H=[(a+b)-2c]kJ/mol D.点燃条件和光照条件下,反应的△H不同 【答案】D 7.【山东临沂市2019届高三2月质检】Li/Li2O体系的能量循环图如图所示。下列说法正确的是 ( ) A.△H3<0 B.△H3+△H4+△H5=△H6 C.△H6>△H5 D.△H1+△H2+△H3+△H4+△H5+△H6=0 【答案】C 【解析】A.由O2的气态分子变为气态原子,需要断裂分子中的化学键,因此要吸收能量,△H3>0,A错误;B. 根据盖斯定律可知:物质含有的能量只与物质的始态与终态有关,与反应途径无关,根据物质转化关系图可知:△H1+△H2+△H3+△H4+△H5=△H6,所以B错误;C.根据物质转化关系图可知:△H1+△H2+△H3+△H4+△H5=△H6,△H1>0,△H2>0,△H3>0,△H4>0,所以△H6>△H5,C正确;D. 根据选项B分析可知△H1+△H2+△H3+△H4+△H5=△H6,所以△H1+△H2+△H3+△H4+△H5-△H6=0,D错误;故合理选项是C。 8.【上海市金山区2019届高三一模】图分别表示红磷、白磷燃烧时的能量变化,下列说法中正确的是 ( ) A.白磷比红磷稳定 B.白磷燃烧产物比红磷燃烧产物稳定 C.1mol白磷转变为红磷放出2244.7kJ的热量 D.红磷燃烧的热化学方程式:4P(s)+5O2(g)=P4O10(s)△H=-2954kJ⋅mol−1 【答案】D 9.【天津蓟州等部分区2019届高三上学期期末】已知:①2H2(g) + O2(g)=2H2O(g) ΔH=-483.6 kJ·mol-1②H2(g) + S(g) =H2S(g) ΔH=-20.1 kJ·mol-1,下列判断正确的是 ( ) A.若反应②中改用固态硫,则1 mol S(s)完全反应放出的热量小于20.1 kJ B.从焓变数值知,单质硫与氧气相比,更容易与氢气化合 C.由①②知,水的热稳定性小于硫化氢 D.氢气的燃烧热为241.8 kJ·mol-1 【答案】A 10.【黑龙江鹤岗市一中2019届高三第一次月考】Ⅰ) (1)实验中能观察到的现象是____________________。(选填代号) A.试管中镁片逐渐溶解 B.试管中产生无色气泡 C.烧杯外壁变冷 D.烧杯底部析出少量白色固体 (2)由实验推知,MgCl2溶液和H2的总能量________(填“大于”“小于”“等于”)镁片和盐酸的总能量。 Ⅱ)用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题: (1)从实验装置上看,图中尚缺少的一种玻璃用品是___________,除此之外还有一处错误的是____________________。 (2)大烧杯上如不盖硬纸板,求得的中和热数值(绝对值)__________(填“偏大、偏小、无影响”)。 Ⅲ)(1)煤燃烧的反应热可通过以下两个途径来利用:a.利用煤在充足的空气中直接燃烧产生的反应热;b.先使煤与水蒸气反应得到氢气和一氧化碳,然后使得到的氢气和一氧化碳在充足的空气中燃烧。这两个过程的热化学方程式为: a.C(s)+O2(g)===CO2(g) ΔH=E1 ① b.C(s)+H2O(g)===CO(g)+H2(g)ΔH=E2 ② H2(g)+1/2O2(g)===H2O(g)ΔH=E3 ③ CO(g)+1/2O2(g)===CO2(g)ΔH=E4 ④ 请表达E1、E2、E3、E4之间的关系为E2=_________________。 (2)如图所示在常温常压下,1摩尔NO2 和1摩尔CO完全反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:___________________。 (3)化学反应的焓变与反应物和生成物的键能有关。已知某些化学键的键能如下表所示: 共价键 H—H Cl—Cl H—Cl 键能/(kJ·mol-1) 436 247 434 则反应:H2(g)+Cl2(g)=2HCl(g)的焓变ΔH = ____________________。 【答案】A B D 小于 环形玻璃搅拌棒 小烧杯口和大烧杯口没有平齐(其它合适答案给分) 偏小 E2=E1-E3-E4 NO2(g)+CO(g)=NO(g)+CO2(g) ΔH=-234 kJ·mol-1 ΔH =-185 kJ·mol-1 Ⅱ)(1)由量热计的构造可知该装置的缺少仪器是环形玻璃搅拌棒;中和热测定实验成败的关键是保温工作,内外烧杯为一样高,否则,热量散失大;故答案为:环形玻璃搅拌棒;小烧杯口和大烧杯口没有平齐; (2)大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小,故答案为:偏小; Ⅲ)(1)①C(s)+O2(g)═CO2(g)△H=E1,③H2(g)+O2(g)═H2O(g)△H=E3,④CO(g)+O2(g)═CO2(g)△H=E4,根据盖斯定律,①-③-④可得:C(s)+H2O(g)═CO(g)+H2(g),故E2=E1-E3-E4,故答案为:E1-E3-E4; (2)由图可知,1摩尔NO2和1摩尔CO完全反应生成CO2和NO放出热量为(368-134)kJ=234kJ,反应热化学方程式为:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1,故答案为:NO2(g)+CO(g)═NO(g)+CO2(g)△H=-234 kJ•mol-1; (3)反应热=反应物总键能-生成物总键能,故反应:H2(g)+Cl2(g)═2HCl(g)的焓变△H=436kJ/mol+247kJ/mol-2×434kJ/mol=-185kJ/mol,故答案为:-185 kJ/mol。 自我提升: 11.【湖南邵东县创新实验学校2019届高三第五次月考】下列描述中正确的是 ( ) A.已知C(石墨,s)=C(金刚石,s) ∆H=+1.9kJ·mol-1,则由石墨制取金刚石的反应是吸热反应,金刚石比石墨稳定 B.CO(g)的燃烧热是283.0 kJ·mol-1,则2CO2(g)=2CO(g)+O2(g)反应的∆H=2×(+283.0) kJ·mol-1 C.有些化学反应的发生不会伴随着能量的变化 D.已知2H2(g)+O2(g)=2H2O(g) ∆H=-483.6 kJ·mol-1,则氢气的燃烧热为241.8 kJ∙mol-1 【答案】B 12.【西安长安区一中2019届高三第二次检测】根据下列图像的叙述正确的是 ( ) A.图(1)表示的热化学方程式为CO(g)+H2O(l)=CO2(g)+H2(g) ΔH= -41 kJ·mol-1 B.图(2)表示的热化学方程式为CO(g)+H2O(g)=CO2(g)+H2(g) ΔH= +41 kJ·mol-1 C.由图可知正、逆反应的热效应的数值相同 D.两个图像表示的含义相同 【答案】C 13.【长春田家炳实验中学2019届高三12月月考】已知:①CH3OH(g)+ O2(g)===CO2(g)+2H2O(g) ΔH1=-a kJ·mol-1 ②CO(g)+ O2(g)===CO2(g) ΔH2=-b kJ·mol-1 ③H2(g)+O2(g)===H2O(g) ΔH3=-c kJ·mol-1 ④H2(g)+O2(g)===H2O(l) ΔH4=-d kJ·mol-1 下列叙述正确的是 ( ) A.由上述热化学方程式可知ΔH3>ΔH4 B.H2的燃烧热为c kJ·mol-1 C.CH3OH(g)===CO(g)+2H2(g) ΔH=( a- b-2c)kJ·mol-1 D.当CO和H2的物质的量之比为1∶2时,其完全燃烧生成CO2和H2O(l)时,放出Q kJ热量,则混合气中CO的物质的量为 mol 【答案】A 【解析】A. ③ 中产物水为气态,④中产物水为液态,水由液态变为气态需要吸收热量,所以③中放出的热量小于④中放出的热量,即ΔH3>ΔH4,故A正确;B. 燃烧热应该是1mol的可燃物完全燃烧产生稳定的氧化物所放出的热量,水的稳定状态是液体,而c kJ·mol-1是生成气态水时的反应热,故B错误;C. 由盖斯定律得:CH3OH(g)===CO(g)+2H2(g)由热化学方程式①-②-2③而来,所以ΔH=( -a+b+2c)kJ·mol-1,故C错误;D. 由热化学方程式②和④知,当CO和H2的物质的量分别为1mol和2mol时,其完全燃烧生成CO2和H2O(l)时,放出的热量为b+2d kJ,若放出Q kJ热量,则混合气中CO的物质的量为 mol,故D错误。故选A。 14.【江西吉安市2019届高三上学期五校联考】物质A在一定条件下可发生一系列转化,由图判断下列关系错误的是 ( ) A.A→F,△H =一△H6 B.△H1 +△H2 + △H3 + △H4 + △H5 + △H6=0 C.C→F, △H= △H1+ △H2 + △H6 D.若A→C为放热过程,则△H3 + △H4 + △H5 + △H6 >0 【答案】C 15.【江西师大附中2019届上学期期末】按要求回答下列问题 (1)已知拆开1 mol H—H键、1 mol N—H键、1 mol N≡N键分别需要的能量是436 kJ、391 kJ、946 kJ,则N2与H2反应生成NH3的热化学方程式为____________________。 (2)已知碳的燃烧热ΔH1= a kJ·mol-1,S(s)+2K(s)=K2S(s);ΔH2= b kJ·mol-12K(s)+N2(g)+3O2(g)=2KNO3(s) ΔH3= c kJ·mol-1,则S(s)+2KNO3(s)+3C(s)=K2S(s)+N2(g)+3CO2(g) ΔH=____________________。 (3)已知:C(s)+O2(g)=CO2(g) ΔH=-437.3 kJ·mol一1,H2(g)+1/2O2(g)=H2O(g) ΔH=-285.8 kJ·mol一1,CO(g)+1/2O2(g)=CO2(g) ΔH=-283.0 kJ·mol一1,写出煤气化(碳和水蒸气反应生成一氧化碳和氢气)的热化学方程式________,计算10m3(标况)水煤气完全燃烧放出的热量为_________kJ(结果保留到小数点后一位)。 【答案】N2(g) + 3H2(g) = 2NH3(g) ΔH=-92kJ·mol一1 (3a+b-c)kJ·mol一1 C(s)+H2O(g)=CO(g) + H2(g) ΔH=131.5 kJ·mol一1 126964.3 kJ 【解析】(1)在反应N2+3H2⇌2NH3中,断裂3molH-H键,1mol N三N键共吸收的能量为:3×436kJ+946kJ=2254kJ,生成2mol NH3,共形成6mol N-H键,放出的能量为:6×391kJ=2346kJ,吸收的能量少,放出的能量多,该反应为放热反应,放出的热量为:2346kJ-2254kJ=92kJ,则N2与H2反应生成NH3的热化学方程式为:N2(g)+3H2(g)⇌2NH3(g) △H=-92kJ•mol-1;因此,正确答案是:N2(g)+3H2(g)⇌2NH3(g) △H=-92kJ•mol-1。 (3) 已知:①C(s)+O2(g)=CO2(g)△H=-437.3kJ•mol一1,②H2(g)+1/2O2(g)=H2O(g)△H=-285.8kJ•mol一1,③CO(g)+1/2O2(g)═CO2(g)△H=-283.0kJ•mol-1 根据盖斯定律计算,①-②-③得到固态碳与水蒸汽反应生成一氧化碳和氢气的热化学方程式是:C(s)+H2O(g)=CO2(g)+H2(g)△H=+131.5kJ•mol-1;因此,答案是:C(s)+H2O(g)=CO2(g)+H2(g)△H=+131.5kJ•mol-1, (4)根据反应②③可以知道,每2摩尔水煤气完全燃烧放出的热量为285.8kJ+283.0kJ=568.8kJ,所以10m3(标况)即10000L/22.4=446.43mol,的水煤气完全燃烧放出的热量为446.43×568.8kJ×1/2=126964.3kJ,因此,答案是:C(s)+H2O(g)=CO2(g)+H2(g)△H=-131.5kJ•mol-1;126964.3。 1.对化学反应与能量变化的复习应从两个角度进行,一是从总能量变化的角度,二是从化学键键能的角度。对热化学方程式的复习,一要抓住热化学方程式的书写规则,二要注意题目定量条件的设置。 2.对盖斯定律有关问题的复习,要理解盖斯定律的本质,熟悉历年高考考查类型(图像型、字母型、数值型等)。 查看更多