2018-2019学年湖北省钢城四中高一下学期5月月考化学试卷
钢城四中2018—2019(下)5月考试卷
学科
化学
年级
高一
命题
彭艳敏
审核
易艳霞
时间
90
分值
100’
可能用到的相对原子质量 H 1 B 11 O 16 C 12
一、选择题(每小题只有一个选项是正确每小题3分,总分48分)
1. 在N2+3H22NH3的反应中,经过一段时间后,H2的浓度减少了0.6 mol·L-1。在此段时间内用NH3表示的平均反应速率为0.4 mol·L-1·s-1,则反应所经过的时间是( )
A.0.44 s B.1 s C.1.33 s D.2 s
2.有机物种类繁多的主要原因是 ( )
A.有机物的分子结构十分复杂
B.碳原子能与其他原子形成四个共价键,而且碳原子之间也能互相成键
C.有机物除含碳元素外,还含有其他多种元素
D.自然界中存在多种形式的、大量的有机物
3. 已知某化学反应的平衡常数表达式为K=,在不同的温度下该反应的平衡常数的值分别为:
t℃
700
800
830
1000
1200
K
1.67
1.11
1.00
0.60
0.38
下列说法错误的是( )
A.该反应的化学方程式是:CO(g)+H2O(g) CO2(g)+H2(g)
B.上述反应的正反应是放热反应
C.如果在一定体积的密闭容器中加入CO2和H2各1 mol,5 min后温度升高到830℃,此时测得CO2为0.4 mol时,该反应为平衡状态
D.某温度下,如果平衡浓度符合下列关系式:=,判断此时的温度是1000℃
4. 化学反应4A(s)+3B(g) 2C(g)+D(g),经2 min,B的浓度减少0.6 mol/L。对此反应速率的表示正确的是( )
A.用A表示的反应速率是0.4 mol·(L·min)-1
B.分别用B、C、D表示的反应速率其比值是3∶2∶1
C.2 min末的反应速率用B表示是0.3 mol·(L·min)-1
D.2 min内,v正(B)和v逆(C)表示的反应速率的值都是逐渐减小的
5. 一定温度下的恒容容器中,发生反应A(s)+2B(g)=当C(g)+D(g),下列能表示该反应已达平衡状态的是( )
A.2v(B)正=V(D)逆 B.气体总物质的量不随时间变化而变化
C.混合气体的压强不随时间变化而变化 D.混合气体的密度保持不变
6. 在2A+B 3C+4D反应中,表示该反应速率最快的是( )
A. υ(A)= 0.5 mol/(L·s) B. υ(B)= 0.3 mol/(L·s)
C. υ(C)= 0.8 mol/(L·s) D. υ(D)= 1 mol/(L·s)
A.平衡状态A与C相比,平衡状态A的c(CO)较小
B.在t2时,D点的反应速率:ν(逆)>ν(正)
C.反应CO(g)+H2O(g)CO2(g)+H2(g)的△H>0
D.若t1、t2时的平衡常数分别为K1、K2,则K1<K2
7. 已知某密闭容器中存在下列平衡: CO(g)+H2O(g)CO2(g)+H2(g),CO2的平衡物质的量浓度c(CO2)与温度t的关系如右图所示。下列的说法正确的是 ( )
8. 主链含5个碳原子,有甲基、乙基2个支链的烷烃有( )
A. 2种 B. 3种 C. 4种 D.5种
9. 一容积恒定的密闭容器中盛有1molPCl5,加热到200℃时发生反应:PCl5(g)PCl3(g)+Cl2
(g),反应达到平衡时,混合气体中PCl5的体积分数为M%,若在同一温度和同一容器中,最初投入的是2molPCl5,反应达到平衡时,PCl5的体积分数为N%,则M和N的关系正确的是( )
A.M>N B.M
0,达到平衡时,下列措施:①升温 ②恒容通入惰性气体③增加CO浓度④减压⑤加催化剂⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④ B.①④⑥ C.②③⑤ D.③⑤⑥
15.某链状有机物分子中含m个-CH3,n个-CH2-,a个其余为-OH,则羟基的数目可能是( )
A.2n+3a-m B.a+2-m C.n+m+a D.a+2n+2-m
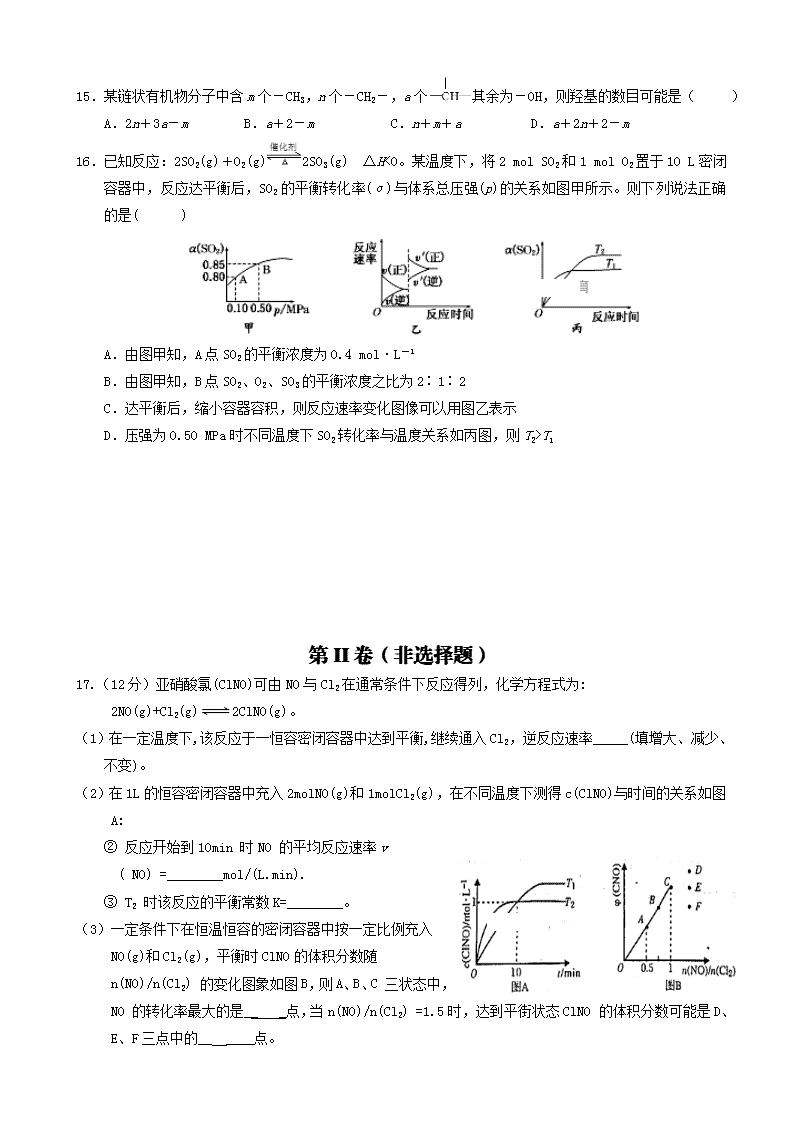
16.已知反应:2SO2(g)+O2(g)2SO3(g) ΔH<0。某温度下,将2 mol SO2和1 mol O2置于10 L密闭容器中,反应达平衡后,SO2的平衡转化率(α)与体系总压强(p)的关系如图甲所示。则下列说法正确的是( )
A.由图甲知,A点SO2的平衡浓度为0.4 mol·L-1
B.由图甲知,B点SO2、O2、SO3的平衡浓度之比为2∶1∶2
C.达平衡后,缩小容器容积,则反应速率变化图像可以用图乙表示
D.压强为0.50 MPa时不同温度下SO2转化率与温度关系如丙图,则T2>T1
第II卷(非选择题)
17.(12分)亚硝酸氯(ClNO)可由NO与Cl2在通常条件下反应得列,化学方程式为:
2NO(g)+Cl2(g)2ClNO(g)。
(1)在一定温度下,该反应于一恒容密闭容器中达到平衡,继续通入Cl2,逆反应速率_____(填增大、减少、不变)。
(2)在1L的恒容密闭容器中充入2molNO(g)和1mol Cl2(g),在不同温度下测得c(ClNO)与时间的关系如图A:
② 反应开始到10min 时NO 的平均反应速率v
( NO) =________mol/(L.min).
③ T2 时该反应的平衡常数K=________。
(3)一定条件下在恒温恒容的密闭容器中按一定比例充入NO(g)和Cl2(g),平衡时ClNO的体积分数随n(NO)/n(Cl2) 的变化图象如图B,则A、B、C 三状态中,NO 的转化率最大的是__ _点,当n(NO)/n(Cl2) =1.5时,达到平街状态ClNO 的体积分数可能是D、E、F三点中的__ ____点。
18.(共13分)合成氨反应是“将空气变成面包”的反应,如果没有合成氨反应,地球将无法养活现在这么多的人。已知合成氨的反应为N2(g)+3H2(g)2NH3(g) ΔH=-92.4 kJ·mol-1。
Ⅰ.在体积为5 L的恒温、恒容密闭容器甲中,起始时投入2 mol N2、3 mol H2,经过10 s达到平衡,测得平衡时NH3的物质的量为0.8 mol。
Ⅱ.在容器乙中,起始时投入3 mol N2、b mol H2,维持恒温、恒压达到平衡,测得平衡时NH3的物质的量为1.2 mol。此时与容器甲中平衡状态温度相同,相同组分的体积分数都相同。
(1)容器甲10 s内用H2表示的平均反应速率v(H2)=________,达平衡时N2的转化率=________。
(2)甲容器中反应的逆反应速率随时间变化的关系如图。t2时改变了某一种条件,改变的条件可能是________、________(填写两项)。
(3)b=________。
19.(共15分)一定温度下在体积为5 L的密闭容器中发生可逆反应。
Ⅰ.若某可逆反应的化学平衡常数表达式为:K=
(1)写出该反应的化学方程式:____________________________________________。
(2)能判断该反应一定达到化学平衡状态的依据是________(填选项编号)。
A.容器中气体的平均相对分子质量不随时间而变化
B.v正(H2O)=v逆(H2)
C.容器中气体的密度不随时间而变化
D.容器中总的物质的量不随时间而变化
E.消耗n mol H2的同时消耗n mol CO
Ⅱ.若该密闭容器中加入的是2 mol Fe(s)与1 mol H2O(g),t1 s时,H2的物质的量为0.20 mol,到第t2 s时恰好达到平衡,此时H2的物质的量为0.35 mol 。
(1) t1~t2这段时间内的化学反应速率
v(H2)=_______________________________。
(2)若继续加入2 mol Fe(s),则平衡________移动
(填“向正反应方向”、“向逆反应方向”或“不”)。
(3)该反应的逆反应速率随时间变化的关系如图。t1时
改变了某种条件,改变的条件可能是________、
________(填写2项)
20.(共12分)一定条件下,在体积为3 L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu2O/ZnO)。
根据题意完成下列问题:
(1)反应达到平衡时,平衡常数表达式K=__________,升高温度,K值______(填“增大”、“减小”或“不变”)。
(2)在500 ℃,从反应开始到平衡,氢气的平均反应速率v(H2)=________________。
(3)在其他条件不变的情况下,对处于E点的体系体积压缩到原来的1/2,下列有关该体系的说法正确的是________。
a.氢气的浓度减小 b.正反应速率加快,逆反应速率也加快
c.甲醇的物质的量增加 d.重新平衡时n(H2)/n(CH3OH)增大
(4)据研究,反应过程中起催化作用的为Cu2O,反应体系中含少量CO2有利于维持催化剂Cu2O的量不变,原因是____________________________(用化学方程式表示)。
2018-2019学年度下学期5月考试高一化学答案
选择题:
1b 2b 3c 4b 5d 6b 7a 8a 9b 10b11a12b 13c 14b15b16c
17(12分)、(1) 增大
② 0.1 (3分) ; ③ 2(3分)
(4) A ; D
18(13分)
(1)0.024 mol·L-1·s-1 (3分) 20%(3分)
(2)升高了温度 增大了氨的浓度 (4分)
(3)4.5(3分)
19.(15分)
(Ⅰ)(1)C(s)+H2O(g)CO(g)+H2 (g)
(2)A、B、C D(4分)
(Ⅱ)(1) mol·L-1·s-1(3分)
(2) 不
(3)升高了温度、增大了H2O的浓度(任答2条) (4分)
20.(12分) (1) 减小
(2) mol/(L·min) (3分)
(3)bc (4)Cu2O+CO2Cu+CO2(3分)