- 2021-04-14 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019届一轮复习人教版晶体结构与性质作业(7)
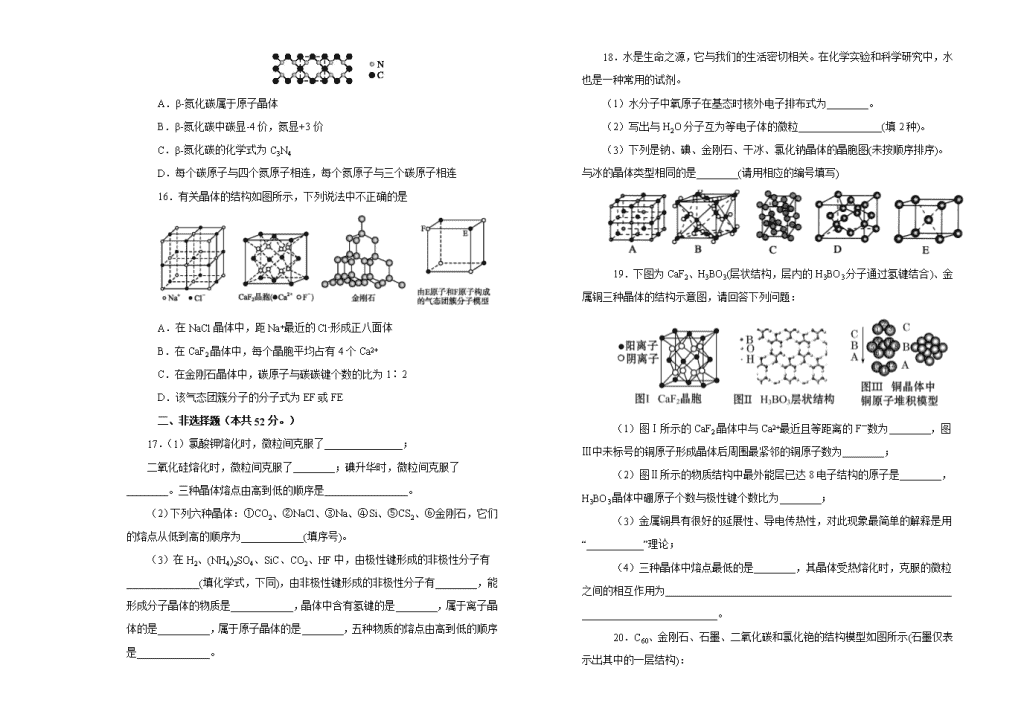
晶体结构与性质 可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Al 32 S 32 Cl 35.5 K 23 Cu 14 一、选择题(本题包括16小题,每小题3分,共48分。每小题只有一个选项符合题意。) 1.下列物质所属晶体类型分类正确的是 A B C D 原子晶体 石墨 生石灰 碳化硅 金刚石 分子晶体 冰 固态氨 氯化铯 干冰 离子晶体 氮化铝 食盐 明矾 芒硝 金属晶体 铜 汞 铝 铁 2.由短周期元素构成的某离子化合物中,一个阳离子和一个阴离子核外电子数之和为20。下列说法中正确的是 A.晶体中阳离子和阴离子的个数不一定相等 B.晶体中一定只有离子键没有共价键 C.所含元素一定不在同一周期也不在第一周期 D.晶体中阳离子半径一定大于阴离子半径 3.下列物质发生变化时,所克服的粒子间相互作用属同种类型的是 A.碘与干冰分别受热变为气体 B.硝酸铵与硝酸分别受热变为气体 C.氯化钠与氯化氢分别溶解在水中 D.晶体钠与冰分别受热熔化 4.下列性质适合于离子晶体的是 A.熔点-218℃,难溶于水 B.熔点3900℃,硬度很大,不导电 C.难溶于水,固体时导电,升温时导电能力减弱 D.难溶于水,熔点高,固体不导电,熔化时导电 5.下列说法正确的是 A.原子晶体中只存在非极性共价键 B.因为HCl的相对分子质量大于HF,所以HCl的沸点高于HF C.干冰升华时,分子内共价键不会发生断裂 D.金属元素和非金属元素形成的化合物一定是离子化合物 6.下列各物质中,按熔点由高到低的顺序排列正确的是 A.CH4>SiH4>GeH4>SnH4 B.KCl>NaCl>MgCl2>MgO C.Rb>K>Na>Li D.石墨>金刚石>SiO2>钠 7.根据下表给出物质的熔点数据(AlCl3沸点为160℃),判断下列说法错误的是 晶体 NaCl MgO SiCl4 AlCl3 晶体硼 熔点/℃ 801 2800 -70 180 2500 A.MgO中的离子键比NaCl中的离子键强 B.SiCl4晶体是分子晶体 C.AlCl3晶体是离子晶体 D.晶体硼是原子晶体 8.钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是 A.该晶体属于离子晶体 B.晶体的化学式为Ba2O2 C.该晶体晶胞结构与NaCl相似 D.与每个Ba2+距离相等且最近的Ba2+共有12个 9.下列数据是对应物质的熔点表,有关的判断正确的是 Na2O Na AlF3 AlCl3 920℃ 97.8℃ 1291℃ 190℃ Al2O3 BCl3 CO2 SiO2 2073℃ -107℃ -57℃ 1723℃ A.只要含有金属阳离子的晶体就一定是离子晶体 B.在共价化合物中各原子都形成8电子结构 C.同族元素的氧化物不可能形成不同类型的晶体 D.金属晶体的熔点不一定比分子晶体的高 10.同主族元素所形成的同一类型的化合物,其结构和性质往往相似,化合物PH4I是一种无色晶体,下列对它的描述中不正确的是 A.在加热此化合物时有紫色气体产生 B.它是一种离子化合物 C.这种化合物不能跟强碱发生化学反应 D.该化合物在一定条件下由PH3与HI化合而成 11.某固体仅由一种元素组成,其密度为5.0 g·cm−3,用X射线研究该固体的结构时得知:在边长1×10−7 cm的正方体中含有20个原子,则此元素的相对原子质量最接近下列数据中的 A.32 B.120 C.150 D.180 12.下列关于晶体的说法一定正确的是 CaTiO3的晶体结构模型(Ca2+、O2−、Ti4+分别位于立方体的体心、面心和顶点) A.分子晶体中都存在共价键 B.金属晶体的熔点都比分子晶体的熔点高 C.SiO2晶体中每个硅原子与两个氧原子以共价键相结合 D.CaTiO3晶体中每个Ti4+与12个O2−相紧邻 13.石墨烯是由碳原子构成的单层片状结构的新材料(结构示意图如图),可由石墨剥离而成,具有极好的应用前景。下列说法正确的是 A.石墨烯与石墨互为同位素 B.0.12 g石墨烯中含6.02×1022个碳原子 C.石墨烯是一种有机物 D.石墨烯中碳原子间以共价键结合 14.下面的排序不正确的是 A.晶体熔点的高低: B.熔点由高到低:Na>Mg>Al C.硬度由大到小:金刚石>碳化硅>晶体硅 D.晶格能由大到小:NaF>NaCl>NaBr>NaI 15.氮化碳结构如下图,其中β-氮化碳硬度超过金刚石晶体,成为首屈一指的超硬新材料。下列有关氮化碳的说法中错误的是 A.β-氮化碳属于原子晶体 B.β-氮化碳中碳显-4价,氮显+3价 C.β-氮化碳的化学式为C3N4 D.每个碳原子与四个氮原子相连,每个氮原子与三个碳原子相连 16.有关晶体的结构如图所示,下列说法中不正确的是 A.在NaCl晶体中,距Na+最近的Cl-形成正八面体 B.在CaF2晶体中,每个晶胞平均占有4个Ca2+ C.在金刚石晶体中,碳原子与碳碳键个数的比为1∶2 D.该气态团簇分子的分子式为EF或FE 二、非选择题(本共52分。) 17.(1)氯酸钾熔化时,微粒间克服了_______________; 二氧化硅熔化时,微粒间克服了________;碘升华时,微粒间克服了________。三种晶体熔点由高到低的顺序是________________。 (2)下列六种晶体:①CO2、②NaCl、③Na、④Si、⑤CS2、⑥金刚石,它们的熔点从低到高的顺序为____________(填序号)。 (3)在H2、(NH4)2SO4、SiC、CO2、HF中,由极性键形成的非极性分子有______________(填化学式,下同),由非极性键形成的非极性分子有________,能形成分子晶体的物质是____________,晶体中含有氢键的是________,属于离子晶体的是__________,属于原子晶体的是________,五种物质的熔点由高到低的顺序是______________。 18.水是生命之源,它与我们的生活密切相关。在化学实验和科学研究中,水也是一种常用的试剂。 (1)水分子中氧原子在基态时核外电子排布式为________。 (2)写出与H2O分子互为等电子体的微粒________________(填2种)。 (3)下列是钠、碘、金刚石、干冰、氯化钠晶体的晶胞图(未按顺序排序)。与冰的晶体类型相同的是________(请用相应的编号填写) 19.下图为CaF2、H3BO3(层状结构,层内的H3BO3分子通过氢键结合)、金属铜三种晶体的结构示意图,请回答下列问题: (1)图Ⅰ所示的CaF2晶体中与Ca2+最近且等距离的F-数为________,图Ⅲ中未标号的铜原子形成晶体后周围最紧邻的铜原子数为________; (2)图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是________,H3BO3晶体中硼原子个数与极性键个数比为________; (3)金属铜具有很好的延展性、导电传热性,对此现象最简单的解释是用“___________”理论; (4)三种晶体中熔点最低的是________,其晶体受热熔化时,克服的微粒之间的相互作用为_______________________________________________________ __________________________。 20.C60、金刚石、石墨、二氧化碳和氯化铯的结构模型如图所示(石墨仅表示出其中的一层结构): (1)C60、金刚石和石墨三者的关系是互为 。 A.同分异构体 B.同素异形体 C.同系物 D.同位素 (2)固态时,C60属于 (填“原子”或“分子”)晶体,C60分子中含有双键的数目是 。 (3)晶体硅的结构跟金刚石相似,1mol晶体硅中含有硅—硅单键的数目约是 NA。 (4)石墨层状结构中,平均每个正六边形占有的碳原子数是 。 (5)观察CO2分子晶体结构的一部分,试说明每个CO2分子周围有 个与之紧邻且等距的CO2分子;该结构单元平均占有 个CO2分子。 (6)观察图形推测,CsCl晶体中两距离最近的Cs+间距离为a,则每个Cs+周围与其距离为a的Cs+数目为 ,每个Cs+周围距离相等且次近的Cs+数目为 ,距离为 ,每个Cs+周围距离相等且第三近的Cs+数目为 ,距离为 ,每个Cs+周围紧邻且等距的Cl−数目为 。 21.某离子晶体的晶胞结构如图所示。试求: (1)晶体中每一个Y同时吸引着________个X,每个X同时吸引着________个Y,该晶体的化学式是________________________。 (2)晶体中在每个X周围与它最接近且距离相等的X共有________个。 (3)晶体中距离最近的2个X与一个Y形成的夹角(∠XYX)为________。 (4)设该晶体的摩尔质量为M g·mol−1,晶体密度为ρ g·cm−3,阿伏加德罗常数为NA,则晶体中两个距离最近的X中心间距离为________cm。 答案解析 1. 【解析】石墨属于混合晶体,生石灰、氯化铯属于离子晶体,氮化铝属于原子晶体,故只有D正确。 【答案】D 2. 【解析】在短周期中符合题设条件的物质有:NaF、Na2O、MgO、NaOH、NH4F等,故A正确;NaOH、NH4F含共价键,故B不正确;所含元素可在同一周期,也可在第一周期,如NH4F,故C不正确;NaF、Na2O、MgO等其阳离子半径都比阴离子半径小,故D不正确。 【答案】A 3. 【解析】碘、干冰都是分子晶体,且都无氢键,变为气体时只克服范德华力;硝酸铵是离子晶体变为气体时克服离子键和共价键,硝酸是分子晶体,且含有氢键,变为气体时需克服范德华力和氢键;氯化钠、氯化氢溶于水分别克服离子键、共价键;晶体钠与冰受热熔化分别克服金属键、分子间作用力。 【答案】A 4. 【解析】离子晶体液态时能导电,难溶于非极性溶剂,熔点较高、质硬而脆,固体不导电,故A、C均不符合离子晶体的特点;B中熔点达3900℃,硬度很大,不导电,应是原子晶体,故只有D符合题意。 【答案】D 5. 【解析】A项SiO2中存在极性键;B项HF分子间含有氢键,故HF沸点高;D项AlCl3为共价化合物。 【答案】C 6. 【解析】晶体熔点的高低取决于构成该晶体的结构粒子间作用力的大小。A项物质均为结构相似的分子晶体,相对分子质量越大者分子间作用力也越大,故A项各物质熔点应为逐渐升高的顺序;B项物质均为离子晶体,离子晶体熔点高低取决于离子键键能的大小,一般来说,离子的半径越小,电荷越多,离子键的键能就越大,故B项各物质熔点也应为升高顺序;C项物质均为同主族的金属晶体,其熔点高低取决于金属键的强弱,金属原子半径越小,价电子数越多,金属键越强。碱金属原子半径依Li→Cs的顺序增大,价电子数相同,故熔点应是Li最高,Cs最低;原子晶体的熔点取决于共价键的键能,石墨中C—C键键长比金刚石中C—C键的键长更短,键能更大,所以石墨熔点比金刚石略高,金刚石熔点又比二氧化硅高,钠的熔点很低。 【答案】D 7. 【解析】NaCl和MgO是离子化合物,形成离子晶体,故熔、沸点越高,说明晶格能越大,离子键越强,A项正确;SiCl4是共价化合物,熔、沸点较低,为分子晶体;硼为非金属单质,熔、沸点很高,是原子晶体,B、D项正确;AlCl3虽是由活泼金属和活泼非金属形成的化合物,但其晶体熔、沸点较低,应属于分子晶体。 【答案】C 8. 【解析】由晶胞结构及“均摊法”计算:一个晶胞中含Ba2+:8×1/8+6× 1/2=4个,含O:12×1/4+1=4个,故晶体化学式是BaO2,其他选项可结合NaCl晶胞知识作出判断。 【答案】B 9. 【解析】金属晶体中含有金属阳离子,但不属于离子晶体,A错;BCl3分子中硼原子的最外层只有6个电子,B错;CO2和SiO2分别属于分子晶体和原子晶体,C错;Na的熔点低于AlCl3,D正确。 【答案】D 10. 【解析】此题为信息题,可把PH看作NH来回答。因铵盐易分解且是离子化合物,分解产生的HI不稳定,易分解,故A、B项正确;NH3与HI易化合,故D项正确;又NH与OH−能反应,故PH与OH−能反应,故C项不正确。 【答案】C 11. 【解析】M=Vm·ρ=×6.02×1023 mol−1×5. 0 g·cm−3≈150g·mol−1,故Mr=150。 【答案】C 12. 【解析】A项分子晶体中的稀有气体仅以分子间作用力结合,无共价键存在;B项中金属汞常温为液态,比I2、S的熔点低;C项中每个硅原子连接4个氧原子。D项选择一个顶点的Ti4+,则该立方体中与其紧邻的O2−占3个,而面心上的O2−占,顶点上的Ti4+占,故其紧邻的O2−个数为3×8×=12。 【答案】D 13. 【解析】石墨烯与石墨均为碳单质,两者互为同素异形体,故A、C错误;0.12 g石墨烯为0.01 mol,碳原子数为6.02×1021个,故B项错误;由题意可知石墨烯应该是单层的石墨,其结构与石墨相似,碳原子之间以共价键结合。 【答案】D 14. 【解析】A中,由于可以形成分子内氢键,使得晶体熔点降低。B中,Na、Mg、Al均为金属晶体,金属键Na查看更多