- 2021-04-14 发布 |
- 37.5 KB |
- 4页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2021新高考化学鲁科版一轮复习突破精练:第4章 专题突破15 喷泉实验及拓展应用
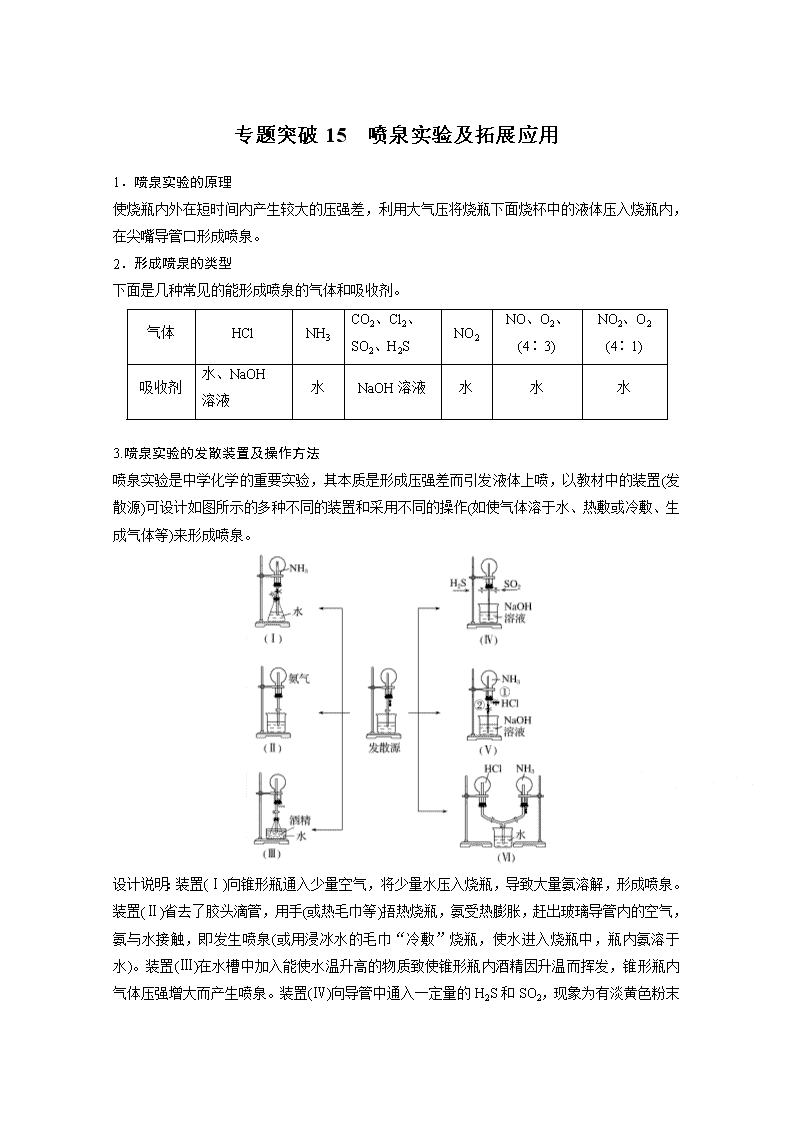
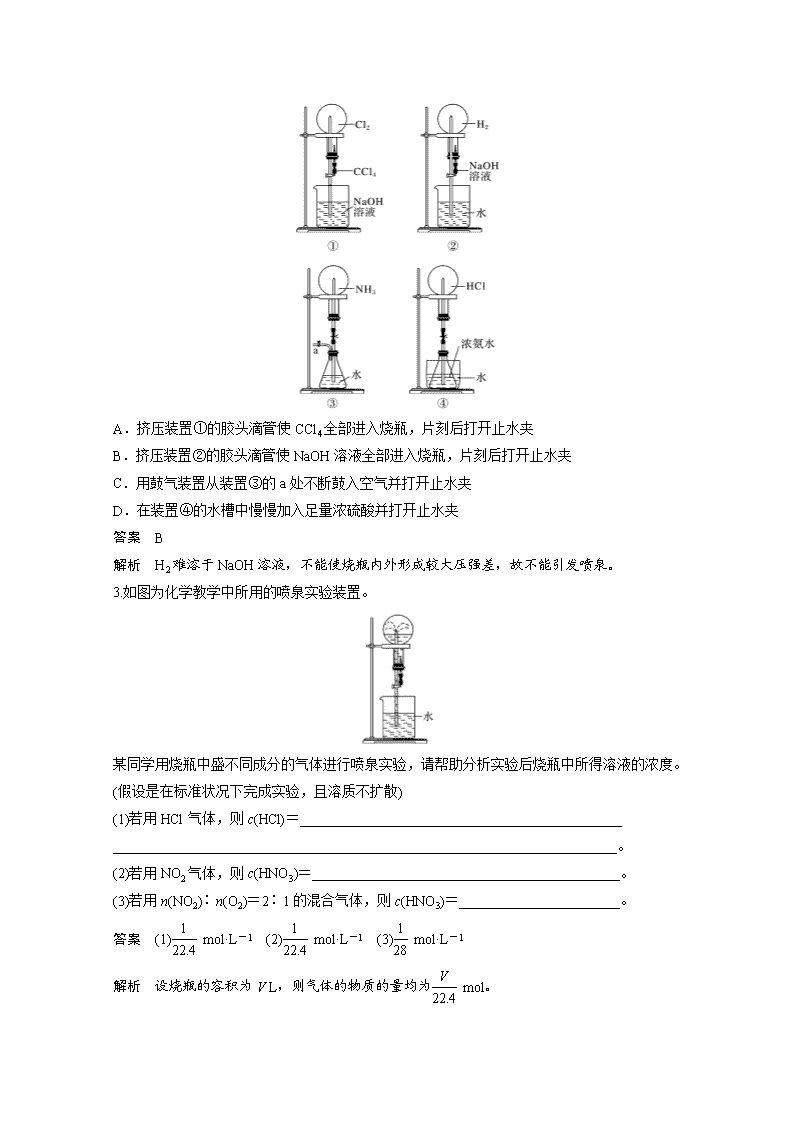
专题突破 15 喷泉实验及拓展应用 1.喷泉实验的原理 使烧瓶内外在短时间内产生较大的压强差,利用大气压将烧瓶下面烧杯中的液体压入烧瓶内, 在尖嘴导管口形成喷泉。 2.形成喷泉的类型 下面是几种常见的能形成喷泉的气体和吸收剂。 气体 HCl NH3 CO2、Cl2、 SO2、H2S NO2 NO、O2、 (4∶3) NO2、O2 (4∶1) 吸收剂 水、NaOH 溶液 水 NaOH 溶液 水 水 水 3.喷泉实验的发散装置及操作方法 喷泉实验是中学化学的重要实验,其本质是形成压强差而引发液体上喷,以教材中的装置(发 散源)可设计如图所示的多种不同的装置和采用不同的操作(如使气体溶于水、热敷或冷敷、生 成气体等)来形成喷泉。 设计说明:装置(Ⅰ)向锥形瓶通入少量空气,将少量水压入烧瓶,导致大量氨溶解,形成喷泉。 装置(Ⅱ)省去了胶头滴管,用手(或热毛巾等)捂热烧瓶,氨受热膨胀,赶出玻璃导管内的空气, 氨与水接触,即发生喷泉(或用浸冰水的毛巾“冷敷”烧瓶,使水进入烧瓶中,瓶内氨溶于水)。 装置(Ⅲ)在水槽中加入能使水温升高的物质致使锥形瓶内酒精因升温而挥发,锥形瓶内气体压 强增大而产生喷泉。装置(Ⅳ)向导管中通入一定量的 H2S 和 SO2,现象为有淡黄色粉末状物质 生成,瓶内壁附有水珠,NaOH 溶液上喷形成喷泉。装置(Ⅴ)打开①处的止水夹并向烧瓶中缓 慢通入等体积的 HCl 气体后关闭该止水夹,等充分反应后再打开②处的止水夹,观察到先有 白烟产生,后产生喷泉。装置(Ⅵ)中,挤压胶头滴管,然后打开导管上部的两个活塞,则在右 面烧瓶出现喷烟现象,再打开导管下部活塞,则可产生双喷泉。 4.喷泉实验产物的浓度计算 关键是确定所得溶液中溶质的物质的量和溶液的体积,标准状况下的气体进行喷泉实验后所 得溶液的物质的量浓度: (1)HCl、NH3、NO2气体或它们与其他不溶于水的气体混合时:所得溶液的物质的量浓度为 1 22.4 mol·L-1。 (2)当是 NO2 和 O2 的混合气体且体积比为 4∶1 时,c(HNO3)= 1 28 mol·L-1。 1.如图装置中,干燥烧瓶内盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,下 列与实验事实不相符的是( ) A.CO2(NaHCO3 溶液)/无色喷泉 B.NH3(H2O 中含酚酞)/红色喷泉 C.H2S(CuSO4 溶液)/黑色喷泉 D.HCl(AgNO3 溶液)/白色喷泉 答案 A 解析 二氧化碳难溶于碳酸氢钠溶液,不能产生压强差,无法形成喷泉,A 项与实验事实不相 符。 2.(2018·沈阳质检)下图是课外活动小组的同学设计的 4 个喷泉实验方案,下列有关操作不可 能引发喷泉的是( ) A.挤压装置①的胶头滴管使 CCl4 全部进入烧瓶,片刻后打开止水夹 B.挤压装置②的胶头滴管使 NaOH 溶液全部进入烧瓶,片刻后打开止水夹 C.用鼓气装置从装置③的 a 处不断鼓入空气并打开止水夹 D.在装置④的水槽中慢慢加入足量浓硫酸并打开止水夹 答案 B 解析 H2 难溶于 NaOH 溶液,不能使烧瓶内外形成较大压强差,故不能引发喷泉。 3.如图为化学教学中所用的喷泉实验装置。 某同学用烧瓶中盛不同成分的气体进行喷泉实验,请帮助分析实验后烧瓶中所得溶液的浓度。 (假设是在标准状况下完成实验,且溶质不扩散) (1)若用 HCl 气体,则 c(HCl)=______________________________________________ ________________________________________________________________________。 (2)若用 NO2 气体,则 c(HNO3)=____________________________________________。 (3)若用 n(NO2)∶n(O2)=2∶1 的混合气体,则 c(HNO3)=_______________________。 答案 (1) 1 22.4 mol·L-1 (2) 1 22.4 mol·L-1 (3) 1 28 mol·L-1 解析 设烧瓶的容积为 V L,则气体的物质的量均为 V 22.4 mol。 (1)若是 HCl 气体,喷泉后,溶液充满烧瓶, 则溶液的体积为 V L,c(HCl)= V 22.4 mol V L = 1 22.4 mol·L-1。 (2)若为 NO2,喷泉后,溶质为 HNO3, 3NO2+H2O===2HNO3+NO V 22.4 mol 2 3 × V 22.4 mol 则喷泉后溶液的体积为 2 3V L, c(HNO3)= 2 3 × V 22.4 mol 2 3V L = 1 22.4 mol·L-1。 4.(2020·开封检测)利用如图所示的装置,可以验证 NH3 和 HCl 的有关性质。实验前 a、b、c 活塞均关闭。 (1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶Ⅰ中不产生“喷泉”现象,其操作方法是 ________________________________________________________________________。 (2) 若 先 打 开 a 、 c 活 塞 , 再 挤 压 胶 头 滴 管 , 在 烧 瓶 中 可 观 察 到 的 现 象 是 ________________________________________________________________________。 (3)通过挤压胶头滴管和控制活塞的开关,在烧瓶Ⅰ中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷 泉”现象,其操作方法是_______________________________________________ ________________________________________________________________________。 若要在该装置中产生双喷泉现象,其操作方法是______________________________ ________________________________________________________________________ ________________________________________________________________________。 答案 (1)先打开 a、b 活塞,再挤压胶头滴管(或先挤压胶头滴管,再打开 a、b 活塞) (2)烧瓶Ⅱ中导管口处产生白烟 (3)先打开 a、c 活塞,再挤压胶头滴管(或先打开 a 活塞,挤压胶头滴管,再打开 c 活塞),片 刻后,关闭 a 活塞,然后打开 b 活塞 先打开 a、c 活塞,再挤压胶头滴管(或先打开 a 活塞, 挤压胶头滴管,再打开 c 活塞),片刻后,打开 b 活塞 解析 (1)打开 a、b 活塞,再将胶头滴管中的水挤入烧瓶Ⅱ中,由于 NH3 极易溶于水,使烧瓶 内气体压强迅速减小,烧杯中的水迅速进入烧瓶Ⅱ中,形成喷泉。 (2)先打开 a、c 活塞,再将胶头滴管中的水挤入烧瓶Ⅱ中,烧瓶Ⅱ中的压强迅速减小,烧瓶Ⅰ 中的 HCl 气体会进入到烧瓶Ⅱ中,且与 NH3 化合生成 NH4Cl 而产生白烟。 (3)在(2)基础上,若关闭 a 活塞,打开 b 活塞,烧杯中的水会迅速进入烧瓶Ⅰ中,形成喷泉; 若打开 b 活塞,不关闭 a 活塞,烧瓶中的水便会同时进入烧瓶Ⅰ和Ⅱ中,形成双喷泉。查看更多