备战2021 高考化学 加餐练26 盐类的水解
加餐练 26 盐类的水解
基础题
1.25 ℃时,浓度均为 0.2 mol·L-1 的 NaHCO3 和 Na2CO3 溶液中,下列判断不正确的是
( )
A.均存在电离平衡和水解平衡
B.存在的粒子种类相同
C.c(OH-)前者大于后者
D.分别加入 NaOH 固体,恢复到原温度,c(CO2-
3 )均增大
2.0.1 mol·L-1AlCl3 溶液,温度从 20 ℃升高到 50 ℃,浓度增幅最大的离子是( )
A.Cl- B.Al3+ C.H+ D.OH-
3.短周期元素 W、X、Y、Z 的原子序数依次增大,其简单离子都能破坏水的电离平衡
的是( )
A.W2-、X+ B.X+、Y3+
C.Y3+、Z2- D.X+、Z2-
4.下列物质在常温时发生水解,对应的离子方程式正确的是( )
A.Na2CO3:CO2-
3 +2H2O H2CO3+2OH-
B.NH4Cl:NH+
4 +H2O NH3↑+H2O+H+
C.CuSO4:Cu2++2H2O Cu(OH)2+2H+
D.NaF:F-+H2O===HF+OH-
5.常温下,稀释 0.1 mol·L-1 NH4Cl 溶液,如图中的横坐标表示加水的量,则纵坐标可
以表示的是( )
A.NH +
4 水解的平衡常数
B.溶液的 pH
C.溶液中 NH +
4 数
D.溶液中 c(NH+
4 )
6.已知 t ℃时,水的离子积为 Kw,该温度下,将 a mol·L-1 氨水溶液和 b mol·L-1 HCl
溶液等体积混合,下列判断一定正确的是( )
A.若 c(OH-)= Kw mol·L-1,则混合液一定呈中性
B.若 a>b,则混合液中的 c(NH+
4 )大于 c(Cl-)
C.若溶液呈酸性,则 a
②>④>③
D.NaHCO3 溶液中,c(Na+)=c(CO2-
3 )+c(HCO-
3 )+c(H2CO3)
8.用物质的量都是 0.1 mol 的 CH3COOH 和 CH3COONa 配成 1 L 混合溶液,已知其中
c(CH3COO-)>c(Na+),对该溶液的下列判断正确的是( )
A.c(H+)>c(OH-)
B.c(CH3COO-)=0.1 mol·L-1
C.c(CH3COOH)>c(CH3COO-)
D.c(CH3COO-)+c(OH-)=0.1 mol·L-1
能力题
9.25 ℃时,用 0.25 mol·L-1 的 NaOH 溶液,分别滴定同浓度的三种稀酸溶液,滴定的
曲线如图所示,下列判断不正确的是( )
A.同浓度的稀酸中:c(A-)>c(B-)>c(D-)
B.滴定至 P 点时,溶液中:c(B-)>c(HB)
C.pH=7 时,三种溶液中:c(A-)>c(B-)>c(D-)
D.当中和百分数达 100%时,将三种溶液混合后:
c(HA)+c(HB)+c(HD)=c(OH-)-2c(H+)
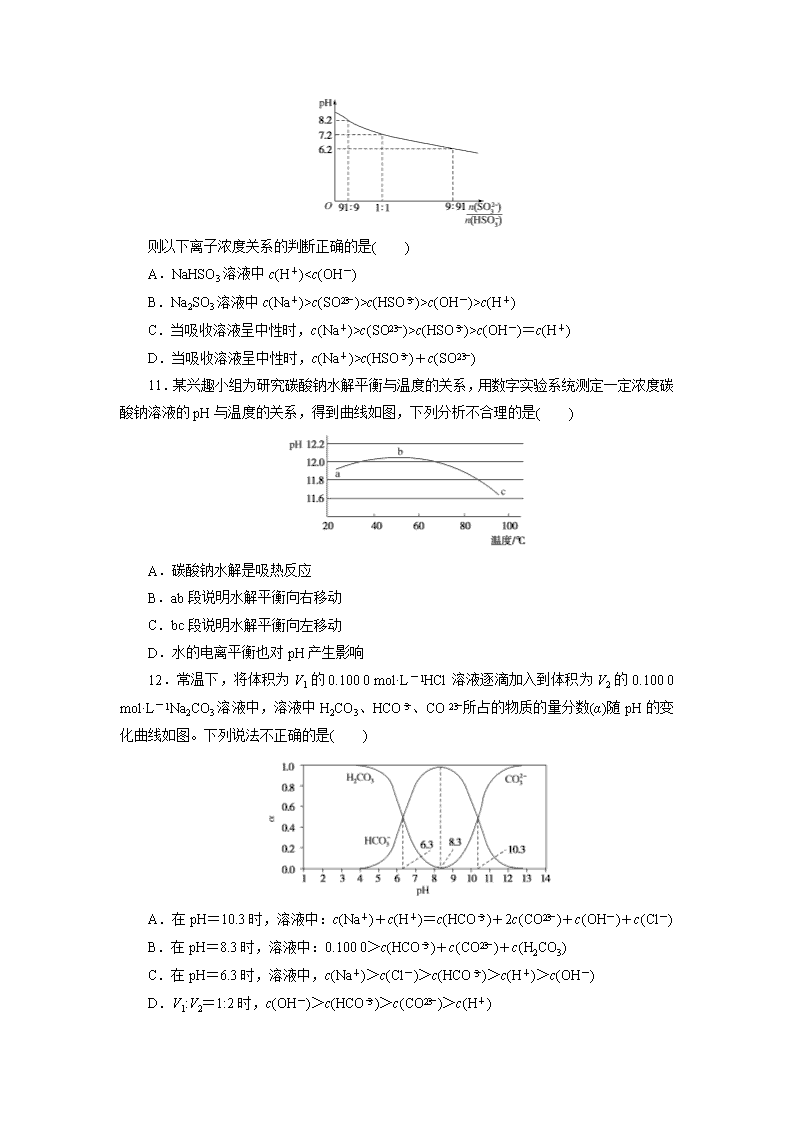
10.Na2SO3 溶液作为吸收液吸收 SO2 时,吸收液 pH 随 n(SO2-
3 ) n(HSO-
3 )变化图像如
图:
则以下离子浓度关系的判断正确的是( )
A.NaHSO3 溶液中 c(H+)c(SO2-
3 )>c(HSO-
3 )>c(OH-)>c(H+)
C.当吸收溶液呈中性时,c(Na+)>c(SO2-
3 )>c(HSO-
3 )>c(OH-)=c(H+)
D.当吸收溶液呈中性时,c(Na+)>c(HSO-
3 )+c(SO2-
3 )
11.某兴趣小组为研究碳酸钠水解平衡与温度的关系,用数字实验系统测定一定浓度碳
酸钠溶液的 pH 与温度的关系,得到曲线如图,下列分析不合理的是( )
A.碳酸钠水解是吸热反应
B.ab 段说明水解平衡向右移动
C.bc 段说明水解平衡向左移动
D.水的电离平衡也对 pH 产生影响
12.常温下,将体积为 V1 的 0.100 0 mol·L-1HCl 溶液逐滴加入到体积为 V2 的 0.100 0
mol·L-1Na2CO3 溶液中,溶液中 H2CO3、HCO-
3 、CO 2-
3 所占的物质的量分数(α)随 pH 的变化
曲线如图。下列说法不正确的是( )
A.在 pH=10.3 时,溶液中:c(Na+)+c(H+)=c(HCO-
3 )+2c(CO2-
3 )+c(OH-)+c(Cl-)
B.在 pH=8.3 时,溶液中:0.100 0>c(HCO-
3 )+c(CO2-
3 )+c(H2CO3)
C.在 pH=6.3 时,溶液中,c(Na+)>c(Cl-)>c(HCO-
3 )>c(H+)>c(OH-)
D.V1:V2=1:2 时,c(OH-)>c(HCO-
3 )>c(CO2-
3 )>c(H+)
13.下列根据反应原理设计的应用,不正确的是( )
A.CO2-
3 +H2O HCO-
3 +OH-;用热的纯碱溶液清洗油污
B.Al3++3H2O Al(OH)3(胶体)+3H+;明矾净水
C.TiCl4+(x+2)H2O(过量) TiO2·xH2O↓+4HCl;制备 TiO2 纳米粉
D.SnCl2+H2O Sn(OH)Cl↓+HCl;配制氯化亚锡溶液时加入氢氧化钠
14.现有 0.175 mol·L-1 醋酸钠溶液 500 mL(已知醋酸的电离常数 Ka=1.75×10-5)。
(1)写出醋酸钠水解反应的化学方程式:
________________________________________________________________________
________________________________________________________________________。
(2)下列图像能说明醋酸钠的水解反应达到平衡的是
________________________________________________________________________
________________________________________________________________________。
A.溶液中 c(Na+)与反
应时间 t 的关系
B.CH3COO-的水解
速率与反应时间 t 的
关系
C.溶液的 pH 与反应
时间 t 的关系
D.Kw 与反应时间 t 的
关系
(3)在醋酸钠溶液中加入下列少量物质,水解平衡向正反应方向移动的有________。
A.冰醋酸 B.纯碱固体
C.醋酸钙固体 D.氯化铵固体
(4)欲配制 0.175 mol·L-1 醋酸钠溶液 500 mL,可采用以下两种方案:
方案一:用托盘天平称取________g 无水醋酸钠,溶于适量水中,配成 500 mL 溶液。
方案二:用体积均为 250 mL 且浓度均为__________mol·L-1 的醋酸与氢氧化钠两溶液
混合而成(设混合后的体积等于混合前两者体积之和)。
(5)在室温下,0.175 mol·L-1 醋酸钠溶液的 pH 约为________[已知醋酸根离子水解反应
的平衡常数 K= Kw
Ka CH3COOH ]。
15.在含有弱电解质的溶液中,往往有多个化学平衡共存。
(1)一定温度下,向 1 L 0.1 mol·L-1 CH3COOH 溶液中加入 0.1 mol CH3COONa 固体,则
溶液中c CH3COO- ·c H+
c CH3COOH
________(填“增大”“不变”或“减小”);写出表示该混合溶液
中所有离子浓度之间的一个等式
________________________________________________________________________
________________________________________________________________________。
(2)土壤的 pH 一般在 4~9 之间。土壤中 Na2CO3 含量较高时,pH 可高达 10.5,试用离
子方程式解释土壤呈碱性的原因
________________________________________________________________________
________________________________________________________________________。
加入石膏(CaSO4·2H2O)可以使土壤碱性降低,有关反应的化学方程式为
________________________________________________________________________
________________________________________________________________________。
(3)常温下在 20 mL 0.1 mol·L-1 Na2CO3 溶液中逐滴加入 0.1 mol·L-1HCl 溶液 40 mL,溶
液中含碳元素的各种微粒(CO2 因逸出未画出)物质的量分数(纵轴)随溶液 pH 变化的部分情
况如图所示。
回答下列问题:
①在同一溶液中,H2CO3、HCO-
3 、CO2-
3 ________(填“能”或“不能”)大量共存;
②当 pH=7 时,溶液中含碳元素的主要微粒为________,溶液中各种离子的物质的量
浓度的大小关系为__________________________________________________;
③已知在 25 ℃时,CO 2-
3 水解反应的平衡常数即水解常数 Kh=c HCO-
3 · c OH-
c CO2-
3
=
2.0×10-4 mol·L-1,当溶液中 c(HCO-
3 ):c(CO2-
3 )=2:1 时,溶液的 pH=________。
加餐练 26 盐类的水解
1.解析:A 项,Na2CO3 溶液中存在水的电离平衡和碳酸根的水解平衡,NaHCO3 在水
溶液中存在碳酸氢根的电离平衡和水解平衡以及水的电离平衡,故 A 正确;B 项,NaHCO3
和 Na2CO3 溶液中存在的微粒均为:钠离子、碳酸根、碳酸氢根、氢氧根、氢离子、碳酸分
子、水分子,存在的粒子种类相同,故 B 正确;C 项,碳酸根的水解程度大于碳酸氢根,
二者水解均显碱性,根据水解规律:谁强显谁性,所以碳酸钠中的氢氧根浓度大于碳酸氢钠
溶液中的氢氧根浓度,故 C 错误;D 项,分别加入 NaOH 固体,恢复到原温度,碳酸氢根
和氢氧根在溶液中反应会生成碳酸根和水,氢氧根对它们的水解均起到抑制作用,所以
c(CO2-
3 )均增大,故 D 正确。
答案:C
2.解析:升高温度有利于 Al3+水解,溶液的酸性增强,c(H+)增大。
答案:C
3.解析:结合原子序数和简单离子的电荷数,确定 W、X、Y、Z 分别为 O、Na、Al、
S 四种元素,能发生水解的离子为 Al3+、S2-,故 C 项正确。
答案:C
4.解析:多元弱酸根离子水解是分步进行的,是可逆反应,水解的量较少不能生成沉
淀和气体。
答案:C
5.解析:NH +
4 水解的平衡常数不变,A 项不符合题意;NH4Cl 水解呈酸性,加水稀释,
水解程度增大,但酸性减弱,溶液的 pH 将增大,溶液中 NH +
4 数将减小,c(NH+
4 )也减小,
故 C、D 两项均不符合题意。
答案:B
6.解析:a>b 时,溶液可能呈酸性、中性或碱性,c(NH+
4 )可能小于、等于或大于 c(Cl
-),B 不正确;当 a=b 时,氨水和 HCl 恰好完全反应生成 NH4Cl,因水解该溶液呈酸性,C
不正确;只有 a=b 时,混合液中 c(Cl-)=c(NH+
4 )+c(NH3·H2O)才成立,D 不正确。
答案:A
7.解析:由于 CH3COONa 的 pH 小于 NaClO 的 pH,说明 ClO-的水解程度大,等浓度
的 CH3COOH 和 HClO,HClO 的酸性弱,pH 大,A 项错误;碳酸根离子分两步水解:CO2-
3
+H2O HCO-
3 +OH-、HCO-
3 +H2O H2CO3+OH-,碳酸氢根离子既电离又水解:
HCO-
3 H++CO2-
3 、HCO-
3 +H2O H2CO3+OH-,Na2CO3 和 NaHCO3 溶液中离子种类
相同,B 项错误;盐中弱离子的水解程度越大,水的电离程度越大,①<②<④<③,C 项错
误;NaHCO3 溶液中,根据物料守恒,c(Na+)=c(CO2-
3 )+c(HCO-
3 )+c(H2CO3),D 项正确。
答案:D
8.解析:由电荷守恒:c(CH3COO-)+c(OH-)=c(Na+)+c(H+),因 c(CH3COO-)>c(Na
+),则 c(H+)>c(OH-);由物料守恒:c(CH3COOH)+c(CH3COO-)=0.2 mol·L-1,因 c(CH3COO
-)>c(Na+)=0.1 mol·L-1,则 c(CH3COO-)>c(CH3COOH)。
答案:A
9.解析:A 项,根据图像可知三种酸(HA、HB 和 HD)溶液的起始 pH 值 HA 最小,酸
性最强,HD 的 pH 最大,酸性最弱,酸性越强,酸根离子的浓度越大,正确;B 项,滴定
至 P 点时溶质为等物质的量浓度的 HB 和 NaB,溶液显酸性,电离大于水解,因此 c(B-)>
c(HB),正确;C 项,pH=7 时,三种溶液中阴离子的水解程度不同,D-水解程度最大,则
三种溶液中:c(A-)>c(B-)>c(D-),正确;D 项,混合溶液的质子守恒关系式,c(HA)+c(HB)
+c(HD)=c(OH-)-c(H+),错误。
答案:D
10.解析:A 项,NaHSO3 溶液显酸性,c(H+)>c(OH-);B 项,Na2SO3 溶液中,c(Na
+)>c(SO2-
3 )>c(OH-)>c(HSO-
3 )>c(H+);C 项, c SO2-
3
c HSO-
3
=1:1 时,溶液略显碱性,若使溶
液显中性,则 c(SO2-
3 )c(Cl-)>c(HCO-
3 )>c(H+)=c(OH-) ③10