- 2021-05-26 发布 |
- 37.5 KB |
- 21页
申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019-2020学年安徽省合肥市包河区九年级(上)期末化学试卷
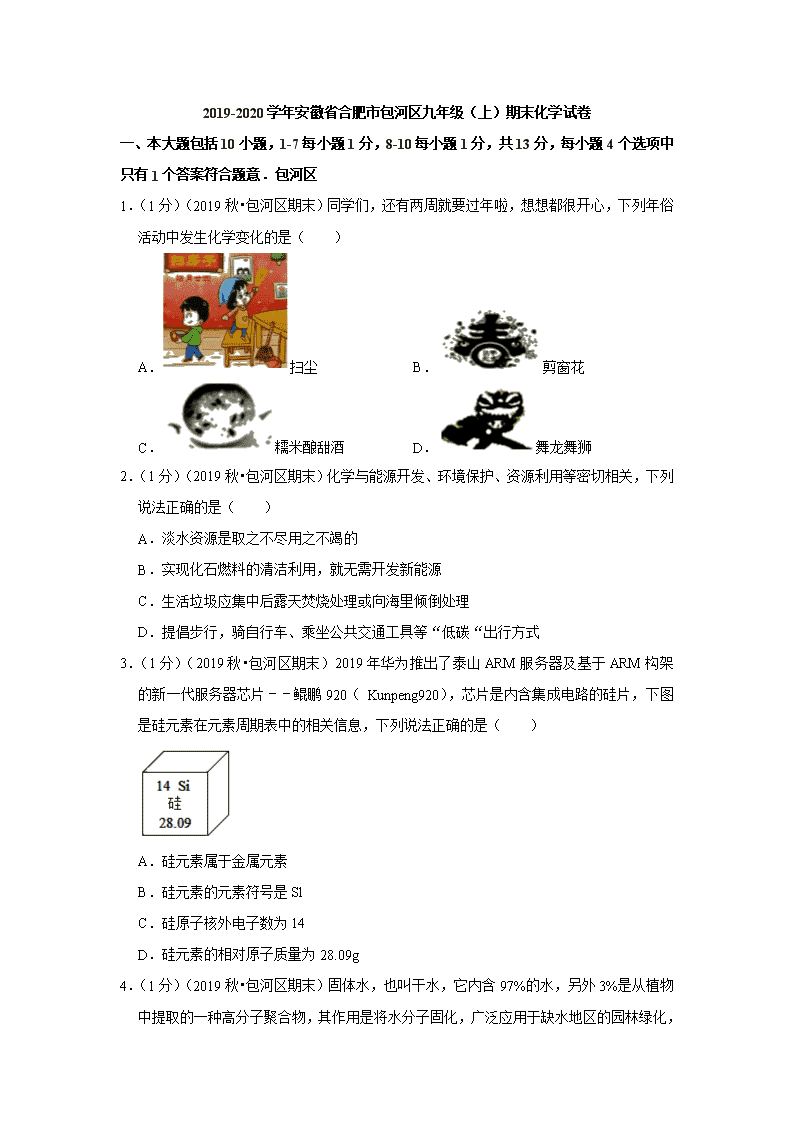
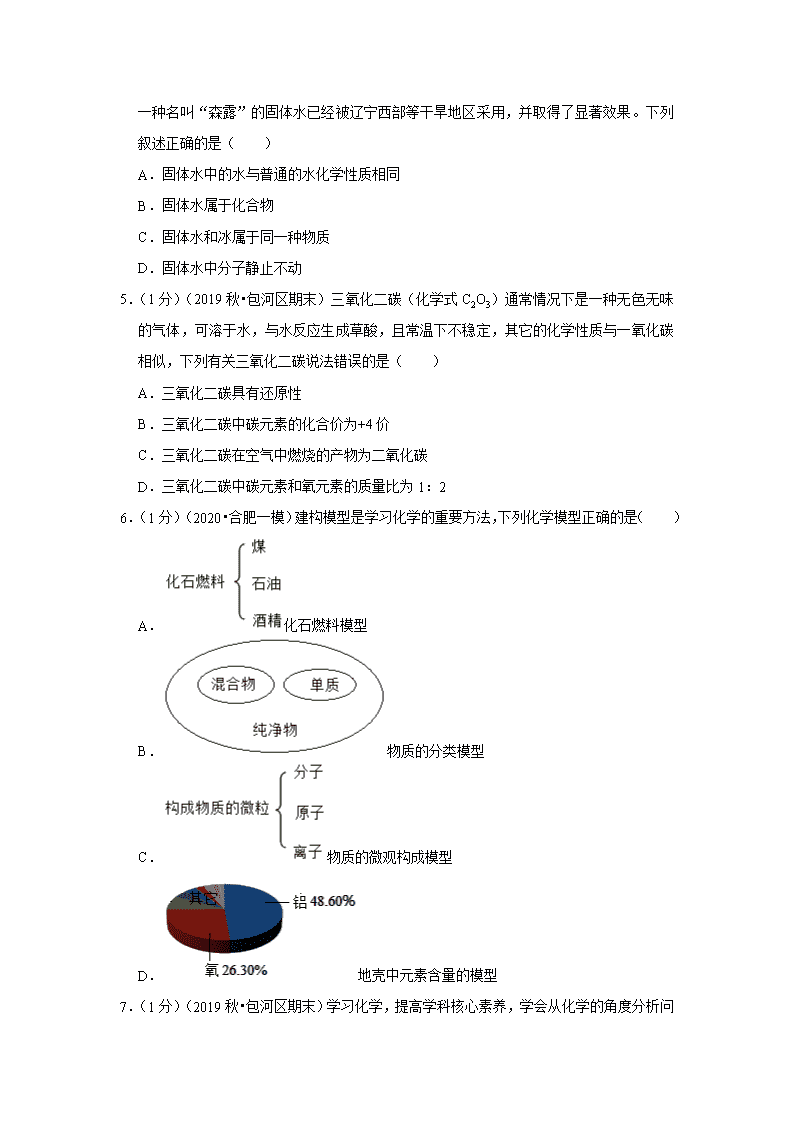
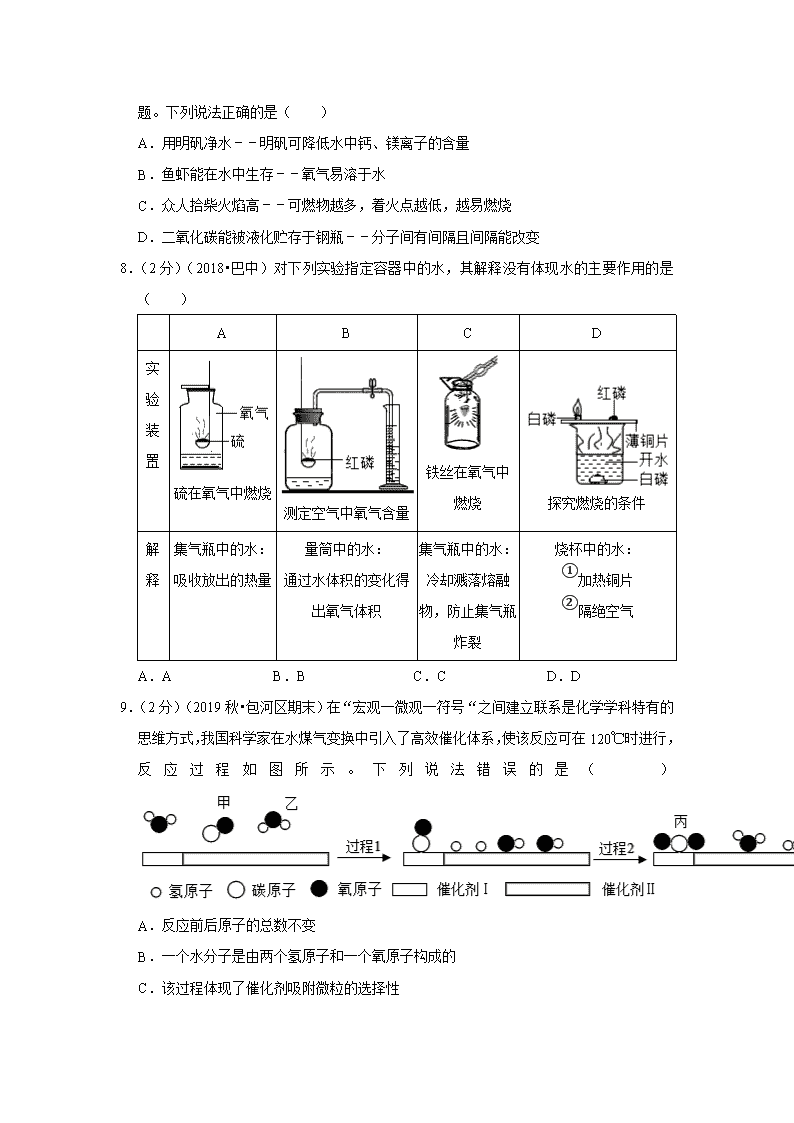
2019-2020 学年安徽省合肥市包河区九年级(上)期末化学试卷 一、本大题包括 10 小题,1-7 每小题 1 分,8-10 每小题 1 分,共 13 分,每小题 4 个选项中 只有 1 个答案符合题意.包河区 1.(1 分)(2019 秋•包河区期末)同学们,还有两周就要过年啦,想想都很开心,下列年俗 活动中发生化学变化的是( ) A. 扫尘 B. 剪窗花 C. 糯米酿甜酒 D. 舞龙舞狮 2.(1 分)(2019 秋•包河区期末)化学与能源开发、环境保护、资源利用等密切相关,下列 说法正确的是( ) A.淡水资源是取之不尽用之不竭的 B.实现化石燃料的清洁利用,就无需开发新能源 C.生活垃圾应集中后露天焚烧处理或向海里倾倒处理 D.提倡步行,骑自行车、乘坐公共交通工具等“低碳“出行方式 3.(1 分)(2019 秋•包河区期末)2019 年华为推出了泰山 ARM 服务器及基于 ARM 构架的 新一代服务器芯片﹣﹣鲲鹏 920( Kunpeng920),芯片是内含集成电路的硅片,下图是 硅元素在元素周期表中的相关信息,下列说法正确的是( ) A.硅元素属于金属元素 B.硅元素的元素符号是 Sl C.硅原子核外电子数为 14 D.硅元素的相对原子质量为 28.09g 4.(1 分)(2019 秋•包河区期末)固体水,也叫干水,它内含 97%的水,另外 3%是从植物 中提取的一种高分子聚合物,其作用是将水分子固化,广泛应用于缺水地区的园林绿化, 一种名叫“森露”的固体水已经被辽宁西部等干旱地区采用,并取得了显著效果。下列 叙述正确的是( ) A.固体水中的水与普通的水化学性质相同 B.固体水属于化合物 C.固体水和冰属于同一种物质 D.固体水中分子静止不动 5.(1 分)(2019 秋•包河区期末)三氧化二碳(化学式 C2O3)通常情况下是一种无色无味 的气体,可溶于水,与水反应生成草酸,且常温下不稳定,其它的化学性质与一氧化碳 相似,下列有关三氧化二碳说法错误的是( ) A.三氧化二碳具有还原性 B.三氧化二碳中碳元素的化合价为+4 价 C.三氧化二碳在空气中燃烧的产物为二氧化碳 D.三氧化二碳中碳元素和氧元素的质量比为 1:2 6.(1 分)(2020•合肥一模)建构模型是学习化学的重要方法,下列化学模型正确的是( ) A. 化石燃料模型 B. 物质的分类模型 C. 物质的微观构成模型 D. 地壳中元素含量的模型 7.(1 分)(2019 秋•包河区期末)学习化学,提高学科核心素养,学会从化学的角度分析问 题。下列说法正确的是( ) A.用明矾净水﹣﹣明矾可降低水中钙、镁离子的含量 B.鱼虾能在水中生存﹣﹣氧气易溶于水 C.众人拾柴火焰高﹣﹣可燃物越多,着火点越低,越易燃烧 D.二氧化碳能被液化贮存于钢瓶﹣﹣分子间有间隔且间隔能改变 8.(2 分)(2018•巴中)对下列实验指定容器中的水,其解释没有体现水的主要作用的是 ( ) A B C D 实 验 装 置 硫在氧气中燃烧 测定空气中氧气含量 铁丝在氧气中 燃烧 探究燃烧的条件 解 释 集气瓶中的水: 吸收放出的热量 量筒中的水: 通过水体积的变化得 出氧气体积 集气瓶中的水: 冷却溅落熔融 物,防止集气瓶 炸裂 烧杯中的水: ① 加热铜片 ② 隔绝空气 A.A B.B C.C D.D 9.(2 分)(2019 秋•包河区期末)在“宏观一微观一符号“之间建立联系是化学学科特有的 思维方式,我国科学家在水煤气变换中引入了高效催化体系,使该反应可在 120℃时进行, 反 应 过 程 如 图 所 示 。 下 列 说 法 错 误 的 是 ( ) A.反应前后原子的总数不变 B.一个水分子是由两个氢原子和一个氧原子构成的 C.该过程体现了催化剂吸附微粒的选择性 D.反应每消耗 14g 甲,可生成 22g 丙 10.(2 分)(2020•合肥一模)按表进行试验,在等质量的大理石中加入足量的酸(假设杂 质不与酸反应),用数字检测仪分别测得产生的二氧化碳体积随时间的变化曲线如图所 示,根据图示,下列说法正确的是( ) 实验编号 药品 Ⅰ 块状大理石、10%的稀硫酸溶液 Ⅱ 块状大理石、7%的稀盐酸溶液 Ⅲ 粉未状大理石,7%的稀盐酸溶液 A.曲线甲代表的是实验Ⅰ B.实验室可用块状大理石和 10%的稀硫酸溶液反应制取二氧化碳 C.实验室可用粉末状大理石和 7%的稀盐酸溶液反应制取二氧化碳 D.据图分析,在其他条件相同时,固体的颗粒越小,反应速率越快 二、本大题包括 4 小题,共 23 分.(除标注外,每空 1 分,) 11.(4 分)(2019 秋•包河区期末)自 2018 年 1 月 1 日起,合肥市区禁止燃放烟花爆竹,开 启了霸都环保新时代。 (1)“禁止燃放烟花爆竹“的安全标志是 。 (2)烟花爆竹的主要成分是黑火药,其化学组成为硝酸钾(KNO3)硫磺和木炭等。黑 火药中至少有 种元素,燃放烟花爆竹时产生有刺激性气味的二氧化硫的化学方程 式是 ,故禁止燃放烟花爆竹不仅可以减少噪声污染、火灾等,还可以减少二氧化 硫和可吸入颗粒物等空气污染物的排放,提升空气质量。 (3)燃放烟花爆竹时还有可能引起火灾,“火立熄”是一种新型的家用灭火用品,“火立 熄接触到火焰 3﹣5 秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使 火焰熄灭。“火立熄”的灭火原理是 。 A.清除可燃物 B.使可燃物与空气隔绝 C.降低可燃物的着火点 12.(6 分)(2019 秋•包河区期末)如图是实验室中常见装置,回答下列问题。 (1)写出指定仪器的名称:a 。 (2)用装置 A 进行实验时,首先应 (填序号)。 ① 加药品 ② 加热 ③ 检查装置气密性 (3)小雨同学用 A 装置制取氧气,发生反应的化学方程式为 ,若选用装置 F 收 集氧气,气体应该从 端(选填“b”或“c”)通入。 (4)小明同学用 B 装置制取二氧化碳,并测量生成的二氧化碳体积,应选用的收集装置 是 (填字母序号),实验室检验二氧化碳的化学方程式为 。 13.(6 分)(2019 秋•包河区期末)空气是一种宝贵的自然资源,如图是以空气等为原料合 成尿素【CO(NH2)2】的流程。请按要求回答下列问题: (1)图中分离空气的过程属于 变化(填“物理”或“化学”)。 (2)天然气的主要成分是 CH4,天然气属于 再生资源(填“可”或“不可”), 点燃 CH4 之前应 。 (3)因为二氧化碳具有 的性质,常用于灭火。 (4)写出图中“X”与氢气反应的化学方程式 。 14.(7 分)(2019 秋•包河区期末)常温下,H2O2 分解生成 O2 的速率较为缓慢,研究性学 习小组选择“H2O2 分解生成 O2 的快慢与什么因素有关”的课题进行探究,以下是他们探 究的主要过程: 【提出假设】催化剂的种类会影响 H2O2 分解生成 O2 的快慢。 【供选择的试剂】5%H2O2 溶液、15%H2O2 溶液、30%H2O2 溶液、二氧化锰粉末、二氧 化锰、氧化铜粉末 【设计方案】常温下,取两份 5%H2O2 溶液各 100mL,分别加入 ,测量各生成一 瓶相同体积的 O2 所需的时间。 【实验探究】如图 1 是他们进行实验的装置图,此实验中 A 处宜采用的气体收集方法 是 。检查装置气密性良好,将分液漏斗中的液体加入锥形瓶中,立即收集一瓶气 体。 【实验记录】 实验编号 ① ②反应物 5%H2O2 溶液 100mL 5%H2O2 溶液 100mL 加入固体 CuO MnO2 收集一瓶气体所需时间 165s 46s 【实验分析】(1)若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证它们在化 学反应前后的 和 没有改变。 (2)要定量地比较化学反应速度的快慢,除了上述方法外,还可以 。 【得出结论】该探究过程得出的结论是 ,故实验室用 H2O2 溶液制取氧气的化学 方程式为 。 注意:若答对以下小题奖励 4 分,化学试卷总分不超过 40 分。 【反思】还有哪些因素可能影响该反应的速率呢? (1)在老师的帮助下,小组同学们使用压强传感器等设备,探究在其他条件相同时,不 同温度下过氧化氢溶液分解时密闭容器内压强的变化,经过实验、数据处理等,获得如 图 2 所示的压强时间的曲线变化图。由此得出的结论是 。 (2)你还有其他的猜想吗? 猜想 。 请选择题目中提供的试剂,设计实验证明你的猜想(包括实验方案和结论) 。 三、本大题共 4 分 15.(4 分)(2019 秋•包河区期末)碳酸氢钠(NaHCO3)俗称小苏打,是焙制糕点所用的 发醇粉的主要成分之一,在 270℃时分解:2NaHCO3 Na2CO3+H2O+CO2↑,现称 取碳酸氢钠固体 16.8g,在敞口容器中加热到质量不再改变,请计算生成碳酸钠的质量。 (计算结果请保留一位小数) 2019-2020 学年安徽省合肥市包河区九年级(上)期末化学试卷 参考答案与试题解析 一、本大题包括 10 小题,1-7 每小题 1 分,8-10 每小题 1 分,共 13 分,每小题 4 个选项中 只有 1 个答案符合题意.包河区 1.(1 分)(2019 秋•包河区期末)同学们,还有两周就要过年啦,想想都很开心,下列年俗 活动中发生化学变化的是( ) A. 扫尘 B. 剪窗花 C. 糯米酿甜酒 D. 舞龙舞狮 【解答】解:A、扫尘没有新物质生成,属于物理变化;故选项错误; B、剪窗花没有新物质生成,属于物理变化;故选项错误; C、糯米酿甜酒,酒精是新物质,属于化学变化;故选项正确; D、舞龙舞狮没有新物质生成,属于物理变化;故选项错误; 故选:C。 2.(1 分)(2019 秋•包河区期末)化学与能源开发、环境保护、资源利用等密切相关,下列 说法正确的是( ) A.淡水资源是取之不尽用之不竭的 B.实现化石燃料的清洁利用,就无需开发新能源 C.生活垃圾应集中后露天焚烧处理或向海里倾倒处理 D.提倡步行,骑自行车、乘坐公共交通工具等“低碳“出行方式 【解答】解:A、淡水资源是取之不尽用之不竭的错误,故选项错误; B、实现化石燃料的清洁利用,就无需开发新能源错误,故选项错误; C、生活垃圾应集中后露天焚烧处理或向海里倾倒处理,会污染空气和水源;故选项错误; D、提倡步行,骑自行车、乘坐公共交通工具等“低碳“出行方式正确,可以保护环境; 故选项正确; 故选:D。 3.(1 分)(2019 秋•包河区期末)2019 年华为推出了泰山 ARM 服务器及基于 ARM 构架的 新一代服务器芯片﹣﹣鲲鹏 920( Kunpeng920),芯片是内含集成电路的硅片,下图是 硅元素在元素周期表中的相关信息,下列说法正确的是( ) A.硅元素属于金属元素 B.硅元素的元素符号是 Sl C.硅原子核外电子数为 14 D.硅元素的相对原子质量为 28.09g 【解答】解:A、根据元素周期表中的一格可知,中间的汉字表示元素名称,该元素的名 称是硅,带“石”字旁,属于固态非金属元素,故选项说法错误。 B、根据元素周期表中的一格可知,字母表示该元素的元素符号,硅元素的元素符号是 Si,故选项说法错误。 C、根据元素周期表中的一格可知,左上角的数字为 14,表示原子序数为 14;根据原子 中原子序数=核电荷数=质子数=核外电子数,则硅元素的原子核外电子数为 14,故选 项说法正确。 D、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,该元素的相对原 子质量为硅元素的相对原子质量为 28.09,相对原子质量单位是“1”,不是“克”,故选 项说法错误。 故选:C。 4.(1 分)(2019 秋•包河区期末)固体水,也叫干水,它内含 97%的水,另外 3%是从植物 中提取的一种高分子聚合物,其作用是将水分子固化,广泛应用于缺水地区的园林绿化, 一种名叫“森露”的固体水已经被辽宁西部等干旱地区采用,并取得了显著效果。下列 叙述正确的是( ) A.固体水中的水与普通的水化学性质相同 B.固体水属于化合物 C.固体水和冰属于同一种物质 D.固体水中分子静止不动 【解答】解:A.固体水中的水也是由水分子构成,所以固体水中水的化学性质与普通水 相同,故正确; B.固体水含 97%的水,另外 3%是高分子聚合物,是混合物;故错误; C.固体水含 97%的水,另外 3%是高分子聚合物,而冰是固态的水,二者不是同一种物 质,故错误; D.水分子不断运动,故错误; 故选:A。 5.(1 分)(2019 秋•包河区期末)三氧化二碳(化学式 C2O3)通常情况下是一种无色无味 的气体,可溶于水,与水反应生成草酸,且常温下不稳定,其它的化学性质与一氧化碳 相似,下列有关三氧化二碳说法错误的是( ) A.三氧化二碳具有还原性 B.三氧化二碳中碳元素的化合价为+4 价 C.三氧化二碳在空气中燃烧的产物为二氧化碳 D.三氧化二碳中碳元素和氧元素的质量比为 1:2 【解答】解:A、由于 CO 具有还原性,而三氧化二碳化学性质与一氧化碳相似,可判断 C2O3 具有还原性,故选项说法正确。 B、氧元素显﹣2 价,设碳元素的化合价是 x,根据在化合物中正负化合价代数和为零, 可得:2x+(﹣2)×3=0,则 x=+3 价,故选项说法错误。 C、由于 CO 具有可燃性,而三氧化二碳化学性质与一氧化碳相似,可判断 C2O3 具有可 燃性,充分燃烧的产物为 CO2,故选项说法正确。 D、三氧化二碳中碳元素和氧元素的质量比为(12×2):(16×3)=1:2,故选项说法正 确。 故选:B。 6.(1 分)(2020•合肥一模)建构模型是学习化学的重要方法,下列化学模型正确的是( ) A. 化石燃料模型 B. 物质的分类模型 C. 物质的微观构成模型 D. 地壳中元素含量的模型 【解答】解:A、三大化石燃料:煤、石油、天然气,故 A 错; B、纯净物分为单质和化合物,故 B 错; C、物质的构成微粒:分子、原子和离子,故 C 正确; D、地壳中含量最多的元素是氧元素,故 D 错。 故选:C。 7.(1 分)(2019 秋•包河区期末)学习化学,提高学科核心素养,学会从化学的角度分析问 题。下列说法正确的是( ) A.用明矾净水﹣﹣明矾可降低水中钙、镁离子的含量 B.鱼虾能在水中生存﹣﹣氧气易溶于水 C.众人拾柴火焰高﹣﹣可燃物越多,着火点越低,越易燃烧 D.二氧化碳能被液化贮存于钢瓶﹣﹣分子间有间隔且间隔能改变 【解答】解:A、明矾净水是除去水中的不溶性固体杂质,错误; B、氧气在水中是不易溶于水,错误; C、众人拾柴火焰高是增加可燃物的量,不是说着火点的问题,错误; D、二氧化碳能被液化贮存于钢瓶是因为分子间有间隔且间隔能改变,正确; 故选:D。 8.(2 分)(2018•巴中)对下列实验指定容器中的水,其解释没有体现水的主要作用的是 ( ) A B C D 实 验 装 置 硫在氧气中燃烧 测定空气中氧气含量 铁丝在氧气中 燃烧 探究燃烧的条件 解 释 集气瓶中的水: 吸收放出的热量 量筒中的水: 通过水体积的变化得 出氧气体积 集气瓶中的水: 冷却溅落熔融 物,防止集气瓶 炸裂 烧杯中的水: ① 加热铜片 ② 隔绝空气 A.A B.B C.C D.D 【解答】解:A、硫在氧气中燃烧生成的二氧化硫气体有毒,扩散到空气中会污染空气, 水能够吸收二氧化硫从而防止了二氧化硫向外扩散。水的主要作用是吸收二氧化硫。故 A 没有体现水的主要作用,故 A 正确; B、测定空气中氧气的体积分数时,通过量筒中水的体积变化可知氧气的体积。水的主要 作用是间接测定氧气的体积。因此该选项体现了水的主要作用,故 B 错; C、铁在氧气中燃烧时,水的用途是冷却溅落的四氧化三铁,防止炸裂集气瓶。因此该选 项没有体现了水的主要作用,故 C 错; D、探究燃烧条件实验中,热水的作用一是加热铜片,二是让白磷与空气隔绝。因此,该 选项体现了水的主要作用,故 D 错。 故选:A。 9.(2 分)(2019 秋•包河区期末)在“宏观一微观一符号“之间建立联系是化学学科特有的 思维方式,我国科学家在水煤气变换中引入了高效催化体系,使该反应可在 120℃时进行, 反 应 过 程 如 图 所 示 。 下 列 说 法 错 误 的 是 ( ) A.反应前后原子的总数不变 B.一个水分子是由两个氢原子和一个氧原子构成的 C.该过程体现了催化剂吸附微粒的选择性 D.反应每消耗 14g 甲,可生成 22g 丙 【解答】解:由反应的微观模型图可知,在高效催化体系使水煤气中的 CO 和 H2O 在 120℃ 下发生反应,反应方程式为:CO+H2O CO2+H2; A.由化学方程式可知,反应前后原子的总数不变,故正确; B.每个水分子是由两个氢原子和一个氧原子构成的,正确; C.由微粒的变化可知,该过程不能体现了催化剂吸附微粒的选择性,故错误; D.由方程式可知,甲与丙的质量比是 28:44,所以反应每消耗 14g 甲,可生成 22g 丙, 故正确; 故选:C。 10.(2 分)(2020•合肥一模)按表进行试验,在等质量的大理石中加入足量的酸(假设杂 质不与酸反应),用数字检测仪分别测得产生的二氧化碳体积随时间的变化曲线如图所 示,根据图示,下列说法正确的是( ) 实验编号 药品 Ⅰ 块状大理石、10%的稀硫酸溶液 Ⅱ 块状大理石、7%的稀盐酸溶液 Ⅲ 粉未状大理石,7%的稀盐酸溶液 A.曲线甲代表的是实验Ⅰ B.实验室可用块状大理石和 10%的稀硫酸溶液反应制取二氧化碳 C.实验室可用粉末状大理石和 7%的稀盐酸溶液反应制取二氧化碳 D.据图分析,在其他条件相同时,固体的颗粒越小,反应速率越快 【解答】解:A、大理石和稀硫酸反应生成硫酸钙微溶于水,覆盖在大理石表面阻止了反 应的进一步发生,图中甲对应实验Ⅰ,故 A 错误; B、大理石和稀硫酸反应生成硫酸钙微溶于水,覆盖在大理石表面阻止了反应的进一步发 生,所以实验室不能用块状大理石和 10%的稀硫酸溶液反应制取二氧化碳,故 B 错误; C、实验室可用粉末状大理石和 7%的稀盐酸溶液反应速率太快,不适合制取二氧化碳, 故 C 错误; D、据图分析,在其他条件相同时,固体的颗粒越小,反应速率越快,故 D 正确。 故选:D。 二、本大题包括 4 小题,共 23 分.(除标注外,每空 1 分,) 11.(4 分)(2019 秋•包河区期末)自 2018 年 1 月 1 日起,合肥市区禁止燃放烟花爆竹,开 启了霸都环保新时代。 (1)“禁止燃放烟花爆竹“的安全标志是 C 。 (2)烟花爆竹的主要成分是黑火药,其化学组成为硝酸钾(KNO3)硫磺和木炭等。黑 火药中至少有 5 种元素,燃放烟花爆竹时产生有刺激性气味的二氧化硫的化学方程式 是 S+O2 SO2 ,故禁止燃放烟花爆竹不仅可以减少噪声污染、火灾等,还可以 减少二氧化硫和可吸入颗粒物等空气污染物的排放,提升空气质量。 (3)燃放烟花爆竹时还有可能引起火灾,“火立熄”是一种新型的家用灭火用品,“火立 熄接触到火焰 3﹣5 秒后炸开,释放的粉末覆盖在燃烧物上,同时放出不可燃烧气体,使 火焰熄灭。“火立熄”的灭火原理是 B 。 A.清除可燃物 B.使可燃物与空气隔绝 C.降低可燃物的着火点 【解答】解:(1)据图可以看出,“禁止燃放烟花爆竹“的安全标志是 C,故填:C。 (2)黑火药的化学组成为硝酸钾(KNO3)硫磺和木炭,则黑火药中至少有钾、氮、氧、 硫、碳 5 种元素,燃放烟花爆竹时产生有刺激性气味的二氧化硫的化学方程式是 S+O2 SO2,故填:5;S+O2 SO2。 (3)“火立熄”的灭火原理是使可燃物与空气隔绝,故填:B。 12.(6 分)(2019 秋•包河区期末)如图是实验室中常见装置,回答下列问题。 (1)写出指定仪器的名称:a 锥形瓶 。 (2)用装置 A 进行实验时,首先应 ③ (填序号)。 ① 加药品 ② 加热 ③ 检查装置气密性 ( 3 ) 小 雨 同 学 用 A 装 置 制 取 氧 气 , 发 生 反 应 的 化 学 方 程 式 为 2KMnO4 K2MnO4+MnO2+O2↑ ,若选用装置 F 收集氧气,气体应该从 b 端 (选填“b”或“c”)通入。 (4)小明同学用 B 装置制取二氧化碳,并测量生成的二氧化碳体积,应选用的收集装置 是 H (填字母序号),实验室检验二氧化碳的化学方程式为 CO2+Ca(OH)2=CaCO3 ↓+H2O 。 【解答】解:(1)锥形瓶是常用的反应容器,故答案为:锥形瓶; (2)用装置 A 进行实验时,首先应检查装置的气密性;故答案为: ③ ; (3)A 装置的试管中有棉花团,因此是用高锰酸钾制氧气,高锰酸钾受热分解生成锰酸 钾和二氧化锰和氧气,要注意配平;若选用装置 F 收集氧气,气体应该从长管进入,因 为氧气的密度比空气大;故答案为:2KMnO4 K2MnO4+MnO2+O2↑:b; (4)小明同学用 B 装置制取二氧化碳,并测量生成的二氧化碳体积,应选用的收集装置 是 H;二氧化碳一般用澄清的石灰水检验:把气体通入澄清的石灰水中,石灰水变浑浊, 就证明是二氧化碳;故答案为:H;CO2+Ca(OH)2=CaCO3↓+H2O; 13.(6 分)(2019 秋•包河区期末)空气是一种宝贵的自然资源,如图是以空气等为原料合 成尿素【CO(NH2)2】的流程。请按要求回答下列问题: (1)图中分离空气的过程属于 物理 变化(填“物理”或“化学”)。 (2)天然气的主要成分是 CH4,天然气属于 不可 再生资源(填“可”或“不可”), 点燃 CH4 之前应 验纯 。 (3)因为二氧化碳具有 不燃烧不支持燃烧,密度比空气大 的性质,常用于灭火。 (4)写出图中“X”与氢气反应的化学方程式 N2+3H2 2NH3 。 【解答】解:(1)图中分离空气的过程没有新物质生成,属于物理变化。 (2)天然气的主要成分是 CH4,天然气属于化石燃料,属于不可再生资源,CH4 是可燃 性的气体,点燃 CH4 之前应验纯。 (3)因为二氧化碳具有不燃烧不支持燃烧,密度比空气大的性质,常用于灭火。 (4)由质量守恒定律可知,图中“X”是氮气,与氢气反应的化学方程式是: N2+3H2 2NH3。 故答案为:(1)物理。(2)不可;验纯。(3)密度比空气大,通常不燃烧也不支持燃烧。 (4)N2+3H2 2NH3。 14.(7 分)(2019 秋•包河区期末)常温下,H2O2 分解生成 O2 的速率较为缓慢,研究性学 习小组选择“H2O2 分解生成 O2 的快慢与什么因素有关”的课题进行探究,以下是他们探 究的主要过程: 【提出假设】催化剂的种类会影响 H2O2 分解生成 O2 的快慢。 【供选择的试剂】5%H2O2 溶液、15%H2O2 溶液、30%H2O2 溶液、二氧化锰粉末、二氧 化锰、氧化铜粉末 【设计方案】常温下,取两份 5%H2O2 溶液各 100mL,分别加入 相同质量的二氧化锰 粉末和氧化铜粉末 ,测量各生成一瓶相同体积的 O2 所需的时间。 【实验探究】如图 1 是他们进行实验的装置图,此实验中 A 处宜采用的气体收集方法是 排水法 。检查装置气密性良好,将分液漏斗中的液体加入锥形瓶中,立即收集一瓶气 体。 【实验记录】 实验编号 ① ②反应物 5%H2O2 溶液 100mL 5%H2O2 溶液 100mL 加入固体 CuO MnO2 收集一瓶气体所需时间 165s 46s 【实验分析】(1)若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证它们在化 学反应前后的 质量 和 化学性质 没有改变。 (2)要定量地比较化学反应速度的快慢,除了上述方法外,还可以 测量相同时间收集 到的氧气体积 。 【得出结论】该探究过程得出的结论是 在其他条件相同时,二氧化锰对该反应的催化 效 果 比 氧 化 铜 好 , 故 实 验 室 用 H2O2 溶 液 制 取 氧 气 的 化 学 方 程 式 为 2H2O2 2H2O+O2↑ 。 注意:若答对以下小题奖励 4 分,化学试卷总分不超过 40 分。 【反思】还有哪些因素可能影响该反应的速率呢? (1)在老师的帮助下,小组同学们使用压强传感器等设备,探究在其他条件相同时,不 同温度下过氧化氢溶液分解时密闭容器内压强的变化,经过实验、数据处理等,获得如 图 2 所示的压强时间的曲线变化图。由此得出的结论是 在其他条件相同时,温度越高 过氧化氢分解速率越快 。 (2)你还有其他的猜想吗? 猜想 过氧化氢溶液的浓度影响反应速率 。 请选择题目中提供的试剂,设计实验证明你的猜想(包括实验方案和结论) 实验步骤: 常温下,取两份等质量的二氧化锰粉末分别放入锥形瓶中,再分别量取 100mL5%和 15% 的过氧化氢溶液加入锥形瓶中,测量各生成一瓶相同体积的 O2 所需的时间; 实验现象:15%的过氧化氢溶液需要时间短; 实验结论:在其他条件相同时,过氧化氢溶液浓度越大,反应速率越快 。 【解答】解:【设计方案】 常温下,取两份 5%H2O2 溶液各 100mL,分别加入相同质量的二氧化锰粉末和氧化铜粉 末,测量各生成一瓶相同体积的 O2 所需的时间。 故填:相同质量的二氧化锰粉末和氧化铜粉末。 【实验探究】 如图 1 是他们进行实验的装置图,此实验中 A 处宜采用的气体收集方法是排水法。 故填:排水法。 【实验分析】 (1)若要证明二氧化锰、氧化铜是该反应的催化剂,还需要验证它们在化学反应前后的 质量和化学性质没有改变。 故填:质量;化学性质。 (2)要定量地比较化学反应速度的快慢,除了上述方法外,还可以测量相同时间收集到 的氧气体积,即相同时间内收集的氧气越多,反应速率越快。 故填:测量相同时间收集到的氧气体积。 【得出结论】 该探究过程中,收集相同体积的氧气,利用二氧化锰比利用氧化铜需要时间短,得出的 结论是在其他条件相同时,二氧化锰对该反应的催化效果比氧化铜好,故实验室用 H2O2 溶液制取氧气的化学方程式为:2H2O2 2H2O+O2↑。 故 填 : 在 其 他 条 件 相 同 时 , 二 氧 化 锰 对 该 反 应 的 催 化 效 果 比 氧 化 铜 好 ; 2H2O2 2H2O+O2↑。 【反思】 (1)如图 2 所示的压强时间的曲线变化图可知,温度越高,气体压强越大,由此得出的 结论是在其他条件相同时,温度越高过氧化氢分解速率越快。 故填:在其他条件相同时,温度越高过氧化氢分解速率越快。 (2)其他的猜想:过氧化氢溶液的浓度影响反应速率; 实验方案:实验步骤:常温下,取两份等质量的二氧化锰粉末分别放入锥形瓶中,再分 别量取 100mL5%和 15%的过氧化氢溶液加入锥形瓶中,测量各生成一瓶相同体积的 O2 所需的时间; 实验现象:15%的过氧化氢溶液需要时间短; 实验结论:在其他条件相同时,过氧化氢溶液浓度越大,反应速率越快。 故填:过氧化氢溶液的浓度影响反应速率;实验步骤:常温下,取两份等质量的二氧化 锰粉末分别放入锥形瓶中,再分别量取 100mL5%和 15%的过氧化氢溶液加入锥形瓶中, 测量各生成一瓶相同体积的 O2 所需的时间; 实验现象:15%的过氧化氢溶液需要时间短; 实验结论:在其他条件相同时,过氧化氢溶液浓度越大,反应速率越快。 三、本大题共 4 分 15.(4 分)(2019 秋•包河区期末)碳酸氢钠(NaHCO3)俗称小苏打,是焙制糕点所用的 发醇粉的主要成分之一,在 270℃时分解:2NaHCO3 Na2CO3+H2O+CO2↑,现称 取碳酸氢钠固体 16.8g,在敞口容器中加热到质量不再改变,请计算生成碳酸钠的质量。 (计算结果请保留一位小数) 【解答】解:设生成的碳酸钠的质量为 x 2NaHCO3+ Na2CO3+H2O+CO2↑ 168 106 16.8g x x=10.6g 答:生成碳酸钠的质量为 10.6g。查看更多