- 2021-05-24 发布 |
- 37.5 KB |
- 13页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
高考专题复习实验装置
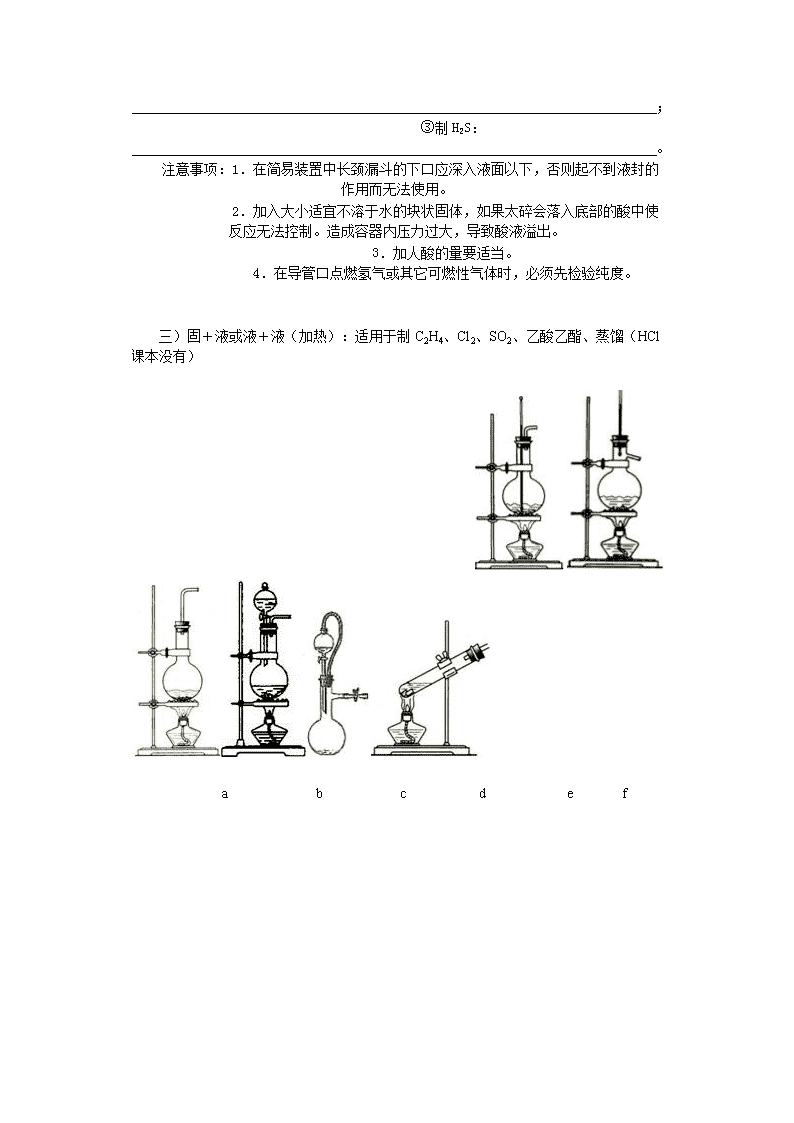
高考专题复习——气体的制备装置 ---试验装置分解 华油三中 杨亚平 高中化学中气体制备装置一般分四大部分:发生装置,净化装置(干燥装置),收集装置,尾气处理装置。 一、气体的发生装置 一)固+固(加热):适用于制O2、NH3、(CH4课本没有)。 制备原理:①制氧气: ; ②制氨气: ; ③制甲烷: 。 注意事项: l.试管口应稍向下倾斜,以防止产生的水蒸气在管口冷 却后倒流而引起试管破裂。 2.铁夹应夹在距管口l/3处。 3.固体药品要放在试管底部平铺开,加热时首先均匀预热,然后在试管的最后部位集中加热,并逐步前移。 4.胶塞上的导管伸入试管里不能过长,否则会妨碍气体导出。 5.如用排气法收集气体,当停止制气时,应先从水槽中把导管撤出,然后再撤走酒精灯。以防止水倒流。 二)固+液体(不加热):适用于制CO2、C2H2、H2 、H2S(SO2、NO2、NO课本没有制法)。 (一)常规类 制备原理:①制CO2: ; ②制C2H2: ; ③制H2: ; ④制SO2、NO2、H2S、NO: 。 注意事项:1.瓶内气密性要好。 2.先放固体后加液体。(为什么?) 3.加入酸的量要适当。 4.生成气体微溶或难溶于水。 (二)启普发生器类 制备原理: ①制CO2: ; ②制H2: ; ③制H2S: 。 注意事项:1.在简易装置中长颈漏斗的下口应深入液面以下,否则起不到液封的作用而无法使用。 2.加入大小适宜不溶于水的块状固体,如果太碎会落入底部的酸中使反应无法控制。造成容器内压力过大,导致酸液溢出。 3.加人酸的量要适当。 4.在导管口点燃氢气或其它可燃性气体时,必须先检验纯度。 三)固+液或液+液(加热):适用于制C2H4、Cl2、SO2、乙酸乙酯、蒸馏(HCl课本没有) a b c d e f 注意点: 1、用KMnO4制取O2时,为了防止生成的细小颗粒堵塞导管,在大试管口放一松软棉花。 2、实验室制取氨气时,由于氨气极易与空气中的水结合,导致外部空气向试管里“冲”,里面氨气向外逸出,在小试管口放一疏松棉花。 3、在制取C2H2时,若用大试管为反应器时,在大试管口放一松软棉花,防止生成的泡沫喷出。 4、Cu和浓硫酸制取SO2做性质试验的小试管口堵一块蘸有少量碱液的棉花防止污染。 二、气体的净化(干燥)装置 (一)常见净化原理:气体的净化可分为物理方法和化学方法。遵循以下原理: ①不损失主体气体;②不引入新杂质;③在密闭容器中进行;④先除易除的气体。 1.物理方法: (1)液化法:利用沸点不同从空气中分离N2和O2。 (2)水洗法:利用溶解度不同从N2和NH3中除去NH3;从NO和NO2中除去NO2。 △ 2.化学方法: (1)氧化还原法:灼热铜丝网除去混合物中的O2(2Cu+O2=2CuO);CuO除去H2、CO等。 (2)酸碱法:NH3和CO2通过碱石灰除去CO2。(CaO+CO2=CaCO3) (3)沉淀法:除去CO2中的H2S通过CuSO4溶液。H2S+CuSO4=CuS↓+H2SO4 (4)最常用的为洗气法: ①用饱和NaCl除去Cl2中的HCl; ②用饱和NaHCO3除去CO2中的HCl、SO2等; ③用酸性高锰酸钾除去气体中的SO2;(如CO2中的SO2) 注意:以下考得比较少: ④用饱和NaHSO3除去SO2中的SO3;[浓硫酸也可除SO3(SO3易溶于浓硫酸)];冷却同样可以除SO3。 ⑤用饱和Na2CO3溶液除去乙酸乙酯中的乙醇或乙酸; (二)常见净化装置 a b c d e a为加热固态试剂以除去气体中杂质的装置,为防止固体“流动”,两端用石棉或玻璃棉堵住,但要使气流通畅。b、c、d一般盛液体药品,用于洗液。e一般盛固体药品,往往根据增重可测出吸收物质的质量,用于定量计算。 (三)常见干燥剂及气体的干燥 液态干燥剂 固态干燥剂 装置 常见干燥剂 浓硫酸 无水氯化钙 碱石灰 可干燥气体 H2、O2、Cl2、SO2、CO2、CH4、N2、CO H2、O2、Cl2、SO2、CO2、CH4、N2、CO H2、O2、NH3、N2、CO、CH4 不可干燥气体 NH3、H2S、HBr、HI NH3 Cl2、H2S、HCl、SO2、CO2 三、气体的收集装置 根据气体溶解性(分子极性)和密度(相对分子量,与29比较)不同,把气体的收集方法分为排液法(常为排水法)和排气法(常为排空气法)。装置图见下: 1.排液法:难溶或微溶于水且不与水发生化学反应的气体。例如:H2、O2、CO、CH4、NO(只能用排液法收集)、CH2=CH2、CH≡CH等。注意:Cl2不用排水法收集,但可用排饱和食盐水收集,CO2可以用排饱和NaHCO3 收集。排液法的典型仪器是a,注意导管只能伸入集气瓶内少许。 2.排气法:不与空气反应且密度与空气相差较大的气体;又可分为向上排空气法和向下排空气法。用排气法收集气体时,导气管一定要伸入集气瓶底部,把空气尽量排出。为了减少空气扩散,集气瓶口可盖上毛玻璃片(如图b);试管口轻轻塞上一小团疏松的棉花(如图d) (1)向上排空气法:式量大于29的气体。如O2、CO2、SO2、H2S、Cl2、NO2(只用排空气)、HCl等;典型装置是b。 (2)向下排空气法:式量小于29的气体。如H2、CH4、NH3等;典型装置是c。 a b向上排空气法 c向下排空气法 d 练习:(发散思维) 1.下列装置也能用于收集气体,试根据气体的流向判断收集气体的种类。 2.排水法收集的气体和排气法收集的气体纯度有何不同? 3.某些气体要求非常干燥,则收集前后都要干燥,如何组装仪器? 四、尾气处理装置 通常有毒和有污染的尾气必须适当处理。常用经典仪器有: a b c d e a用于NaOH吸收氯气、CO2;硫酸铜吸收H2S(气体溶解或反应速度不很快,不易引起倒吸); b用于收集少量气体然后处理;c、d收集极易溶且溶解很快的气体。如HCl、HBr、NH3等;其中d 吸收量少。e用于处理难以吸收(有毒)且可燃的气体。如H2、CO等。 实验装置总装思路 1.装置的安装顺序 2.操作顺序 装置连接→气密性检查→装固体药品→加液体药品→气体制取 要点:气密性的检查 1.将装置的导管口一端浸没于水中,再用双手手掌握住容器(试管可用一只手握住,如左图;复杂仪器还可微热),若在导管口处有气泡冒出,松手后,水在导管里形成了一段水柱,则装置的气密性良好。 概括为:微热看气泡,静置看液面(又称整体法)。 2.如上图,关闭止水夹后,从长颈漏斗向试管中注入一定量的水,使漏斗内液面高于试管内液面,静置后若漏斗内液面不下降,则装置的气密性良好;液面下降,则装置的漏气; 概括为:注液静置看液面(又称局部法)。 创新设计方案集锦: 1.气体安全装置 1)防倒吸安全装置 2)防堵塞安全装置 3)防污染安全装置 2.液封装置 3.量气体体积装置(读数时,要使量筒与洗气瓶中的液面保持水平,消除水位差造成的误差) 4.启普发生器原理及类似反应器 经典套图 中和热测定 制乙烯 CO尾气吸收 海水蒸馏 制乙炔 CO尾气吸收查看更多