- 2021-05-13 发布 |
- 37.5 KB |
- 19页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
【化学】海南省嘉积中学2019-2020学年高二上学期第三次月考(解析版)
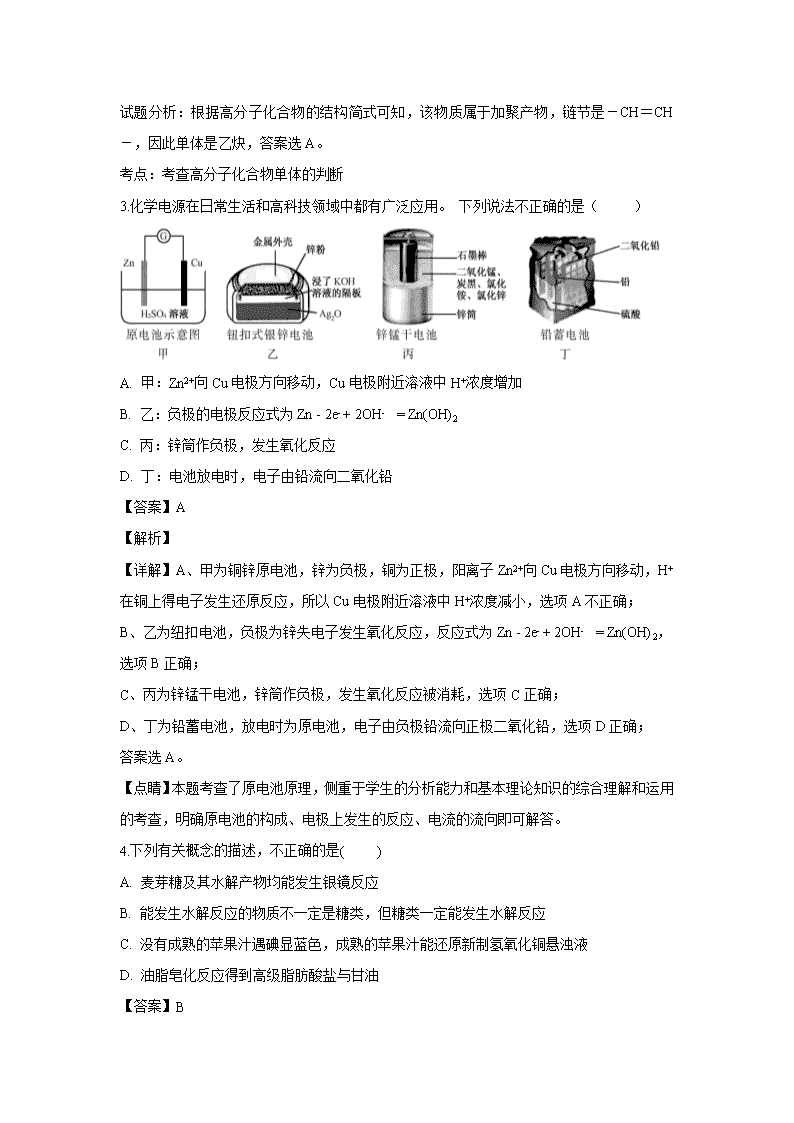
海南省嘉积中学2019-2020学年高二上学期第三次月考 可能用到的相对原子质量:H:1 C:12 N:14 O:16 Na:23 Mg:24 S:32 Cl:35.5 第I卷 一、单选题(每题2分,共8题 ,每小题只有一个正确的选项)。 1.下列说法正确的是( ) A. 己烷共有4种同分异构体,它们的熔点、沸点各不相同 B. 用溴水即可鉴别苯酚溶液、2,4-己二烯和甲苯 C. 有机物 的名称是2,3,5,5-四甲基-4-乙基己烷 D. 名称:2-乙基丙烷 【答案】B 【解析】 【详解】A、己烷共有5种同分异构体,支链越多,熔点、沸点越低,选项A错误; B、苯酚遇溴水出现白色沉淀,2,4-已二烯和溴水发生加成反应使溴水褪色,甲苯和溴水不反应,发生萃取原理,会分层,上层为橙红色;现象不同,可以用溴水即可鉴别苯酚溶液、2,4-已二烯和甲苯,选项B正确; C、命名遵循:长、多、近、简、小,有机物 名称为2,2,4,5-四甲基-3-乙基己烷,选项C错误; D、的名称为2-甲基丁烷,选项D错误; 答案选B。 2. 结构为…-CH=CH-CH=CH-CH=CH-CH=CH-…的高分子化合物用碘蒸气处理后,其导电能力大幅提高。上述高分子化合物的单体是 A. 乙炔 B. 乙烯 C. 丙烯 D. 1,3-丁二烯 【答案】A 【解析】 试题分析:根据高分子化合物的结构简式可知,该物质属于加聚产物,链节是-CH=CH-,因此单体是乙炔,答案选A。 考点:考查高分子化合物单体的判断 3.化学电源在日常生活和高科技领域中都有广泛应用。 下列说法不正确的是( ) A. 甲:Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度增加 B. 乙:负极的电极反应式为Zn - 2e- + 2OH- = Zn(OH)2 C. 丙:锌筒作负极,发生氧化反应 D. 丁:电池放电时,电子由铅流向二氧化铅 【答案】A 【解析】 【详解】A、甲为铜锌原电池,锌为负极,铜为正极,阳离子Zn2+向Cu电极方向移动,H+在铜上得电子发生还原反应,所以Cu电极附近溶液中H+浓度减小,选项A不正确; B、乙为纽扣电池,负极为锌失电子发生氧化反应,反应式为Zn - 2e- + 2OH- = Zn(OH)2,选项B正确; C、丙为锌锰干电池,锌筒作负极,发生氧化反应被消耗,选项C正确; D、丁为铅蓄电池,放电时为原电池,电子由负极铅流向正极二氧化铅,选项D正确; 答案选A。 【点睛】本题考查了原电池原理,侧重于学生的分析能力和基本理论知识的综合理解和运用的考查,明确原电池的构成、电极上发生的反应、电流的流向即可解答。 4.下列有关概念的描述,不正确的是( ) A. 麦芽糖及其水解产物均能发生银镜反应 B. 能发生水解反应的物质不一定是糖类,但糖类一定能发生水解反应 C. 没有成熟的苹果汁遇碘显蓝色,成熟的苹果汁能还原新制氢氧化铜悬浊液 D. 油脂皂化反应得到高级脂肪酸盐与甘油 【答案】B 【解析】 【详解】A、麦芽糖及其水解产物葡萄糖有醛基,能发生银镜反应,选项A正确; B、单糖不能发生水解,如葡萄糖,选项B不正确; C、没有成熟的苹果汁含有淀粉,成熟的含有葡萄糖,淀粉遇碘单质变蓝色,葡萄糖能还原新制氢氧化铜悬浊液,选项C正确; D、油脂水解生成高级脂肪酸和甘油,碱性条件下,高级脂肪酸和碱反应生成高级脂肪酸盐和水,即油脂在碱性条件下水解生成甘油和高级脂肪酸盐,该反应为皂化反应,选项D正确; 答案选B。 5.用0.55 mol·L-1 NaOH溶液分别与0.5 mol·L-1的盐酸、醋酸溶液反应,且所取的溶液体积均相等,测出的中和热数值分别为ΔH1和ΔH2,则ΔH1和ΔH2两者的关系正确的是( ) A. ΔH1>ΔH2 B. ΔH1=ΔH2 C. ΔH1<ΔH2 D. 无法比较 【答案】C 【解析】 【详解】因为盐酸是强酸完全电离,而醋酸是弱酸,在反应过程中醋酸电离要吸收热量,所以醋酸与氢氧化钠溶液反应时放出的热量少,盐酸与氢氧化钠反应放出的热量多,中和热数值分别为ΔH1和ΔH2,而ΔH1和ΔH2是用负值表示,因此ΔH1<ΔH2,答案选C。 6.按下图的装置进行实验,若图中x轴表示阴极的电子的量,则y轴可能表示( ) A. Cu2+物质的量浓度 B. Fe棒的质量 C. Cl-物质的量浓度 D. C棒的质量 【答案】D 【解析】 石墨为阳极,铁为阴极,电解氯化铜溶液,总反应为:CuCl2Cu+Cl2↑。因为铜离子得电子转化为单质附着在铁电极表面,所以随着电子的转移,Cu2+ 物质的量浓度减小,Fe棒的质量增加,选项A、选项B都错误。反应中氯离子也会失电子转化为氯气,所以随着电子的转移,Cl-物质的量浓度减小,选项C错误。反应中石墨电极表面生成氯气,不影响石墨电极的质量,所以电子转移,石墨质量不变,选项D正确。 7.下列三种有机物是某些药物中的有效成分: 以下说法正确的是( ) A 三种有机物都能与浓溴水发生反应 B. 三种有机物苯环上的氢原子若被氯原子取代,其一氯代物都只有2种 C. 将等物质的量的三种物质加入氢氧化钠溶液中,阿司匹林消耗氢氧化钠最多 D. 使用FeCl3溶液和稀硫酸不能鉴别出这三种有机物 【答案】C 【解析】 【详解】A、对羟基桂皮酸中含有酚羟基,能够与溴水发生取代反应,而布洛芬和阿司匹林不与浓溴水反应,故A错误; B、苯环上的氢原子被氯原子取代,其前两种的一氯代物有2种,第三种的一氯代物有4种,故B错误; C、将等物质的量的三种物质加入氢氧化钠溶液中,对羟基桂皮酸中酚羟基和羧基与氢氧化钠反应,布洛芬中羧基与氢氧化钠反应,阿司匹林中羧基和酯基与氢氧化钠反应,其中酯水解得到酚羟也会与氢氧化钠反应,则消耗氢氧化钠的之比为:2:1:3,故C正确; D、对羟基桂皮酸中含有酚羟基,遇FeCl3溶液发生显色反应,阿司匹林中有酯基,遇稀硫酸发生酯的水解,香味变淡,则使用FeCl3溶液和稀硫酸能鉴别出这三种有机物,故D错误, 答案选C。 8.下列图示中关于铜电极的连接错误的是 A. 铜锌原电池 B. 电解精炼铜 C. 镀件上镀铜 D. 电解氯化铜溶液 【答案】C 【解析】 【详解】A、该原电池中,较活泼的金属锌作负极,较不活泼的金属铜作正极,故A正确; B、电解精炼铜时,粗铜作阳极,阳极上铜失电子发生氧化反应,纯铜作阴极,阴极上铜离子得电子发生还原反应,故B正确; C、电镀时,镀层铜作阳极,镀件作阴极,电解过程中,铜离子在阴极析出,故C错误; D、电解氯化铜溶液时,惰性电极作阳极,则阳极上氯离子放电生成氯气,无论阴极是否活泼,阴极上都是铜离子得电子生成铜,故D正确; 故选C。 二、不定项选择题(每小题4分,共计24分。每小题有一个或两个选项符合题意。若正确答案只包括一个选项,多选得0分,若正确答案包含两个选项,只选一个且正确得2分,选两个且都正确得4分,只要选错一个就得0分) 9.下面是丁醇的两种同分异构体,其结构简式、沸点及熔点如下表所示: 异丁醇 叔丁醇 结构简式 沸点/℃ 108 82.3 熔点/℃ -108 25.5 下列说法不正确的是 A. 用系统命名法给异丁醇命名为:2-甲基-1-丙醇 B. 异丁醇的核磁共振氢谱有三组峰,且面积之比是1∶2∶6 C. 用蒸馏的方法可将叔丁醇从二者的混合物中分离出来 D. 两种醇发生消去反应后得到同一种烯烃 【答案】B 【解析】 【详解】A. 醇的系统命名步骤:1.选择含羟基的最长碳链作为主链,按其所含碳原子数称为某醇;2.从靠近羟基的一端依次编号,写全名时,将羟基所在碳原子的编号写在某醇前面,例如1-丁醇CH3CH2CH2CH2OH;3.侧链的位置编号和名称写在醇前面。因此系统命名法给异丁醇命名为:2-甲基-1-丙醇,故不选A; B. 有几种氢就有几组峰,峰面积之比等于氢原子个数比;异丁醇的核磁共振氢谱有四组峰,且面积之比是1∶2∶1∶6,故选B; C. 根据表格可知,叔丁醇的沸点与异丁醇相差较大,所以用蒸馏的方法可将叔丁醇从二者的混合物中分离出来,故不选C; D. 两种醇发生消去反应后均得到2-甲基丙烯,故不选D; 答案:B 10.电化学气敏传感器可用于监测环境中的含量,其工作原理如图所示,被氧气化为,下列说法错误的是 A. 溶液中向电极b移动 B. 氨气在电极a上发生氧化反应 C. 反应消耗的与的物质的量之比为4:5 D. 正极的电极反应式为: 【答案】C 【解析】 【分析】 该电池为燃料电池,根据装置图,通氨气一极为负极,通氧气一极为正极,然后根据原电池工作原理进行分析; 【详解】根据装置图,通氨气一极为负极,通氧气一极为正极, A、根据上述分析,a为负极,b为正极,根据原电池工作原理可知,K+从a极移向b极,故A说法正确; B、通氨气一极为负极,N元素的化合价升高,发生氧化反应,故B说法正确; C、根据得失电子数目守恒,n(NH3)×3=n(O2)×4,n(NH3):n(O2)=4:3,故C说法错误; D、环境为碱性,因此正极反应式为O2+4e-+2H2O=4OH-,故D说法正确; 11.下列表述正确的是 ( ) A. 已知在常温常压下:CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH= -890.3kJ·mol-1甲烷的燃烧热为ΔH= -890.3kJ·mol-1, B. 加入催化剂可以改变化学反应的反应热,使反应更容易发生. C. 等质量的硫蒸气和硫固体分别完全燃烧,后者放出的热量更多 D. 同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的ΔH相同 【答案】D 【解析】 【详解】A、在25℃,100kPa时,1 mol纯物质完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热,应生成液态水,选项A错误; B、反应热只与反应物总能量和生成物总能量的相对大小有关系,选项B错误; C、等质量的硫蒸气和硫固体分别完全燃烧,前者放出热量更多,选项C错误; D、反应热与反应物的总能量和生成物的总能量有关,与反应条件无关,则光照和点燃条件的△H相同,选项D正确; 答案选D。 12.某种药物合成中间体的结构简式如下,有关该物质的说法不正确的是( ) A. 属于芳香烃 B. 能发生消去反应和酯化反应 C. 分子中所有碳原子不可能在同一平面内 D. 1mol该有机物与足量NaOH溶液反应,消耗5mol NaOH 【答案】AD 【解析】 【详解】A.分子中含有苯环,为芳香族化合物,含有氧元素,不属于芳香烃,选项A不正确; B.分子中含有醇羟基,可发生消去和酯化反应,选项B正确; C.分子中含有环烷烃的结构,所有碳原子不可能在同一平面上,选项C正确; D.分子中含有2个酚羟基和1个羧基,则1mol该有机物与足量NaOH溶液反应,消耗3mol NaOH,选项D不正确; 答案选AD。 【点睛】本题考查有机物结构与性质,比较基础,注意掌握官能团的性质与转化,易错点为D.分子中含有2个酚羟基和1个羧基,则1mol该有机物与足量NaOH溶液反应,消耗3mol NaOH,注意结构上有两个为醇羟基。 13.下列各组热化学方程式中,化学反应的ΔH前者大于后者的是 ( ) A. C(s)+O2(g)=CO2(g) ΔH1 C(s)+O2(g)=CO(g) ΔH2 B. S(g)+O2(g)=SO2(g) ΔH3 S(l)+O2(g)=SO2(g) ΔH4 C. 2H2(g)+O2(g)=2H2O(l) ΔH5 H2(g)+ O2(g)=H2O(l) ΔH6 D. CaCO3(s)=CaO(s)+CO2(g) ΔH7 CaO(s)+H2O(l)=Ca(OH)2(s) ΔH8 【答案】D 【解析】 【详解】A、完全燃烧产生的热量大于不完全燃烧产生的热量,ΔH前者小于后者; B、相同质量的物质,气态含有的能量高于固体的,因此前者放出的能量多,ΔH前者小于后者; C、物质状态相同时,物质反应的越多,放出的热量就越多,ΔH前者小于后者; D、前者是吸热反应,后者是放热反应,所以ΔH前者大于后者; 答案选D。 14.锂电池用金属锂和石墨作电极材料,电解质溶液是由四氯铝锂(LiAlCl4)溶解在亚硫酰氯(SOCl2)中形成,该电池的总反应方程式为:8Li+3SOCl2=6LiCl+Li2SO3+2S,下列叙述中正确的是( ) A. 电解质溶液中混入水,对电池反应无影响 B. 上述过程中是化学能转化成电能 C. 电池工作过程中,亚硫酰氯(SOCl2)被氧化为Li2SO3 D. 电池放电时,金属锂提供电子的物质的量与析出硫的物质的量之比为4 :1 【答案】BD 【解析】 【详解】A、锂性质活泼,易与水反应,且SOCl2对水也不稳定,则电解质为非水溶液,选项A错误; B、上述过程是原电池原理,是化学能转化成电能,选项B正确; C、根据总反应8Li+3SOCl2=6LiCl+Li2SO3+2S可知,亚硫酰氯(SOCl2)被还原为S,选项C错误; D、根据总反应8Li+3SOCl2=6LiCl+Li2SO3+2S可知,8mol锂反应失去8mol电子,生成2mol S,金属锂提供的电子与正极区析出硫的物质的量之比为4: 1,选项D正确; 答案选BD。 【点睛】本题考查化学电源新型电池,该电池的负极材料为锂,性质活泼,易与水反应,则电解质为非水溶液,根据总反应8Li+3SOCl2=6LiCl+Li2SO3+2S可知,亚硫酰氯( SOCl2 )被还原为S,由反应的总方程式可知金属锂提供的电子与正极区析出硫的物质的量之比。 第II卷(共60分) 三、填空题(共5题) 15.从樟科植物枝叶提取的精油中含有下列甲、乙两种成分: (1)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同): 设计步骤①和③的目的是__________________________;指出①的反应类型____________;反应②的化学方程式为____________________________________________________。 (2)欲检验乙中的含氧官能团,下列试剂可选用的是_______________。 A.溴水 B.酸性高锰酸钾溶液 C.溴的CCl4溶液 D.银氨溶液 (3)乙经过氢化、氧化得到丙()。写出同时符合下列要求的丙的两个同分异构体结构简式_______________________、________________________。 ①能发生银镜反应; ②能与FeCl3溶液发生显色反应; ③核磁共振氢谱图上产生4个吸收峰。 【答案】 (1). 保护碳碳双键,防止其被氧化 (2). 加成反应 (3). 2+O2+2H2O (4). D (5). (6). 【解析】 【分析】 (1)甲发生加成反应生成,发生氧化反应生成X,X发生消去反应生成乙,据此分析; (2)乙中的含氧官能团为醛基,醛基的检验用银氨溶液; (3)丙为,其同分异构体中①能发生银镜反应,则含-CHO;②能与FeC13溶液发生显色反应,则含酚-OH;③核磁共振氢谱图上产生4个吸收峰,分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,据此分析。 【详解】(1)甲发生加成反应生成,发生氧化反应生成X,X发生消去反应生成乙,则设计步骤①和③的目的是保护碳碳双键,防止其被氧化; 反应①的反应类型为加成反应; 反应②的化学方程式为2+O2+2H2O; (3)乙中的含氧官能团为醛基,醛基的检验用银氨溶液; 答案选D; (4)丙为,其同分异构体中①能发生银镜反应,则含-CHO; ②能与FeC13溶液发生显色反应,则含酚-0H;③核磁共振氢谱图上产生4个吸收峰,分子中有四种不同化学环境的H原子,则苯环上和甲基中各有1种位置的H,符合条件的同分异构体为、。 16.阅读下列有关能源的材料,回答有关问题: (1)在常温,1.01×105Pa时,48g 甲醇在足量的氧气中充分燃烧生成二氧化碳和液态水,放出1089kJ的热量,则表示甲醇燃烧热的热化学方程式为____________________________。 (2)在生产和生活中经常遇到化学能与电能的相互转化。在如图甲、乙两装置中,甲中负极电极反应式为____________________________,甲中的阳离子向 _______ 极移动(填“正”或“负”);乙中铝电极作____极,乙中正极电极反应式为____________________________ (3)肼(N2H4)可作为火箭发动机的燃料,有关肼化学反应的能量变化如图所示,已知断裂1mol化学键所需的能量(kJ):N≡N为944、O=O为500、N-N为154,则反应物转化为中间产物的ΔH3=_________,断裂1 mol N—H键所需的能量是__________ kJ。 (4)工业制氢气的一个重要反应是:CO(g)+ H2O(g) =CO2(g) + H2(g), 已知25℃时: C(石墨)+O2(g) = CO2(g) ; △H1 = -394 kJ•mol-1 C(石墨)+O2(g) = CO(g); △H2 = -111 kJ•mol-1 H2(g)+ O2 (g)=H2O(g); △H3= -242kJ•mol-1 试计算25℃时CO(g)+H2O(g)=CO2(g)+H2(g)的反应热△H=____________kJ•mol-1。 【答案】 (1). CH3OH(l)+O2(g)=CO2(g)+2H2O(l) △H=-726kJ/moL (2). Zn-2e-=Zn2+ (3). 正 (4). 负 (5). 2H2O+2e-=H2↑+2OH- (6). +2218kJ/moL (7). 391 (8). -39kJ/moL 【解析】 【分析】 根据盖斯定律,由已知热化学方乘以适当的系数进行加减构造目标热化学方程式,反应热也乘以相应的系数并进行相应的加减,据此计算。 【详解】(1)48g CH3OH在氧气中燃烧生成CO2和液态水,放出1089kJ热量,32g即1mol CH3OH在氧气中燃烧生成CO2和液态水,放出726kJ热量,则表示甲醇燃烧热的热化学方程式为:CH3OH(g)+O2(g)═CO2(g)+2H2O(l) △H= -726kJ/mol; (2)原电池中较活泼的金属是负极,失去电子,发生氧化反应,甲中负极电极反应式为:Zn-2e-=Zn2+;原电池中阳离子向正极移动,即向Pt电极移动; 乙中镁的金属性强于铝的,但镁不与氢氧化钠溶液反应,铝与氢氧化钠溶液反应,铝失电子作为负极,乙中正极上水电离产生的氢离子得电子产生氢气,电极反应式为2H2O+2e-=H2↑+2OH-; (3)根据图像可知:N2H4(g)+O2(g)=2N(g)+4H(g)+2O(g) △H3=2752kJ/mol-534kJ/mol=+2218kJ/mol; 化学反应中,旧键断裂吸收能量,设断裂1molN-H键所需的能量为x,则旧键断裂吸收的能量=154+4x+500=2218,解得:x=391; (4)已知在25℃时: ①C(石墨)+O2(g)═CO2(g) △H1= -394kJ/mol ②C(石墨)+O2(g)═CO(g) △H2= -111kJ/mol ③H2(g)+O2(g)═H2O(g) △H3= -242kJ/mol 由盖斯定律,①-③-②得:CO(g)+H2O(g)═CO2(g)+H2(g),故△H=△H1-△H3-△H2= -111kJ/mol -(-394kJ/mol)-(-242kJ/mol)= -39kJ/mol。 17.肉桂酸甲酯( )可用于调制草莓、葡萄、樱桃等香味的食用香精。 (1)肉桂酸甲酯的分子式是__________________。 (2)有关肉桂酸甲酯的叙述中,不正确的是____________(填标号)。 A.能与溴的四氯化碳溶液发生加成反应 B.无法使酸性高锰酸钾溶液褪色 C.在碱性条件下能发生水解反应 D.不可能发生加聚反应 (3)G为肉桂酸甲酯的同分异构体,其分子结构模型如图所示(图中、、表示不同的原子,连线表示原子间的共价键)。G的结构简式为________________ 。 (4)用芳香烃A为原料合成G的路线如下: ①化合物E中的官能团有_____________________(填名称)。 ②E→F的反应类型是__________,该反应的化学方程式为:_____________________________ 写出符合下列条件的F的同分异构体的结构简式:___________________________________ ⅰ.分子内含苯环,且苯环上只有一个支链; ⅱ.一定条件下,1 mol该物质与足量的银氨溶液充分反应,生成4 mol银单质。 【答案】 (1). C10H10O2 (2). BD (3). (4). 羧基、羟基 (5). 消去反应 (6). +H2O (7). 【解析】 【分析】 (1)根据结构简式得出其分子式; (2)含有碳碳双键,决定具有烯的性质;含有酯基决定具有酯的性质.苯环虽不是官能团,但含有苯环,具有苯的一些性质; (3)G为肉桂酸甲酯的一种同分异构体,根据结构可知,黑色球是C原子、白色球是H原子、斜线球是O原子,再根据C的四价结构确定C原子间的成键情况,写出G的结构简式; (4)①根据D、E的分子式可知,E比D多1个O原子,再结合G的结构,所以应是D中的醛基被氧化为羧基而生成E; ②根据G的结构可知,F为,E→F的反应为消去反应; 根据条件推出F的同分异构体的结构简式。 【详解】(1)根据结构简式可知,肉桂酸甲酯( )的分子式是C10H10O2; (2)A、分子中含有碳碳双键,能与溴的四氯化碳溶液发生加成反应,选项A正确; B、分子中含有碳碳双键,能被酸性高锰酸钾溶液氧化,而使酸性高锰酸钾溶液褪色,选项B不正确; C、分子中含有酯基,在碱性条件下能发生水解反应,得到相应羧酸的盐和甲醇,选项C正确; D、分子中含有碳碳双键,能发生加聚反应,选项D不正确; 答案选BD; (3)G为肉桂酸甲酯的一种同分异构体,结合图中结构可知,黑色球是C原子、白色球是H原子、斜线球是O原子,再根据C的四价结构确定C原子间的成键情况,所以G的结构简式为; (3)①根据D、E的分子式可知,E比D多1个O原子,再结合G的结构,所以D中的醛基被氧化为羧基而生成E,所以E中含有的官能团是羟基、羧基; ②根据G的结构可知,F为,E→F是发生消去反应生成和水,反应类型为消去反应;反应的化学方程式为:+H2O; F()的同分异构体,符合ⅰ.分子内含苯环,且苯环上只有一个支链;ⅱ.一定条件下,1 mol该物质与足量的银氨溶液充分反应,生成4 mol银单质,则含有两个醛基,符合条件的同分异构体有。 18 .如图表示一个电解池,装有电解液a、X、Y是两块电极板,通过导线与直流电源相连,请回答以下问题: (1)若X、Y是惰性石墨电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴石蕊试液,在X极附近观察到的现象是______________________________;Y电极上的电极反应式是 ___________________,电解NaCl溶液的离子方程式是________________________________。 (2)若要在铜制品上镀Ag,则电解质溶液a可为___________________,Y电极反应式为_________________________________。 (3)若上图装置中的电源为甲醇—空气—KOH溶液的燃料电池,则电池负极的电极反应式_________________,电池工作过程中,正极附近的pH将______(填“增大、减小或不变”)。 【答案】 (1). 石蕊溶液变蓝,有气泡产生 (2). 2Cl--2e-=Cl2↑ (3). 2Cl-+2H2O2OH-+Cl2↑+H2↑ (4). AgNO3溶液 (5). Ag-e-=Ag+ (6). CH3OH-6e-+8OH- = CO32-+6H2O (7). 增大 【解析】 【分析】 (1)电解饱和食盐水时,阳极上是氯离子失电子,阴极上是氢离子得电子; (2)若要在铜上镀银,镀层作阳极,镀件作阴极,电解质为含有与阳极材料相同金属元素的可溶性盐,阴极上银离子得电子发生还原反应; (3)依据燃料电池中燃料在负极失电子发生氧化反应,结合电荷守恒配平书写电极反应。 【详解】(1)①和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴石蕊试液会变蓝,则在X极附近观察到的现象是石蕊溶液变蓝,有气泡产生; 和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e- =Cl2↑,电解NaCl溶液的离子方程式是2Cl-+2H2O2OH-+Cl2↑+H2↑; (2)若要在铜上镀银,镀层作阳极,镀件作阴极,要想在铜上镀银,电解质为含有与阳极材料相同金属元素的可溶性盐,则电解质溶液a可为AgNO3溶液;Y电极为阳极,Ag失电子产生Ag+,电极反应式为Ag- e- = Ag+; (3)若上图装置中的电源为甲醇-空气-KOH溶液的燃料电池,甲醇在负极失电子发生氧化反应,在碱溶液中生成碳酸盐,则电池负极的电极反应式为CH3OH-6e-+8OH-═CO32-+6H2O,电池工作过程中,正极氧气得电子产生OH-,附近的pH将增大。 19.水杨酸甲酯是一种无色透明油状液体,相对分子质量为152,密度为1.184g•cm﹣3,沸点223.3℃,熔点﹣86℃,微溶于水,易溶于有机溶剂,露置在空气中则易缓慢变色。由水杨酸和甲醇在浓硫酸存在条件下反应制得水杨酸甲酯(冬青油)的反应如下: 某学校的实验探究小组利用如图装置制备冬青油.步骤如下 ①将三颈烧瓶、量筒,置于烘箱中干燥10min; ②用天平称取6.9g水杨酸,用量筒分别量取30mL(约24g)甲醇,6mL浓硫酸,然后将3种试剂分别加入已干燥的三颈烧瓶中,组装好实验装置后置于磁力搅拌加热器上加热; ③加热到85~95℃,反应结束后将盛有混合物的烧瓶置于冷水浴中冷却,然后再将冷却后的混合物倒入分液漏斗中,依次加入NaHCO3溶液和30mL水,充分震荡,静置,分层; ④弃去水层,将有机层注入干燥的锥形瓶中,加入适量无水氯化钙; ⑤将步骤④所得的产品蒸馏,收集221~224℃的馏分,称得产物质量为4.56g 试回答下列问题: (1)装置中仪器a的作用是_______________;水应该从________(填“Ⅰ”或“Ⅱ”)处流入,仪器b的适宜规格为___________(填序号); ①10℃ ②50℃ ③150℃ (2)加入NaHCO3溶液的目的除了将冬青油中的甲醇、水杨酸、硫酸等除去外,还有___________;加入水震荡分层后,冬青油的粗产品在_______(填“上”或“下”)层; (3)在本实验分离过程中,水层应该从分液漏斗的_________________(填“上口倒出”或“下口放出”); (4)本次实验冬青油的产率是____________。 【答案】 (1). 冷凝回流 (2). Ⅱ (3). ③ (4). 降低冬青油在水中的溶解度 (5). 下层 (6). 上口倒出 (7). 60% 【解析】 【分析】 (1)分析装置图和仪器形状分析为冷凝管,逆流冷凝效果好;反应加热加热到85~95℃,发生反应,所以反应的温度计应选择大于此量程的温度计; (2)加入NaHCO3溶液的目的是降低酯的溶解性,水杨酸,溶解甲醇,便于分层分类得到酯;冬青油密度为1.184g/cm-3,比水溶液重; (3)冬青油的粗产品的密度比水大,水层应从分液漏斗的上口倒出; (4)结合反应定量关系计算理论量,产率=×100%。 【详解】(1)分析装置图和仪器形状分析为冷凝管,逆流冷凝效果好,应从Ⅱ通入;反应加热加热到85~95℃,发生反应,所以反应的温度计应选择大于此量程的温度计,选择150℃的温度计; 故答案为:冷凝管,Ⅱ;③; (2)加入NaHCO3溶液的目的是降低酯的溶解性,水杨酸,溶解甲醇,便于分层分类得到酯;冬青油密度为1.184g/cm-3,比水溶液重,粗产品在下层; 故答案为:降低冬青油在水中的溶解度;下层; (3)冬青油的粗产品的密度比水大,水层应从分液漏斗的上口倒出; 故答案为:上口倒出; (4)结合反应定量关系计算理论量, 138 152 6.9g m m=7.6g 产率=×100%=×100%=60%。 【点睛】本题考查了有机物的性质分析和实验制备方法,实验基本操作和有机物性质和反应原理是解题关键,易错点为(1)分析装置图和仪器形状分析为冷凝管,逆流冷凝效果好;反应加热加热到85~95℃,发生反应,所以反应的温度计应选择大于此量程的温度计。查看更多