- 2021-05-10 发布 |
- 37.5 KB |
- 3页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
中考化学专题复习热点题型归类推断题
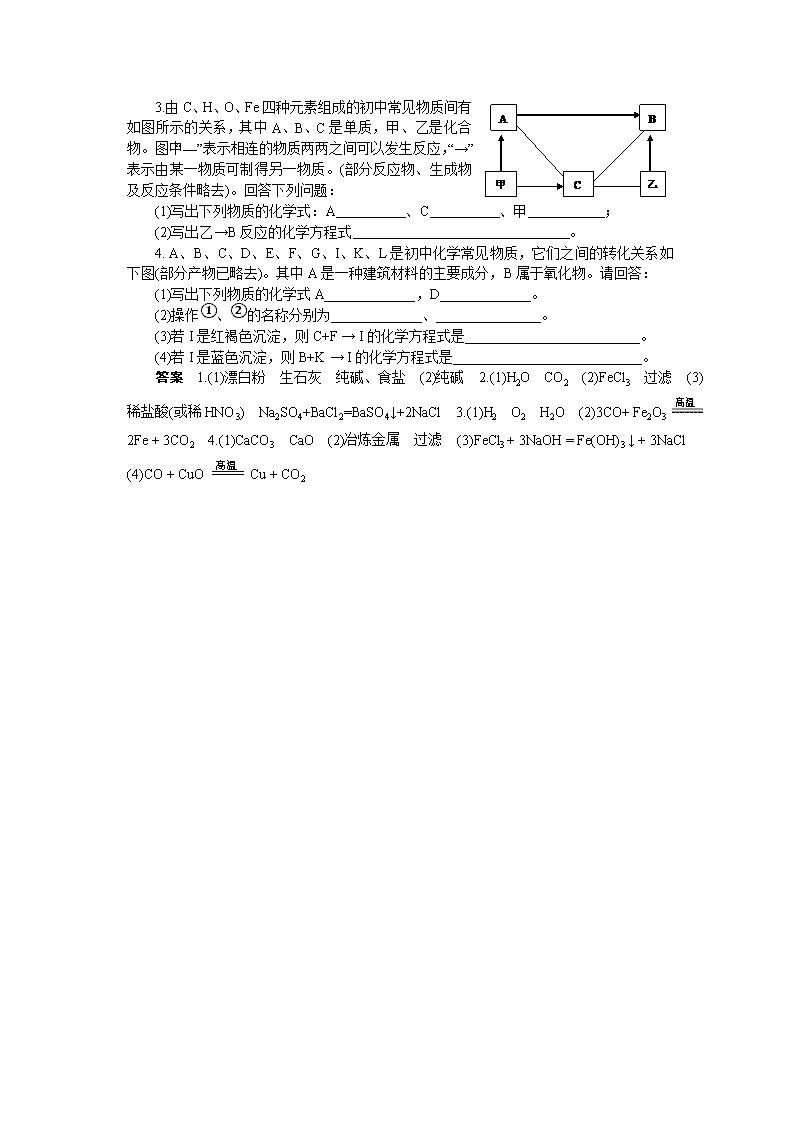
推断题 例1 现有木炭、一氧化碳、氧化铜、氧化铁、稀硫酸五种物质,它们之间发生的反应,可用“A + B → C + D”表示。 (1)若A为单质,A与B在高温下反应,可观察到固体粉末由黑色逐渐变红,则B是______________,其反应类型为_____________________。 (2)若A为气体化合物,A与B在高温下反应,可观察到固体粉末由红色逐渐变黑,则B是________________。 (3)若A溶液pH < 7,A与B在常温下反应,可观察到溶液由无色变为黄色,则A与B反应的化学方程式为_______________,其反应类型为____________。 解析 木炭还原氧化铜生成红色的铜和二氧化碳,则B是氧化铜,该反应属于置换反应;一氧化碳还原氧化铁生成铁粉和二氧化碳,铁粉呈黑色;溶液pH < 7,呈酸性,A为稀硫酸,黄色溶液是可溶性铁盐溶液,即B是氧化铁,反应的化学方程式是Fe2O3+3H2SO4=Fe2(SO4)3+3H2O,属于复分解反应。 答案 (1)氧化铜 置换反应 (2)氧化铁 (3)Fe2O3+3H2SO4=Fe2(SO4)3+3H2O 复分解反应 例2 用五个圆表示A(氧化铁)、B(稀硫酸)、C(碳酸钠溶液)、D(稀盐酸)、E(氯化钡溶液)五种物质,用两圆相切表示两种物质可以发生反应,如图所示。请回答下列问题: (1)将C、D、E三个圆画到图中A、B周围适当的位置,并标出物质; (2)反应生成白色沉淀的化学方程式为 ; (3)A与B反应的实验现象是 。 解析 根据“两圆相切表示两种物质可以发生反应”,上述五种物质两两之间的反应关系为: 根据图示易知:A(Fe2O3)、B(H2SO4)、C(Na2CO3)、D(HCl)四种物质两两相切,而E(BaCl2)与B(H2SO4)、C(Na2CO3)都相切;在上述反应中,H2SO4与BaCl2、Na2CO3与BaCl2反应都能生成白色沉淀;氧化铁是红色固体,与稀硫酸反应生成黄色的Fe2(SO4)3溶液。 答案 (1)如图所示 (2)Na2CO3+BaCl2=BaCO3↓+2NaCl BaCl2+H2SO4=BaSO4↓+2HCl (3)(红色)固体减少(或消失),溶液由无色变为黄色 例3 现有一包固体粉末,可能由CaCO3、CaO、Na2CO3中的一种或几种组成。为确定其组成,进行了如下图所示的实验(假设实验过程无损耗)。 请回答: (1)根据实验可以确定白色沉淀是___________;原固体粉末中一定含有___________,它的可能组成有___________种。 (2)若实验取固体粉末20g,生成白色沉淀10g,最后得到溶质质量分数为5.85%的X溶液200g(只含一种溶质),则X溶液中溶质的质量是___________g,固体粉末由___________(填化学式,下同)组成,其中质量小于10g的是___________。 解析 CaO溶于水生成Ca(OH)2,Ca(OH)2与Na2CO3反应也产生白色沉淀,即不管原粉末中是否含有 CaCO3,则白色沉淀一定为CaCO3;在滤液中加稀盐酸产生无色气体,说明滤液中含CO32-,即原粉末中一定含有Na2CO3,则其可能组合为:①CaCO3和Na2CO3;②CaO和Na2CO3;③CaCO3、CaO、Na2CO3。 X溶液中溶质为NaCl,质量为200g×2.85%=11.7g。设固体粉末中Na2CO3的质量为x。由钠元素守恒,推知关系式:Na2CO3~2NaCl 106 117 117 106×11.7g x 11.7g x= =10.6g 即20g固体粉末中Na2CO3占10.6g,若10g白色沉淀仅由原混合物中CaCO3提供,则CaCO3的质量为20g-10.6g=9.4g<10g,不成立,即原组合为:CaO、Na2CO3和CaCO3的混合,其中质量小于10g的为CaO和CaCO3。 答案 (1)CaCO3(或“碳酸钙”) Na2CO3(或“碳酸钠”) 3 (2)11.7 CaCO3、CaO、Na2CO3 CaCO3、CaO 例4 图中字母A~I分别表示不同的常见物质。“→”表示物质间存在转化关系,部分反应条件和部分生成物已略去。 请回答下列问题: (1)反应①的基本反应类型为____________。 (2)写出与A具有相同元素组成的另一种物质的名称和其一种用途:名称_______,用途_____________。 (3)写出C、G的化学式:C_____________, G______________。 加热 (4)写出反应②的化学方程式:______________________。 高温 解析 H为紫红色单质,可推知H为Cu;由G(气体)+B(黑色固体)——→H(Cu)可推知:B中含有铜元素,又是黑色固体,则B为CuO,再由B(CuO)+盐酸→D知:D为CuCl2;由I为浅绿色溶液,可推知I为含Fe2+的溶液,由D(CuCl2)+E(单质)→I(FeCl2)+H(Cu)知:E为Fe,则反应②为:Fe+CuCl2=FeCl2+Cu;含有铁元素的红棕色固体C为Fe2O3,高温时还原Fe2O3生成单质铁知,单质A为碳,故由碳元素组成的另一种单质为金刚石,可用作装饰品,则反应①为:Fe2O3+2C4Fe+3CO2↑,反应类型为置换反应,由A(C)+F(CO2)——→G知:G为CO。 答案 (1)置换反应 (2)金刚石 装饰品(或其他合理答案) (3)Fe2O3 CO (4)Fe + CuCl2 = FeCl2 + Cu 跟踪训练 1.小林的妈妈把家庭久置不用的食盐、纯碱、漂白粉(主要成分是氯化钙和碳酸钙)和生石灰干燥剂中的一种或几种打包准备扔掉。小林为研究白色粉末的组成,将其带到实验室,设计并进行了以下实验: (1)将部分粉末放人烧杯中,加适量水充分搅拌后,得到白色浊液,杯壁温度无明显变他得出:粉末中一定含有__________,一定没有__________,可能含有__________; (2)向实验(1)的浊液中滴加酚酞试剂,浊液变红。查阅资料知食盐、氯化钙溶液呈中性他又得出粉末中一定含有___________。 经反思,小林感觉实验设计还不完善,不能确定粉末中是否含有食盐。 2.实验室有一包粉末状物质,可能由NaCl、Na2SO4、Na2CO3、FeCl3中的一种或几种组成。为了确定原粉末的成分,某校化学兴趣小组的同学,按下图所示进行实验: 请回答下列问题(填化学式): (1)若A是相对分子质量最小的氧化物,则A为 ;无色气体是 。 (2)该粉末中一定不含 ,操作Ⅰ的名称是 。 (3)为了不干扰对第③步实验现象的判断,试剂B最好选择 ,请写出步骤③的化学方程式: 。 3.由C、H、O、Fe四种元素组成的初中常见物质间有如图所示的关系,其中A、B、C是单质,甲、乙是化合物。图中“—”表示相连的物质两两之间可以发生反应,“→”表示由某一物质可制得另一物质。(部分反应物、生成物及反应条件略去)。回答下列问题: (1)写出下列物质的化学式:A 、C 、甲 ; (2)写出乙→B反应的化学方程式 。 4. A、B、C、D、E、F、G、I、K、L是初中化学常见物质,它们之间的转化关系如下图(部分产物已略去)。其中A是一种建筑材料的主要成分,B属于氧化物。请回答: (1)写出下列物质的化学式A_____________,D_____________。 (2)操作①、②的名称分别为_____________、_______________。 (3)若I是红褐色沉淀,则C+F → I的化学方程式是_________________________。 (4)若I是蓝色沉淀,则B+K → I的化学方程式是___________________________。 答案 1.(1)漂白粉 生石灰 纯碱、食盐 (2)纯碱 2.(1)H2O CO2 (2)FeCl3 过滤 (3)稀盐酸(或稀HNO3) Na2SO4+BaCl2=BaSO4↓+2NaCl 3.(1)H2 O2 H2O (2)3CO+ Fe2O3 2Fe + 3CO2 4.(1)CaCO3 CaO (2)冶炼金属 过滤 (3)FeCl3 + 3NaOH = Fe(OH)3 ↓ + 3NaCl (4)CO + CuO Cu + CO2查看更多