- 2021-05-08 发布 |
- 37.5 KB |
- 5页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
中考化学真题试题
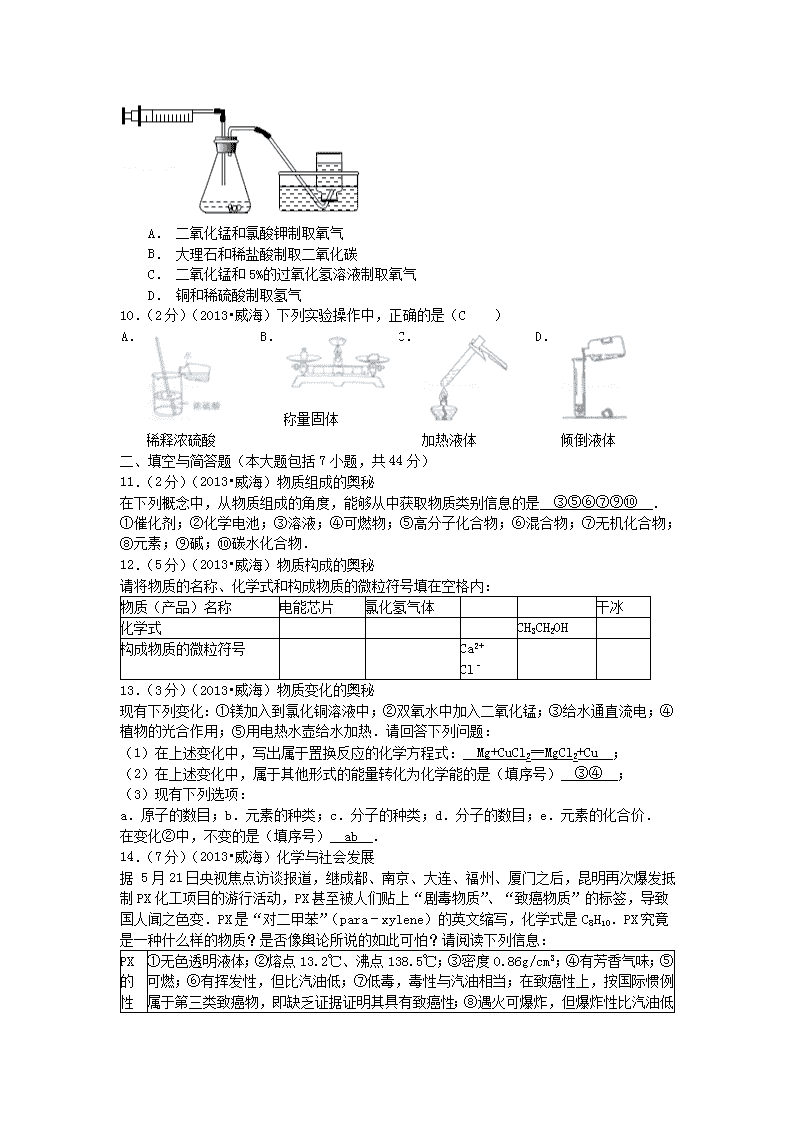
山东省威海市 中考化学试卷 一、选择题(本题包括10小题,每小题2分,共20分。每小题只有一个选项符合题意) 1.(2分)(2013•威海)在自然科学领域,对于“物质”概念的认识中,正确的是( D ) A. 物质不灭理论说明物质不会转化 B. 物质用肉眼都能看的见,但构成物质的微粒,用肉眼都是看不见的 C. 物质是可变的,但物体在静止状态下,构成物质的微粒是不会发生变化的 D. 物质都是由肉眼看不见的微粒按一定规律构成的 2.(2分)(2013•威海)下列对于物质变化的认识中,正确的是( A ) A. 我们观察到的物质的宏观变化,本质上都是构成物质的微粒不断运动与变化的结果 B. 外界条件是导致物质变化的决定性因素 C. 物质发生变化时,微粒之间一定发生了相互作用,而物质发生物理变化时,微粒之间没有发生相互作用 D. 凡是伴随着能量的变化,一定是化学变化 3.(2分)(2013•威海)化学变化的结果是有“新物质”生成.如果把反应物看成是“旧物质”,下面对“新物质”和“旧物质”的理解,正确的是( C ) A. 新物质是指世界上没有的物质 B. 新物质不会再变成其它物质 C. 新物质和旧物质的性质及用途不可能完全相同 D. 新物质的元素组成与旧物质的元素组成肯定不同 4.(2分)(2013•威海)化学上经常要使用下列各种“表”,根据物质的化学式并利用下表,能够计算出物质的相对分子质量的是( B ) A. 固体物质的溶解度表 B. 元素周期表 C. 常见元素的化合价表 D. 物质的密度表 5.(2分)(2013•威海)在下列概念中,一定属于描述物质化学变化规律的是( D ) A. 气化 B. 液化 C. 爆炸 D. 缓慢氧化 6.(2分)(2013•威海)在一定条件下,一容器内含有三种微观粒子,一种是阳离子,一种是阴离子,还有一种是分子,且三种微观粒子处于自由移动的状态.当改变条件后,容器内的部分阳离子和部分阴离子便处于不能自由运动的状态,这个过程属于( A ) A. 结晶 B. 蒸馏 C. 溶解 D. 过滤 7.(2分)(2013•威海)下列关于溶解度的说法,不正确的是( b ) A. 溶解度能够表示物质溶解性的强弱程度 B. 溶解度能够表示溶质在溶剂中溶解的程度 C. 溶解度能够表示某种物质在某种溶剂中的溶解限量 D. 在相同温度、相同溶剂的条件下,要判定不同物质的溶解度相对大小,可以根据其饱和溶液的溶质质量分数 8.(2分)(2013•威海)自然界存在许多循环现象,下列四种循环所发生的变化主要通过物理变化实现的是( D ) A. 碳循环 B. 氧循环 C. 二氧化碳循环 D. 水的天然循环 9.(2分)(2013•威海)在实验室里,利用下列物质和装置制取气体的方法正确的是( C ) A. 二氧化锰和氯酸钾制取氧气 B. 大理石和稀盐酸制取二氧化碳 C. 二氧化锰和5%的过氧化氢溶液制取氧气 D. 铜和稀硫酸制取氢气 10.(2分)(2013•威海)下列实验操作中,正确的是(C ) A. 稀释浓硫酸 B. 称量固体 C. 加热液体 D. 倾倒液体 二、填空与简答题(本大题包括7小题,共44分) 11.(2分)(2013•威海)物质组成的奥秘 在下列概念中,从物质组成的角度,能够从中获取物质类别信息的是 ③⑤⑥⑦⑨⑩ . ①催化剂;②化学电池;③溶液;④可燃物;⑤高分子化合物;⑥混合物;⑦无机化合物;⑧元素;⑨碱;⑩碳水化合物. 12.(5分)(2013•威海)物质构成的奥秘 请将物质的名称、化学式和构成物质的微粒符号填在空格内: 物质(产品)名称 电能芯片 氯化氢气体 干冰 化学式 CH3CH2OH 构成物质的微粒符号 Ca2+ Cl﹣ 13.(3分)(2013•威海)物质变化的奥秘 现有下列变化:①镁加入到氯化铜溶液中;②双氧水中加入二氧化锰;③给水通直流电;④植物的光合作用;⑤用电热水壶给水加热.请回答下列问题: (1)在上述变化中,写出属于置换反应的化学方程式: Mg+CuCl2═MgCl2+Cu ; (2)在上述变化中,属于其他形式的能量转化为化学能的是(填序号) ③④ ; (3)现有下列选项: a.原子的数目;b.元素的种类;c.分子的种类;d.分子的数目;e.元素的化合价. 在变化②中,不变的是(填序号) ab . 14.(7分)(2013•威海)化学与社会发展 据 5月21日央视焦点访谈报道,继成都、南京、大连、福州、厦门之后,昆明再次爆发抵制PX化工项目的游行活动,PX甚至被人们贴上“剧毒物质”、“致癌物质”的标签,导致国人闻之色变.PX是“对二甲苯”(para﹣xylene)的英文缩写,化学式是C8H10.PX究竟是一种什么样的物质?是否像舆论所说的如此可怕?请阅读下列信息: ①无色透明液体;②熔点13.2℃、沸点138.5℃;③密度0.86g/cm3 PX的性质 ;④有芳香气味;⑤可燃;⑥有挥发性,但比汽油低;⑦低毒,毒性与汽油相当;在致癌性上,按国际惯例属于第三类致癌物,即缺乏证据证明其具有致癌性;⑧遇火可爆炸,但爆炸性比汽油低(爆炸极限为1.1%~7.0%). PX的用途 化学工业的重要原料,用于纺织、塑料、建材、医药、农药等方面,如雪纺衣物、尼龙绳、塑料保险盒和保鲜袋等,涉及到衣食住行的方方面面.目前,我国每年需要PX1500万吨,而产量仅为800万吨,还需要进口700万吨;PX的价格与供应掌握在外国人手里.有趣的是,在游戏活动中,很多市民戴的口罩、穿的服装都是用PX做的. 根据上述信息,请你回答下列问题: (1)根据物质的组成对PX分类.它属于 有机物 ; (2)上表中属于PX物理性质的是(填性质代号) ①②③④⑥ ; (3)根据PX的性质,从防止环境污染和安全的角度,应如何保存和储运PX? 密封保存、严禁烟火 ; (4)试写出PX在空气中完全燃烧反应的化学方程式. 2C8H10+21O216CO2+10H2O ; (5)对于PX项目的利与弊,请从PX的性质、变化和用途的角度谈谈你的看法 从PX性质看,具有可燃性,爆炸性比汽油低,毒性与汽油相当,对人体危害小; 从燃烧产物看,PX燃烧产物是水和二氧化碳,对环境几乎没有危害; 从PX用途看,应用广泛,能够提高人们的生活质量,经济和社会价值显著. 综上所述,利大于弊. . 15.(11分)(2013•威海)像科学家一样“观察与思考”﹣﹣探秘水世界 如图所示的照片拍摄于我市某处天然温泉,请回答下列问题. (1)观察:当你用一种或多种感官去搜集有关这个世界的信息时,就是在观察. 这幅实景图片包含了与水有关的信息,请你从化学的视角观察图片,然后列出你观察到的关于水的一条信息. 看到了水、雪、雾 . (2)推理:当你对观察到的现象进行解释时,就是在推理,也叫推论.根据你观察到的结果,请做出一个推论. 推论:天气寒冷,气温低于0℃,依据:因为只有温度在0℃以下,水才能以雪的这种状态存在 . (3)理性思维:对比是常用的思维方法,比较是为了找出事物的相同点,对比是为了找出事物的不同点. 比较/对比图中①、②、③三处分子的特征、性质的异同,将结果填在表中.(如果不同,需按从大到小进行排序,填序号) 比较/对比项目 比较/对比结果 水分子的能量 水分子的运动速率 水分子的质量 水分子之间的相互作用力 水的化学性质 (4)物质的分类与符号表征: 天然温泉是大自然赐给人类的宝物.天然温泉富含人体所需的多种化学元素,但不同地区的温泉成分也不完全相同.已知上述温泉富含如下成分:一是钾、钠、钙、镁、铁等阳离子,二是氟、氧、碘、硫酸根等阴离子,三是硫磺、二氧化碳、二氧化硅、偏硅酸等物质.其中,属于单质的有(用化学符号表示) S ;由硫酸根离子和铁离子构成的盐是(用化学符号表示) Fe2(SO4)3 . (5)用微粒的观点认识水: 在100多年的近代自然科学史上,最有影响力的成果莫过于物质的原子/分子模型及物质构成的理论,因为该理论不仅可以很好地解释前人百思不得其解的某些自然现象,还可以指导我们更好地认识和改造物质.请你从物质的构成、分子的构成和原子的构成等层面,描述水的微观构成(任选其中2个层面即可) A. 水是由水分子构成的 . B. 每个水分子是由两个氢原子和一个氧原子构成的 . 16.(6分)(2013•威海)化学与健康: 科学研究表明,人体摄入酸性食物过多会造成酸性体质,酸性体质是百病之源.酸性食物和碱性食物是根据食物在人体内消化后终端产物的酸碱性来划分的,而不是食物本身的酸碱性.通常,富含S、Cl、P、N等非金属元素的食物进入体内,通过转化后会产生酸性物质,而富含K、Ca、Na、Fe、Zn、Mg等金属元素的食物进入体内,通过转化后产生碱性物质. 在一次聚会上,大家针对葡萄酒是酸性食物还是碱性食物的问题,进行了热烈的讨论.李叔叔说:喝葡萄酒对身体有利,因为我听说葡萄酒本身是碱性的,而且是强碱性的.宋叔叔认为:葡萄酒本身不可能呈碱性,而应该呈微弱的酸性,但葡萄酒属于碱性食物.聚会结束后,小玲同学查阅文献资料,获得下列信息: Ⅰ.制造葡萄酒的原料葡萄中富含K、Ca、Na、Fe、Zn、Mg等元素. Ⅱ.葡萄酒的酿制原理是利用野生酵母分解葡萄汁中的葡萄糖,最终转化为乙醇和二氧化碳. 针对上述讨论和提供的信息,请你回答下列问题. (1)在上述金属元素中,属于人体中常量元素的有 K、Ca、Na、Mg . (2)从科学探究的角度,李叔叔关于葡萄酒究竟是呈酸性还是呈碱性的认识方法是否正确 不正确 ;请说明理由 只是听说,没有经过实验验证 . (3)如果让你通过实验给葡萄酒的酸碱性下一个结论,其实验方法是 用pH试纸测定酸碱度或使用石蕊试液检验葡萄酒的酸碱性 ; (4)Ⅱ中发生反应的化学方程式为 C6H12O62C2H5OH+2CO2↑ ; (5)根据Ⅱ中葡萄酒的酿制原理,宋叔叔认定葡萄酒本身应该呈微弱的酸性,其原因是(用化学方程式表示) CO2+H2O═H2CO3 . 17.(10分)(2013•威海)像科学家一样“做科学”﹣﹣探秘氢氧化钠 实验室有一瓶长期暴露在空气中的氢氧化钠固体样品,观察发现,样品表面出现了大量的白色粉末.某兴趣小组的同学对该样品进行了探究.请回答下列问题: (1)实验证明,这份氢氧化钠已经变质,但不能确定是否完全变质.请你从下列药品中选择合适的试剂,探究氢氧化钠是否完全变质. 药品:蒸馏水、酚酞试液、稀盐酸、氯化钙溶液. 你的实验方案是 取少量待测液于试管,加入足量氯化钙或氯化钡溶液至不再产生白色沉淀;再向静置后的上述试管中,滴加少量酚酞溶液,如果溶液变红,则说明氢氧化钠部分变质;如果溶液没有变红,则说明氢氧化钠完全变质 .用化学方程式表示该实验中所依据的化学反应原理: Na2CO3+CaCl2=CaCO3↓+2NaCl . (2)如果给你一份未知浓度的稀硫酸,要求通过定量实验,测定氢氧化钠变质的程度(即样品中氢氧化钠的含量),请你给出具体的实验方案. 实验方案 反应的化学方程式 (3)实验证明,氢氧化钠部分变质,请你设计一个提纯该样品的实验方案,以得到纯净的氢氧化钠固体. 提纯样品应采用的试剂是 氢氧化钙溶液或氢氧化钡溶液 . 实验方案 反应的化学方程式 三、计算(本题共6分) 18.(6分)(2013•威海)为了节约林木资源,近几年兴起石头纸.石头纸可用沿海水产养殖中产生的大量废弃贝壳制得.为了测定某种贝壳中碳酸钙的质量分数,取贝壳15克,加入150克7.3%的盐酸溶液,充分反应后,称得剩余物质的总质量为159.72克.(假设贝壳中其它物质不与盐酸反应)有人认为,根据上述实验数据,可按如下方案计算:根据“150克7.3%的盐酸溶液”,得出参加反应的氯化氢质量,然后根据反应原理求得碳酸钙的质量,最后求出贝壳中碳酸钙的质量分数. (1)以上方案是否正确? 不正确,150克7.3%的盐酸溶液中的氯化氢未完全反应 . (2)计算贝壳中碳酸钙的质量分数. 解:(1)由反应的化学方程式CaCO3+2HCl═CaCl2+H2O+CO2↑碳酸钙与氯化氢的质量比为100:73,故150克7.3%的盐酸溶液能与15g碳酸钙完全反应.所以,氯化氢有剩余不能根据氯化氢质量计算.故以上方案不正确; (2)CO2的质量为:15g+150g﹣159.72g=5.28g 设样品中纯净CaCO3的质量为x,则 CaCO3+2HCl═CaCl2+H2O+CO2↑ 100 44 x 5.28g 解得:x=12g 贝壳中碳酸钙的质量分数为:×100%=80% 故答为:(1)不正确,150克7.3%的盐酸溶液中的氯化氢未完全反应;(2)贝壳中碳酸钙的质量分数为80%.查看更多