- 2021-04-29 发布 |
- 37.5 KB |
- 3页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
苏教版备战高考化学复习必修讲义铁及其重要化合物2
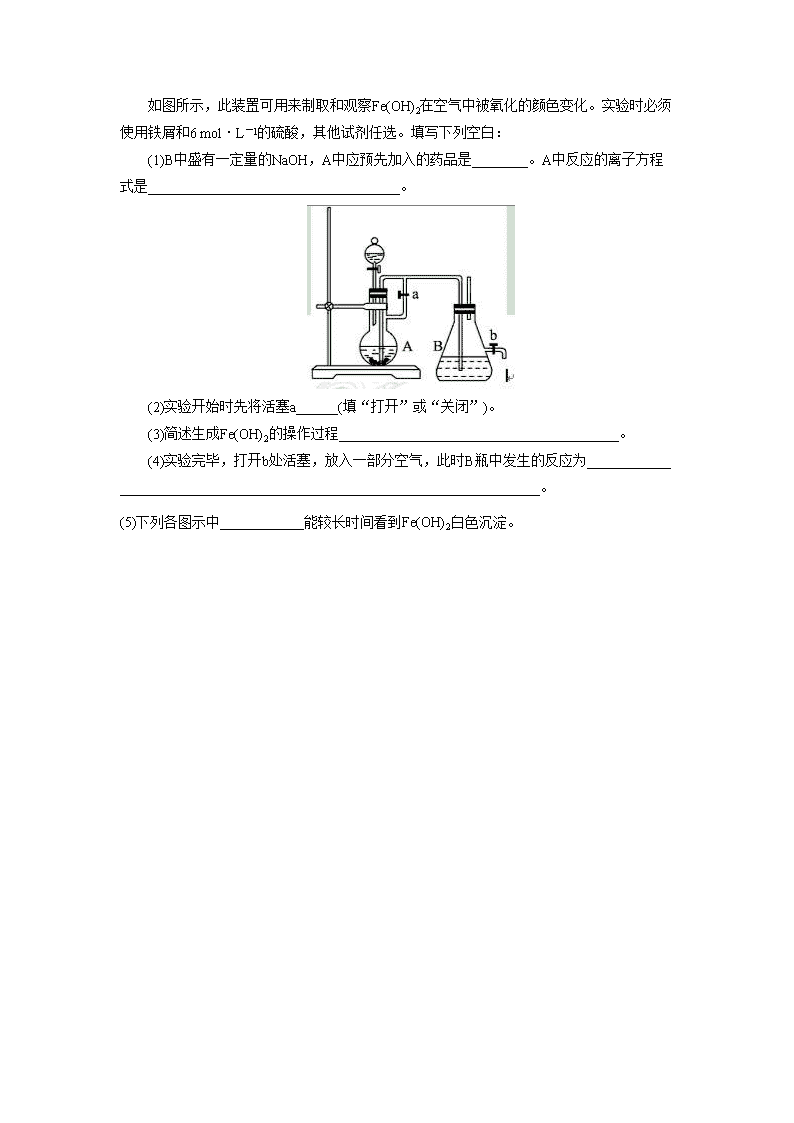
填写下面空白。 (1)图中标号处需加入的相应物质分别是①______________、②______________、③______________、④______________、⑤______________。 (2)写出①处发生反应的离子方程式:________________________;写出③处发生反应的化学方程式:________________________。 (3)铁红的化学式为__________________;分别写出铁红和氧化铜在工业上的一种主要用途:铁红________________________;氧化铜______________________。 二、Fe2+、Fe3+的鉴别方法 1.直接观察颜色 Fe3+的溶液呈棕黄色,Fe2+的溶液呈浅绿色。 2.利用显色反应 3.利用铁化合物沉淀的颜色 有关反应式:Fe2++2OH-===Fe(OH)2↓ 4Fe(OH)2+2H2O+O2===4Fe(OH)3 Fe3++3OH-===Fe(OH)3↓ 4.利用Fe3+的氧化性 (1) 有关离子反应式:2Fe3++Cu===2Fe2++Cu2+ (2) 有关离子反应式:2Fe3++2I-===2Fe2++I2 5.利用Fe2+的还原性 (1) 有关离子反应式:5Fe2++MnO+8H+===5Fe3++Mn2++4H2O (2) 有关离子反应式:2Fe2++Br2===2Fe3++2Br- 【例2】 (2011·广东惠州一次调研)某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色,一位同学由此得出该催化剂中铁元素价态为+3价的结论。 (1)请指出该结论是否合理并说明理由______________________________。 (2)请完成对铁元素价态的探究。限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹;3 mol·L-1 H2SO4、3% H2O2、6 mol·L-1 HNO3、0.01 mol·L-1 KMnO4、NaOH稀溶液、0.1 mol·L-1 KI、20% KSCN、蒸馏水。 ①提出合理假设 假设1:催化剂中铁元素的价态为+3价; 假设2:催化剂中铁元素的价态为+2价; 假设3:____________________________________________________________。 ②设计实验方案证明你的假设(此题不作答) ③实验过程 根据②的实验方案,进行实验。按下表格式写出实验操作步骤、预期现象与结论。 实验操作 预期现象与结论 步骤1: 步骤2: 步骤3: …… 实验与探究 Fe(OH)2的制备 因Fe(OH)2在空气中易被氧化,4Fe(OH)2+O2+2H2O===4Fe(OH)3,故Fe(OH)2在水中稳定存在的寿命只有几秒钟,在实验室制取Fe(OH)2时,一定要用新制的亚铁盐和先加热驱赶掉O2的NaOH溶液,且滴管末端要插入试管内的液面以下,再滴加NaOH溶液,也可以在反应液面上滴加植物油或苯等物质进行液封,以减少Fe(OH)2与O2的接触。 关于Fe(OH)2制备的方法很多,核心问题有两点,一是溶液中的溶解氧必须除去,二是反应过程必须与O2隔绝。 实验典例 如图所示,此装置可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-l的硫酸,其他试剂任选。填写下列空白: (1)B中盛有一定量的NaOH,A中应预先加入的药品是________。A中反应的离子方程式是____________________________________。 (2)实验开始时先将活塞a______(填“打开”或“关闭”)。 (3)简述生成Fe(OH)2的操作过程________________________________________。 (4)实验完毕,打开b处活塞,放入一部分空气,此时B瓶中发生的反应为________________________________________________________________________。 (5)下列各图示中____________能较长时间看到Fe(OH)2白色沉淀。查看更多