- 2021-04-21 发布 |
- 37.5 KB |
- 15页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
浙江省学选考化学2019届高三二轮复习27题对题复习课件(15张)
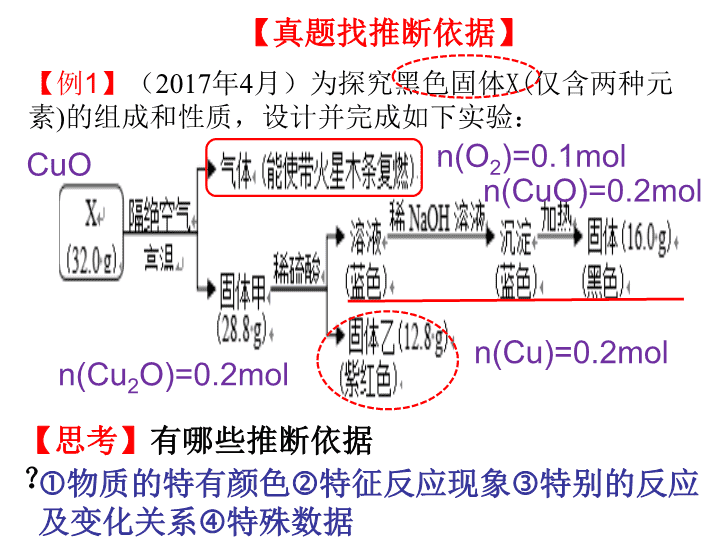
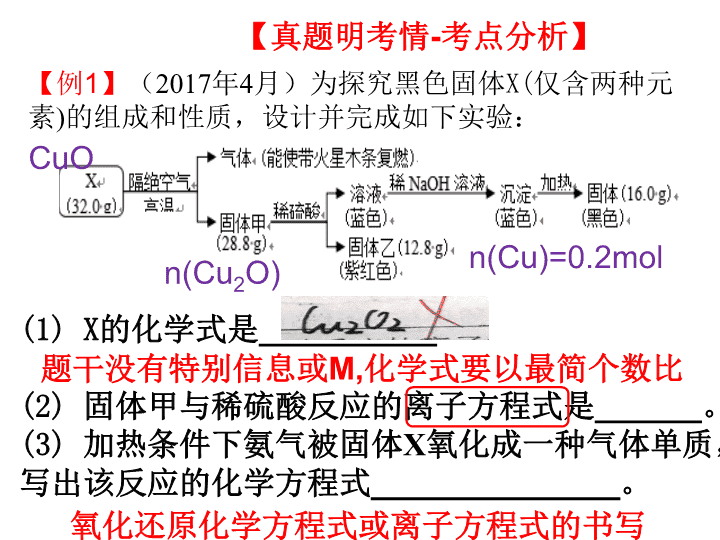
27题之无机物定性定量推断 【真题找推断依据】 【例 1 】 ( 2017 年 4 月)为探究黑色固体 X( 仅含两种元素 ) 的组成和性质,设计并完成如下实验: 【思考】 有哪些推断依据? n(Cu)=0.2mol n(CuO)=0.2mol n(Cu 2 O)=0.2mol n(O 2 )=0.1mol CuO 物质的特有颜色 特征反应现象 特别的反应 及变化关系 特殊数据 【真题明考情 - 考点分析】 【例 1 】 ( 2017 年 4 月)为探究黑色固体 X( 仅含两种元素 ) 的组成和性质,设计并完成如下实验: n(Cu)=0.2mol n(Cu 2 O) CuO (1) X 的化学式是 __________ (2) 固体甲与稀硫酸反应的离子方程式是 ______ 。 (3) 加热条件下氨气被固体 X 氧化成一种气体单质,写出该反应的化学方程式 ______________ 。 题干没有特别信息或 M, 化学式要以最简个数比 氧化还原化学方程式或离子方程式的书写 【例 2 】 ( 2017 年 11 月)已知固体 Na 2 SO 3 受热易分解,实验流程和结果如下: 气体 Y 是一种纯净物,在标准状况下的密度为 1.518g · L - 1 ( 1 )气体 Y 分子的电子式 _______ , ( 2 )该流程中的 Na 2 SO 3 受热分解的化学方程式 ____________________________________ 。 ( 3 )另取固体 X 试样和 Na 2 SO 3 混合,加水溶解后与稀盐酸反应,有淡黄色沉淀产生,写出产生淡黄色沉淀的离子方程式 ___________________________________ 。 写出 H 2 O 2 N 2 H 4 的电子式 2S 2- +SO 3 2- +6H + =3S↓ +3H 2 O 【归纳】熟悉常见物质的摩尔质量 【例 3 】 (2018 年 4 月 ) 某同学用含 结晶水的正盐 X( 四种短 周期元素组成的纯净物 ) 进行了如下实验: 实验中观测到:混合气甲呈无色并被蒸馏水全部吸收;固体 乙为纯净物 ;在步骤 ③ 中, 取 1/ 10 溶液丙 ,恰好中和需消耗 0.00200 mol NaOH ;另取一定量的溶液丙,加入少量 K 2 FeO 4 固体,产生 黄绿色 气体。 n(HCl)=0.02mol n(H 2 O)=0.05mol (1) X 的化学式是 __ ,步骤 ① 的化学方程式是 __________ 。 (2) 溶液丙与 K 2 FeO 4 固体反应的化学方程式是 _ 。 n(MgO)=0.01mol 2K 2 FeO 4 + 16HCl=4KCl + 2FeCl 3 + 3Cl 2 ↑ + 8H 2 O 【考点归纳】 根据题给信息定性和定量结合推 断元素化合物的组成。 (1)电子式、结构(简)式等化学用语规范书写。 (2)化学方程式的书写技能:电离方程式、水解方程式、电极方程式、结合信息分析推理陌生反应的化学(离子)反应方程式; ( 3 )常见物质(离子)的检验方法,实验方案设 计及现象描述、结论分析。 熟记钠镁铁铜及其化合物的性质及主要用途,碳、氮、氧、硅、硫、氯等非金属及其化合物的相互转化关系。 黄色固体 蓝色沉淀 淡黄色固体 蓝色晶体 红色固体 浅绿色溶液 紫黑色固体 紫色溶液 红棕色粉末 棕黄色溶液 黑色粉末 血红色溶液 红褐色沉淀 红棕色气体 白色沉淀 黄绿色气体 Cl 2 AgI , FeS 2 S 、 Na 2 O 2 、 AgBr Cu 、 Cu 2 O KMnO 4 、 I 2 Fe 2 O 3 MnO 2 、 Fe 3 O 4 、 CuO 、 C Fe(OH) 3 BaSO 4 、 BaCO 3 、 CaCO 3 、 AgCl 、 Cu(OH) 2 CuSO 4 Fe 2+ MnO 4 - Fe 3+ Fe(SCN) 3 NO 2 7 物质推断解题突破口之 物质特有的颜色 某化合物甲是制备负载型催化剂的主要原料。经组成分析化合物 甲中含有四种元素 。 气体混合物乙仅含两种元素,由丁和戊组成,其中丁占总体积的 2/3 , 密度为 1.25g · L - 1 。戊能使澄清石灰水变浑浊。 n(CO)=0.06mol n(CO 2 )=0.03mol m( 气 )=3.00g n(Fe 2 O 3 )=0.01mol m(K 2 CO 3 )=4.14g n(K 2 CO 3 )=0.03mol (1) 化合物甲的化学式________ K 3 [Fe(C 2 O 4 ) 3 ] 或 K 3 FeC 6 O 12 (2) 加热化合物甲使其完全分解的化学方程式为 __________________________________________ 。 2K 3 [Fe(C 2 O 4 ) 3 ] = 3K 2 CO 3 + Fe 2 O 3 + 6CO + 3CO 2 ; 5 题 为探究含结晶水的化合物 X( 含四种元素,摩尔质量为 180 g·mol - 1 ) 的组成和性质,某兴趣小组设计并完成如图所示实验: n(FeO)=0.15mol n(CO 2 )=0.15mol n(CO)=0.15mol FeC 2 O 4 2H 2 O n(H 2 O)=0.3mol 1 . (2018· 浙江金华一中月考 ) 某研究小组为了探究一种浅绿色盐 X[ 仅含四种元素,不含结晶水, M (X) < 908 g·mol - 1 ] 的组成和性质,设计并完成了如下实验: 取一定量的浅绿色盐 X 进行上述实验,充分反应后得到 23.3 g 白色沉淀 E 、 28.8 g 红色固体 G 和 12.8 g 红色固体 H 。 ① 浅绿色盐 X 在 570 ℃ 、隔绝空气条件下受热分解为非氧化还原反应; ② 常温下 B 呈液态且 1 个 B 分子含有 10 个电子 。 n(SO 3 )=0.1mol n(Cu 2 O)=0.2mol 第 2 题和讲义第五题 2 、特征反应现象 【讲义 4 】 为探究无机盐 X (仅含 三种短周期元素 )的组成和性质,设计并完成如下实验:请回答: n(SiO 2 )=0.03mol n(Mg(OH) 2 ) =0.06mol ( 3 )高温条件下白色粉末与焦炭发生置换反应,写出该反应的化学方程式 ______ SiO 2 +2C==Si+2CO 高温 注意几个特殊的置换反应: ( 2 )金属 → 非金属 ( 3 )非金属 → 非金属 ( 4 )非金属 → 金属 ( 1 )金属 → 金属 既能跟酸反应又能跟碱反应且生成气体的物质是 Al 、 NH 4 HCO 3 、 (NH 4 ) 2 CO 3 【讲义 7 】 某研究小组为了探究仅一种白色粉末状固体 X( 仅含四种元素 ) 的组成和性质,称取 6.3g 固体 X ,设计并完成了如下实验: n(NH 3 )=0.1mol n(CO 2 )=0.1mol n(Cu 2 O)=0.1mol HCOONa 物质推断中新型方程式书写 ( 1 )某短周期元素组成的金属氢化物可与水反应产生氢气和能溶于 NaOH 的白色沉淀,写出该 金属氢化物与水 反应的化学方程式 。 ( 2 )已知: NH 2 Cl 与水可以微弱地反应产生具有漂白性的物质,因而 NH 2 Cl 具有消毒时间长等优点,写出该反应的化学方程式 。 ( 3 )在空气中直接加热 CuCl 2 •2H 2 O 晶体得不到纯的无水 CuCl 2 ,原因是 。(用化学方程式表示) 例 1 例 2 ( 1 )以 KI 作为加碘剂的食盐在保存过程中,由于空气中氧气的作用,容易引起碘的损失。写出潮湿环境下 KI 与氧气反应的化学方程式 。 ( 2 )在通气良好的土壤中,土壤中 NH 4 + 的氧化途径之一是在硝酸细菌作用下完成,写出反应的离子方程式 。 ( 3 )工业上一般采用电解(惰性电极) K 2 MnO 4 溶液制 KMnO 4 ,写出电解总反应方程式 。查看更多