- 2021-04-20 发布 |
- 37.5 KB |
- 3页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020高考化学二轮增分策略 必考选择题专练(二)化学能与热能
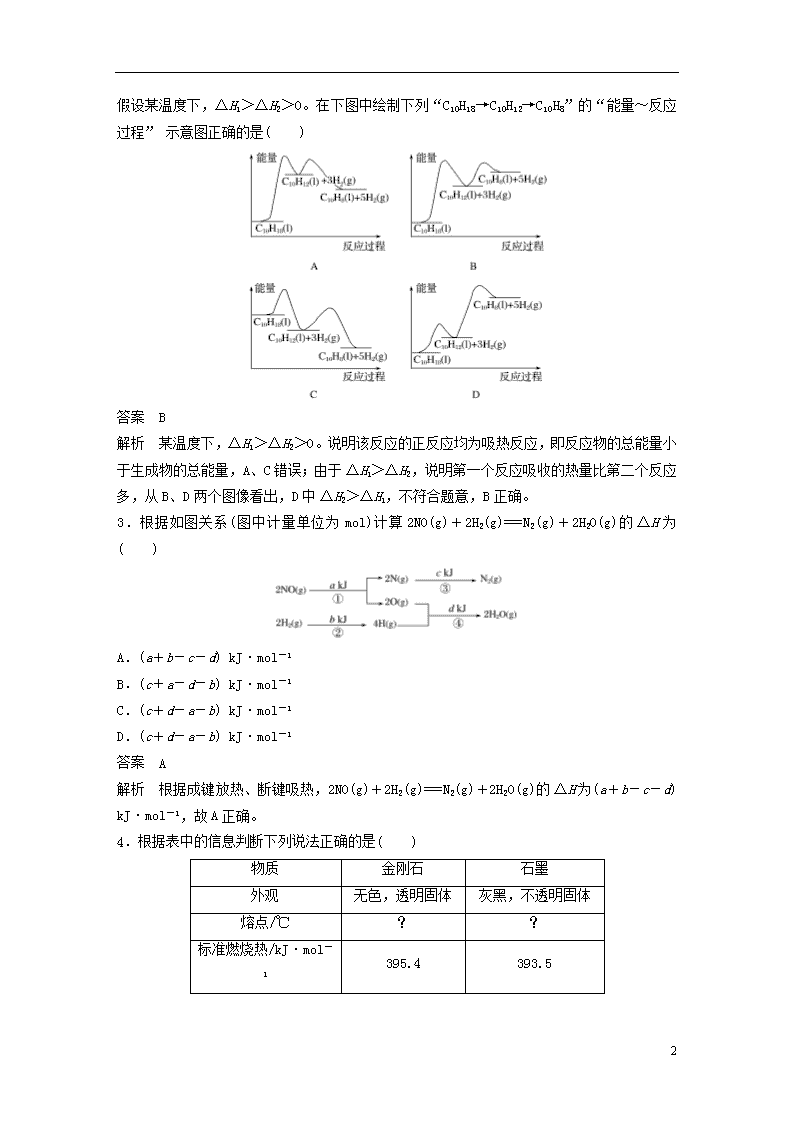
必考选择题专练(二) 化学能与热能 1.已知某化学反应A2(g)+2B2(g)===2AB2(g)(AB2的分子结构为B—A—B)的能量变化如图所示,下列有关叙述中正确的是( ) A.该反应是放热反应 B.该反应的ΔH=-(E1-E2) kJ· mol-1 C.该反应中反应物的键能总和大于生成物的键能总和 D.由2 mol A(g)和4 mol B(g)形成4 mol A—B键吸收E2 kJ能量 答案 C 解析 根据图示,反应物的总能量小于生成物的总能量,该反应是吸热反应,故A错误;该反应的ΔH=(E1-E2) kJ· mol-1,故B错误;焓变=反应物的键能总和-生成物的键能总和,焓变大于0,故C正确;由2 mol A(g)和4 mol B(g)形成4 mol A—B键放出E2 kJ能量,故D错误。 2.十氢萘是具有高储氢密度的氢能载体,经历“十氢萘(C10H18)→四氢萘(C10H12)→萘(C10H8)”的脱氢过程释放氢气。已知: Ⅰ.C10H18(l)===C10H12(l)+3H2(g) ΔH1 Ⅱ.C10H12(l)===C10H8(l)+2H2(g) ΔH2 3 假设某温度下,ΔH1>ΔH2>0。在下图中绘制下列“C10H18→C10H12→C10H8”的“能量~反应过程” 示意图正确的是( ) 答案 B 解析 某温度下,ΔH1>ΔH2>0。说明该反应的正反应均为吸热反应,即反应物的总能量小于生成物的总能量,A 、C错误;由于ΔH1>ΔH2,说明第一个反应吸收的热量比第二个反应多,从B、D两个图像看出,D中ΔH2>ΔH1,不符合题意,B正确。 3.根据如图关系(图中计量单位为mol)计算2NO(g)+2H2(g)===N2(g)+2H2O(g)的ΔH为( ) A.(a+b-c-d) kJ·mol-1 B.(c+a-d-b) kJ·mol-1 C.(c+d-a-b) kJ·mol-1 D.(c+d-a-b) kJ·mol-1 答案 A 解析 根据成键放热、断键吸热,2NO(g)+2H2(g)===N2(g)+2H2O(g)的ΔH为(a+b-c-d) kJ·mol-1,故A正确。 4.根据表中的信息判断下列说法正确的是( ) 物质 金刚石 石墨 外观 无色,透明固体 灰黑,不透明固体 熔点/℃ ? ? 标准燃烧热/kJ·mol-1 395.4 393.5 3 A.表示石墨燃烧热的热化学方程式为C(石墨,s)+O2(g)===CO(g) ΔH=-393.5 kJ·mol-1 B.由表中信息知C(石墨,s)===C(金刚石,s) ΔH=1.9 kJ·mol-1 C.由表中信息可得如图所示的图像 D.由表中信息可推知相同条件下金刚石的熔点高于石墨的 答案 B 解析 根据燃烧热的定义知C(石墨,s)+O2(g)===CO2(g) ΔH=-393.5 kJ·mol-1,C(金刚石,s)+O2(g)===CO2(g) ΔH=-395.4 kJ·mol-1,A项错误;由石墨和金刚石燃烧热的热化学方程式可知,B项正确;图像是错误的,1.9 kJ·mol-1表示金刚石和石墨之间的能量差,而不是金刚石转化为石墨的反应过程中的中间产物与石墨的能量差,C项错误;等物质的量的石墨比金刚石的能量低,能量越低越稳定,因此石墨中碳碳键的键能应大于金刚石中碳碳键的键能,所以石墨的熔点应高于金刚石的,D项错误。 3查看更多