- 2024-05-31 发布 |
- 37.5 KB |
- 30页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
北京专版2020中考化学复习方案实验突破07实验室制取气体课件
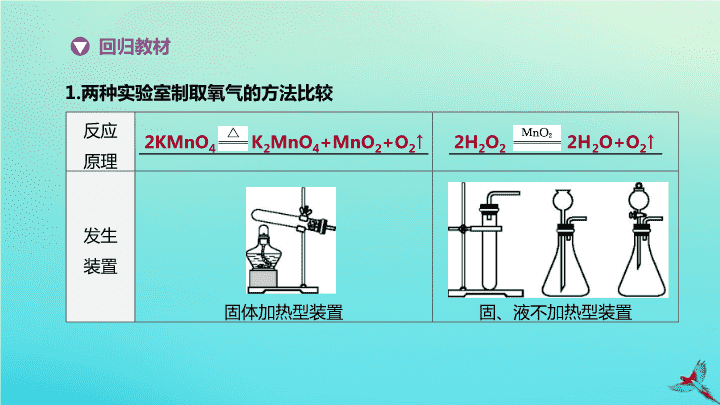
实验突破 ( 七 ) 实验室制取气体 反应 原理 ______________________________________ ____________________________ 发生 装置 固体加热型装置 固、液不加热型装置 回归教材 1. 两种实验室制取氧气的方法比较 2KMnO 4 K 2 MnO 4 +MnO 2 +O 2 ↑ 2H 2 O 2 2H 2 O+O 2 ↑ 反应 类型 分解反应 收集 方法 排水法或向上排空气法 验满 方法 将 带火星的木条放在 , 若木条复燃 , 证明氧气已经收集满 ( 用向上排空气法收集时 ) 检验 方法 将 带火星的木条 , 若木条复燃 , 证明是氧气 (续表) 集气瓶瓶口 伸入集气瓶中 2. 实验室制取二氧化碳 实验原理 在 实验室里 , 二氧化碳通常用大理石 ( 或石灰石 ) 和稀盐酸反应来制取 , 反应的化学方程式为 实验装置 CaCO 3 +2HCl CaCl 2 +CO 2 ↑ +H 2 O 操作步骤 ① 查 : 连接好仪器 , 并检查装置的气密性 装置 b 气密性检查的方法 : ____________________________________________ ② 装 : 先装大理石 ( 或石灰石 ), 再加稀盐酸 ③ 收 : 收集二氧化碳 ④ 验 : 验满二氧化碳 (续表) 用弹簧夹夹紧胶皮管 , 向长颈漏斗中注水 , 长颈漏斗的下端形成一段水柱 , 若一段时间后 , 水柱既不上升也不下降 , 则装置的气密性良好 (续表) 检验及 验满 ① 检验方法 : 将气体 , 若 , 证明生成的气体是二氧化碳 ② 验满方法 : 将 , 如果 , 证明气体已收集满 通入澄清石灰水中 石灰水变浑浊 燃着的木条靠近集气瓶口 木条熄灭 装置改进 及评价 其 优点分别是 : ① ② ③ ④ (续表) 装置简单 , 操作方便 可随时添加液体药品 可控制反应速率 可控制反应的发生和停止 实验反思 不 选择以下物质相互反应生成二氧化碳的原因 : ① 碳在氧气中燃烧 ____________________________________________________ ② 碳酸钠粉末与稀盐酸反应 _______________ ③ 大理石 ( 或石灰石 ) 与稀硫酸 反应 __________________________________________ ④ 大理石 ( 或石灰石 ) 与浓盐酸 反应 ______________________________________________ ________ (续表) 反应速率太快 , 不易控制反应速率和收集气体 生成微溶的硫酸钙覆盖在大理石 ( 或石灰石 ) 表面 , 阻止反应进一步进行。 浓盐酸具有挥发性 , 使收集到的二氧化碳不纯 生成的二氧化碳中可能混有其他气体 , 且不易收集 3. 实验室制备气体的一般思路和方法 (1) 发生装置 类型 固体加热型 固液常温型 装置 (续表) 优缺点 或注意 试管 口应略向下倾斜 便于 添加液体药品 , 长颈漏斗应伸到液面以下 , 防止气体从长颈漏斗逸出 可以 控制反应速率 可以 控制反应的发生与停止 (2) 收集装置 类型 排水法 向上排空气法 向下排空气法 装置 (续表) 类型 排水法 向上排空气法 向下排空气法 适用 范围 收集 不易 ( 或难 ) 溶于水且不与水反应的气体 收集 密度比空气 ( 略 ) 大且不与空气中成 分发生 反应的气体 收集 密度比空气小且不与空气中成分发生反应的气体 优缺 点或 注意 收集 的气体纯度高 , 但不干燥 ; 集气瓶应装满水 , 导管口气泡连续均匀冒出时方可收集 收集 的气体干燥 , 但纯度不高 ; 导管应伸到集气瓶底部 , 便于排出集气瓶内的空气 1. [2017 · 北京节选 ] 高锰酸钾在生产、生活中有广泛应用。实验小组对高锰酸钾的某些性质进行研究。 Ⅰ. 不稳定性 (1) 如图 S7-1 所示进行实验 , 受热分解的化学方程式为 _________________________ 。 (2) 用向上排空气法收集氧气的原因是 ____________________________________ ____________________ 。 拓展训练 图 S7-1 2KMnO 4 K 2 MnO 4 氧气密度大于空气的密度 , 且不与空气中其他成分反应 +MnO 2 +O 2 ↑ 2. [2019 · 西城期末 ] 实验室用图 S7-2 装置制取氧气。 (1) 仪器 a 的名称是 。 (2) 用高锰酸钾制取氧气的化学方程式是 。 (3) 能用排水法收集氧气的原因是 。 (4) 若收集到的氧气不纯 , 可能的原因是 _______________________________________ ( 答 1 条即可 ) 。 图 S7-2 试管 2KMnO 4 K 2 MnO 4 +MnO 2 +O 2 ↑ 氧气不易溶于水且不与水反应 导管口有气泡冒出时 , 立即开始收集 ( 合理即可 ) 3. [2018 · 北京 ] 实验室用图 S7-3 装置制取 CO 2 。 (1) 反应的化学方程式为 。 (2) 用向上排空气法收集 CO 2 的原因是 _______________________________________ 。 图 S7-3 CaCO 3 +2HCl CaCl 2 +H 2 O+CO 2 ↑ CO 2 的密度比空气大且不与空气中的 其他气体发生反应 4. [2019 · 海淀一模 ] 实验室用图 S7-4 所示装置制取 CO 2 。 (1) 反应的化学方程式为 。 图 S7-4 [ 答案 ] (1)CaCO 3 +2HCl CaCl 2 +H 2 O+CO 2 ↑ [ 解析 ] (1) 在实验室中常用大理石或石灰石 ( 主要成分是碳酸钙 ) 与稀盐酸反应制二氧化碳 , 同时生成氯化钙和水 , 化学方程式为 CaCO 3 + 2HCl CaCl 2 +H 2 O+CO 2 ↑。 4. [2019 · 海淀一模 ] 实验室用图 S7-4 所示装置制取 CO 2 。 (2) 检验 CO 2 是否集满的操作为 。 图 S7-4 [ 答案 ] (2) 将燃着的木条放在集气瓶口 [ 解析 ] (2) 二氧化碳不燃烧也不支持燃烧 , 所以验满二氧化碳时可将燃着的木条放在集气瓶口 , 观察木条是否熄灭。 5. 某气体常温下不与空气中的成分反应 , 密度比空气小 , 极易溶于水 , 以下收集该气体的方法正确的是 。 图 S7-5 B 6. 某科学兴趣小组为了研究物质燃烧的剧烈程度与氧气浓度的关系 , 需要收集一瓶大约含空气的氧气 , 下列操作能达到此目的的是 。 图 S7-6 B 7. [2016 · 北京节选 ] 利用表中装置进行下列实验。 (1) 实验中 , 瓶内发生反应的化学方程式为 ; 步骤 Ⅲ 中 , 关闭 K 后的现象是 。 实验装置 实验 Ⅰ. 将盛有足量锌粒的燃烧匙伸入瓶中 , 塞紧瓶塞 Ⅱ. 打开 K, 从长颈漏斗向瓶内加入稀盐酸 , 至浸没锌粒 Ⅲ. 当瓶中产生大量气泡时 , 关闭 K Zn+2HCl ZnCl 2 +H 2 ↑ 瓶内液面缓慢下降 , 长颈漏斗中的液面上升 , 最后反应停止 8. [2017 · 北京节选 ] 利用如下装置进行实验 ( 两支玻璃管内径相同 ) 。实验前 K 1 、 K 2 、 K 3 均已关闭。 (1) 实验 1: 锌与稀硫酸反应的化学方程式为 ; 为使反应停止 ,Ⅲ 中的操作是 。 实验装置 实验 1: 制备气体 左 管中带孔的燃烧匙盛有足量锌粒 , 右管盛有稀硫酸 Ⅰ. 打开 K 1 和 K 2 , 使反应发生 Ⅱ. 在 K 1 的导管口处收集气体 Ⅲ. …… [ 答案 ] (1)Zn+H 2 SO 4 ZnSO 4 +H 2 ↑ 关闭 K 1 [ 解析 ] (1) 锌与稀硫酸反应生成硫酸锌和氢气 , 反应的化学方程式为 Zn+H 2 SO 4 ZnSO 4 +H 2 ↑ ; 欲使反应停止 , 可关闭左侧玻璃管上方的 K 1 , 左侧不断产生气体 , 使管内压强变大 , 固液分离 , 反应停止。 9. 利用表中装置进行实验。实验前 K 1 、 K 2 、 K 3 均已关闭。 实验中 , 锌与稀硫酸反应的化学方程式为 ; 气体收集完毕后 , 在不拆卸装置的情况下 , 使 A 中未反应的稀硫酸大部分转移到 B 中的操作是 。 内容 装置 实验 : 制备气体 Ⅰ. 打开 K 1 , 用注射器向盛有锌粒的 A 中注入稀硫酸 , 直至液面浸没下端导管口 ; Ⅱ. 在 K 1 上方导管口收集气体 [ 答案 ] (1)Zn+H 2 SO 4 ZnSO 4 +H 2 ↑ 打开 K 2 、 K 3 , 关闭 K 1 [ 解析 ] 锌与稀硫酸反应生成硫酸锌和氢气 ; 打开 K 2 、 K 3 , 关闭 K 1 , 导致装置 A 中气体压强增大 , 稀硫酸被气体压入装置 B 中。 10. 利用如图 S7-7 所示装置可以进行氯化氢制备和性质检验一体化实验。实验过程如下 : (1) 检查装置气密性良好。 (2) 制备氯化氢。加热浓硫酸与 氯化钠固体发生复分解反应制 氯化氢气体 , 该反应的化学方程 式是 ________________________ 。 图 S7-7 H 2 SO 4 ( 浓 )+2NaCl Na 2 SO 4 +2HCl ↑ 10. 利用如图 S7-7 所示装置可以进行氯化氢制备和性质检验一体化实验。实验过程如下 : (3) 收集氯化氢。需要打开 a 使 浓硫酸流入 1 号烧瓶 , 同时打开 ( 填“ b ”“ c ”或“ d ” ), 关闭 ( 填“ b ”“ c ”或 “ d ” ) 。当观察到 __________ 时 , 说明 2 号烧瓶内氯化氢气体已收集 满 , 立即关闭 b 、 d, 同时打开 c 。 图 S7-7 bd c 烧杯中紫 色石蕊溶液变为红色 10. 利用如图 S7-7 所示装置可以进行氯化氢制备和性质检验一体化实验。实验过程如下 : (4) 将注射器中的水注入 2 号烧 瓶中 , 片刻后打开 d, 可以观察到 2 号烧瓶中出现红色的“喷泉” , 请解释“喷泉”形成的原因 : _____________________________ _____________________________ __________________ 。 (5) 集气瓶口醮有浓 NaOH 溶液的棉花的作用是 。 图 S7-7 由于氯化氢易溶于水 , 使 2 号烧瓶内气体减少 , 使瓶内压强小于外界大气压 吸收氯化氢 , 减少环境污染 11. 为研究实验室制取二氧化碳的适宜条件 , 进行如下实验。 (1) 大理石与盐酸反应的化学方程式为 。 (2) 实验甲与 对照 , 是为了研究固体反应物颗粒大小对反应速率的影响。 (3) 上述实验中 , 另一个影响反应速率的因素是 。 实验 编号 药品 甲 乙 丙 丁 1 g 大理石 块状 块状 粉末状 粉末状 10 g 盐酸 ( 过量 ) 稀盐酸 浓盐酸 稀盐酸 浓盐酸 CaCO 3 +2HCl CaCl 2 +H 2 O+CO 2 ↑ 丙 盐酸的浓度 拓展阅读 多功能瓶的使用 类型 收集气体 检验、干燥、除杂 检验、吸收并集气 排空气法 排水法 装置 (续表) 注意 用 A 装置收集密度比空气大的气体时 , 气体应从 a 端通入 ; 收集密度比空气小的气体时 , 气体应从 b 端通入 ;B 装置气体进出口顺序与之相反 实验 时应先在瓶中装满水 , 将气体从 f 端通入。如果将排出的水引入量筒中 , 利用此装置还可以测量反应产生的气体体积 用 此装置吸收或检验气体时 , 应将气体从 g 端通入 , 可以简记为“长进短出” 装置 综合性较强 , 如将 CO 和少量 CO 2 混合气体缓缓通入饱和石灰水中 , 石灰水检验并吸收 CO 2 ,CO 贮存在集气瓶内查看更多
相关文章
您可能关注的文档
- 北京专版2020中考化学复习方案实验突破07实验室制取气体课件
- 【生物】2019届一轮复习人教版第6单元第1讲DNA是主要的遗传物质考点
- 河北省正定中学2019-2020学年高二3月月考政治试题
- 2020秋部编版小学语文一年级上册拼音与汉字专项练习及答案 共三套
- 2017-2018学年河南省林州市第一中学高二上学期末期考试化学试题(火箭班) 解析版
- 2020会计述职报告
- 一年级上册数学试题-第四单元测试卷-人教版(word,含答案)
- 2020年八年级物理下册大气压与人类生活
- 班主任工作范文之班级管理案例分析--把不好的事情消灭在萌芽之春
- 2篇2020年党委书记在全国两会精神专题学习会上研讨发言心得交流(党课讲稿)