- 2023-04-14 发布 |
- 37.5 KB |
- 17页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
北京专版2020中考化学复习方案实验突破10认识溶液的组成课件
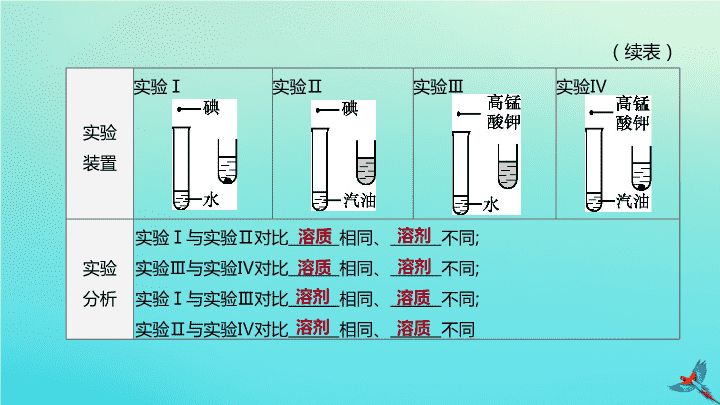
实验突破 ( 十 ) 认识溶液的组成 回归教材 实验仪器及药品 试管、碘、高锰酸钾、水、汽油 实验操作 向 两支试管中各加入 1~2 小粒碘 , 然后分别加入 5 mL 水和 5 mL 汽油 , 振荡 另 取两支试管各加入 1~2 小粒高锰酸钾 , 然后分别加入 5 mL 水和 5 mL 汽油 , 振荡 实验 装置 实验 Ⅰ 实验 Ⅱ 实验 Ⅲ 实验 Ⅳ 实验 分析 实验 Ⅰ 与实验 Ⅱ 对比 相同、 不同 ; 实验 Ⅲ 与实验 Ⅳ 对比 相同、 不同 ; 实验 Ⅰ 与实验 Ⅲ 对比 相同、 不同 ; 实验 Ⅱ 与实验 Ⅳ 对比 相同、 不同 (续表) 溶质 溶剂 溶质 溶剂 溶剂 溶质 溶剂 溶质 实验 结论 实验 反思 (1) 设计实验 Ⅰ 、 Ⅱ 的目的 是 ___________________________________________ ; 设计实验 Ⅰ 、 Ⅲ 的目的 是 ____________________________ (2) 对比实验 Ⅲ 、 Ⅳ 可得出的结论 是 _____________________________________ (续表) 同一种物质在不同的溶剂中溶解性是不同的 , 不同的物质在同一溶剂中的溶解性也是不同的 在同等一定条件下 , 比较溶质碘在溶剂水和 在同等一定条件下 , 比较溶 汽油中的溶解性 质碘和溶质高锰酸钾在溶剂水中的溶解性 在同等一定条件下 , 高锰酸钾在溶剂 水中的溶解性强于在溶剂汽油中的溶解性 1. [2019 · 北京节选 ] 如图 S10-1, 在一只烧杯中进行实验。补全实验方案。 拓展训练 图 S10-1 目的 步骤 验证 KCl 不能无限溶解 20 ℃ 时 ① 加入 100 g 水 ;② 加入 18 g KCl;③ 加入 ____________________ ( 已知 :20 ℃ 时 ,KCl 的溶解度为 34 g) 20 g ( 大于 16 g 即可 ) KCl 固体 2. [2016 · 北京 ] 为了研究物质的溶解现象 , 设计并进行了如下表实验 : (1) 对比实验 ①② 的现象 , 可得出的结论是 _____________________________________ 。 (2) 设计实验 ②③ 的目的是 __________________________________________________ 。 1 小粒高锰酸钾在水中的溶解能力比 实验 现象 固体 溶解 , 形成紫色溶液 固体几乎不溶解 固体 溶解 , 形成紫红色溶液 比较 1 小粒高锰酸钾和 1 小粒碘在 5 mL 汽油中的 在汽油中的溶解能力强 溶解能力 3. 为了研究物质的溶解现象 , 设计并进行了如下实验。 (1) 实验一的目的是 。 (2) 实验二 , 加热后固体全部消失的原因是 ____________________________________ 。 比较 1 小粒高锰酸钾在 5 mL 水和 5 mL 汽油中的溶解能力 图 S10-2 硝酸钾的溶解度随温度的升高而 增大 4. [2019 · 朝阳一模 ] 探究影响物质溶解性的因素。 (1) 实验 1 的目的是探究 对碳酸钠溶解性的影响。 图 S10-3 [ 答案 ] (1) 温度 [ 解析 ] (1) 实验 1, 对试管进行了加热 , 目的是探究温度对碳酸钠溶解性的影响。 4. [2019 · 朝阳一模 ] 探究影响物质溶解性的因素。 (2) 实验 2 可获得的结论是 。 图 S10-3 [ 答案 ] (2)1 g Na 2 CO 3 在 10 mL 水中的溶解能力比在 10 mL 酒精中强 , 溶剂的种类是影响物质溶解性的因素 [ 解析 ] (2) 实验 2, 溶质种类相同 , 溶剂种类不同 , 由碳酸钠在水和酒精中的溶解情况 , 可得出溶剂的种类是影响物质溶解性的因素。 5. [2019 · 石景山二模 ] 向 5 个烧杯的液体中分别加入固体充分溶解 , 结果如图 S10 -4 所示。 (1)A 溶液一定是 ( 填 “饱和”或“不饱和” ) 溶液。 图 S10-4 [ 答案 ] (1) 不饱和 [ 解析 ] (1)A 、 B 两个烧杯中水的体积与温度都相同 ,B 烧杯中放入的 6 g 蔗糖全部溶解 , 所以 A 烧杯中溶解了 2.5 g 蔗糖形成不饱和溶液。 5. [2019 · 石景山二模 ] 向 5 个烧杯的液体中分别加入固体充分溶解 , 结果如图 S10 -4 所示。 (2) 能比较食盐和蔗糖溶解性 强弱的是 ( 填序号 ) 。 图 S10-4 [ 答案 ] (2)B 和 E [ 解析 ] (2)B 、 E 烧杯中水的体积与温度都相同 ,B 烧杯中放入的 6 g 蔗糖全部溶解 , 而 E 烧杯中放入的 4 g 食盐没有完全溶解 , 说明蔗糖在水中的溶解性比食盐在水中的溶解性强。 5. [2019 · 石景山二模 ] 向 5 个烧杯的液体中分别加入固体充分溶解 , 结果如图 S10 -4 所示。 (3) 对比 C 和 D, 得出的结论是 。 图 S10-4 [ 答案 ] (3) 在 20 ℃,10 mL( 或相同体积 ) 溶剂中 , 食盐在水中的溶解性比在酒精中好 [ 解析 ] (3)C 、 D 两个烧杯中的溶剂的温度与体积相同 , 但溶剂的种类不同 , 两个烧杯中均加入 2.5 g 食盐 ,C 烧杯 ( 水 ) 中的 2.5 g 食盐全部溶解 , 而 D 烧杯 ( 酒精 ) 中的 2.5 g 食盐没有全部溶解 , 说明在 20 ℃,10 mL( 或相同体积 ) 溶剂中 , 食盐在水中的溶解性比在酒精中好。 6. [2019 · 朝阳二模 ] 根据下表中的数据和相关实验回答问题。 (1) 实验 A 中的白色固体是 。 图 S10-5 温度 /℃ 溶解度 /g NaOH Ca(OH) 2 10 51 0.176 20 109 0.165 40 129 0.141 60 174 0.116 80 314 0.094 [ 答案 ] (1)NaOH [ 解析 ] (1) 实验 A 加入的固体完全溶解 , 可知该物质的溶解度较大 , 故 A 中的白色固体是 NaOH 。 6. [2019 · 朝阳二模 ] 根据下表中的数据和相关实验回答问题。 (2) 通过实验 B 中溶液是否变浑浊 , 可以鉴别 NaOH 和 Ca(OH) 2 两种饱和溶液的依据是 。 图 S10-5 温度 /℃ 溶解度 /g NaOH Ca(OH) 2 10 51 0.176 20 109 0.165 40 129 0.141 60 174 0.116 80 314 0.094 [ 答案 ] (2) 氢氧化钠的溶解度随温度升高而增大 , 氢氧化钙的溶解度随温度升高而减小 [ 解析 ] (2) 因为氢氧化钠的溶解度随温度升高而增大 , 氢氧化钙的溶解度随温度升高而减小 , 故通过实验 B 中溶液是否变浑浊 , 可以鉴别 NaOH 和 Ca(OH) 2 两种饱和溶液。查看更多