- 2021-06-04 发布 |
- 37.5 KB |
- 4页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2020版高中化学 第1章 认识化学科学 1
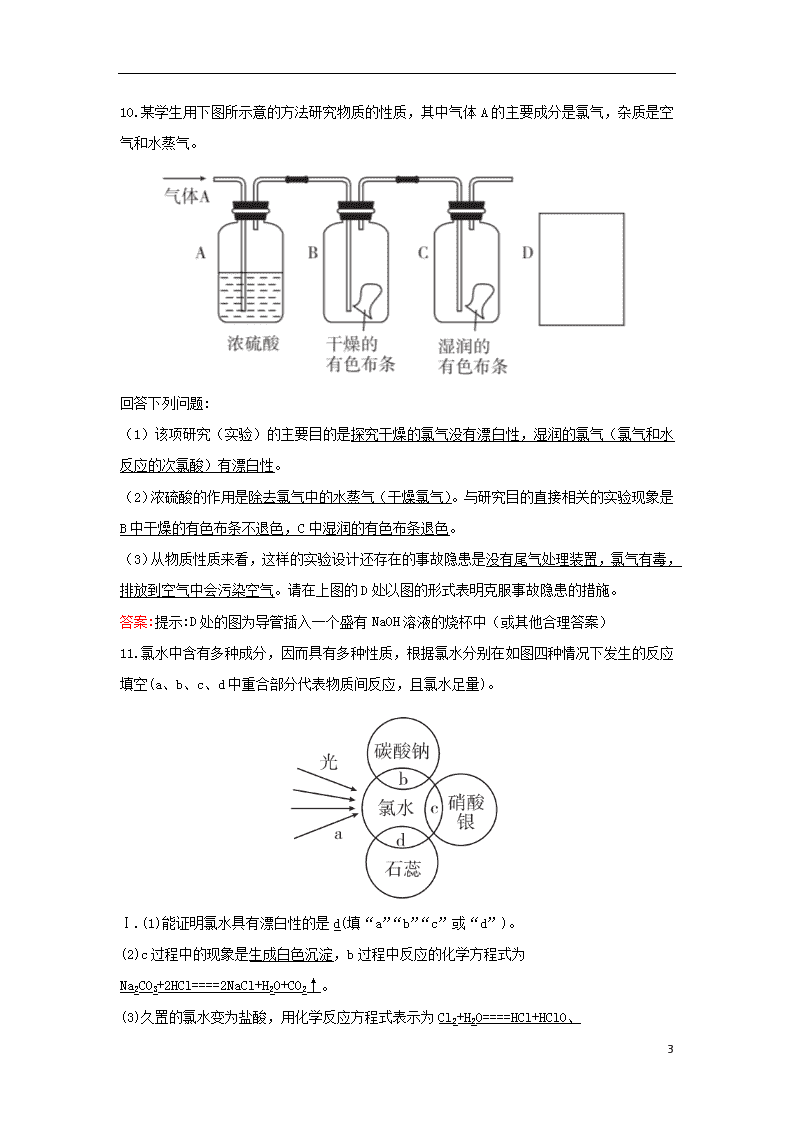
第2课时研究物质性质的基本程序 1.2010年7月27日四川广元发生氯气泄漏,导致多人中毒,作为消防干警,在现场的下列处理方法和过程较合理的是(B) ①及时转移疏散人群,向有关部门如实报告事故有关情况 ②被转移人群应戴上用浓NaOH溶液处理过的口罩③用高压水枪向空中喷洒含碱性物质的水溶液④被转移人群可戴上用肥皂水打湿的口罩⑤将人群转移到地势较低的地方即可,不必走太远⑥及时清理现场,检查水源和食物等是否被污染⑦常温下氯气能溶于水,所以只要向空气中喷洒水就可以解毒 A.②③④⑤ B.①③④⑥ C.①②⑤⑥ D.①③⑤⑦ 2.用自来水(以Cl2为杀菌消毒剂)配制下列物质的水溶液,不会出现明显的药品变质问题的是 (C) A.Na2CO3 B.AgNO3 C.CuSO4 D.NaOH 3.下列有关氯气的叙述中正确的是(B) A.氯气在常温下能与铁反应,故不能用铁罐存放液氯 B.液氯和氯水不是同一物质 C.点燃氢气和氯气的混合气体可以制取氯化氢 D.用氯气对生活用水进行消毒的原因是氯气能杀灭细菌 4.下列说法正确的是(C) A.铁丝在氯气燃烧时生成棕红色烟雾 B.铜丝在氯气中燃烧时生成棕黄色烟,产生CuCl C.向田鼠洞里通入氯气杀灭田鼠,利用了氯气有毒和密度较大的性质 D.铁分别与氯气、盐酸反应时得到相同的氯化物 5.检验氯化氢气体中是否混有Cl2,可采取的方法是(D) A.用干燥的蓝色石蕊试纸 B.用干燥有色布条 C.将气体通入硝酸银溶液 4 D.用湿润的红色布条 6.如图所示:若关闭Ⅰ阀,打开Ⅱ阀,让一种含氯气的气体经过甲瓶后,通入乙瓶,布条不退色;若关闭Ⅱ阀,打开Ⅰ阀再通入这种气体,布条退色。甲瓶中所盛的试剂可能是(D) ①浓硫酸②饱和氯化钠溶液③NaOH溶液 ④少量碳酸氢钠溶液 A.①②③ B.②③④ C.①②④ D.①③ 7.下列说法错误的是(A) A.氯水中的溶质就是Cl2分子 B.氯水的pH<7 C.氯水在阳光下放置,会有气泡冒出 D.为防止见光变质,应该用棕色瓶来保存氯水 8.用玻璃棒蘸取新制氯水点在pH试纸上,观察到的现象是(B) 9.下列说法不符合事实的是(A) A.漂白粉是纯净物 B.将CO2通入次氯酸钙溶液可生成次氯酸 C.氯气与烧碱溶液或石灰乳反应都能得到含氯消毒剂 D.新制氯水有酸性和强氧化性,滴入少量的紫色石蕊溶液的现象是先变红,后退色 4 10.某学生用下图所示意的方法研究物质的性质,其中气体A的主要成分是氯气,杂质是空气和水蒸气。 回答下列问题: (1)该项研究(实验)的主要目的是探究干燥的氯气没有漂白性,湿润的氯气(氯气和水反应的次氯酸)有漂白性。 (2)浓硫酸的作用是除去氯气中的水蒸气(干燥氯气)。与研究目的直接相关的实验现象是B中干燥的有色布条不退色,C中湿润的有色布条退色。 (3)从物质性质来看,这样的实验设计还存在的事故隐患是没有尾气处理装置,氯气有毒,排放到空气中会污染空气。请在上图的D处以图的形式表明克服事故隐患的措施。 答案:提示:D处的图为导管插入一个盛有NaOH溶液的烧杯中(或其他合理答案) 11.氯水中含有多种成分,因而具有多种性质,根据氯水分别在如图四种情况下发生的反应填空(a、b、c、d中重合部分代表物质间反应,且氯水足量)。 Ⅰ.(1)能证明氯水具有漂白性的是d(填“a”“b”“c”或“d”)。 (2)c过程中的现象是生成白色沉淀,b过程中反应的化学方程式为 Na2CO3+2HCl====2NaCl+H2O+CO2↑。 (3)久置的氯水变为盐酸,用化学反应方程式表示为Cl2+H2O====HCl+HClO、 4 2HClO2HCl+O2↑。 (4)实验室保存饱和氯水的方法是装在棕色瓶中保存在阴暗处。 Ⅱ.用滴管将新制的饱和氯水慢慢滴入含酚酞的NaOH稀溶液中。当滴到最后一滴时红色突然退去。其原因可能有两种,试回答下列问题: (1)可能是由于酚酞被强氧化剂HClO氧化。 (2)可能是由于NaOH被氯水中的酸性物质中和,红色退去。 简述怎样用实验证明红色退去的原因是(1)还是(2)。 答案:向所得溶液中再滴入几滴NaOH溶液,若溶液又恢复成红色,原因(2)对;若无变化,原因(1)对。 12.现有A、B、C三种气体,A是密度最小的气体,B在通常情况下呈黄绿色,纯净的A可以在B中安静地燃烧生成C。把气体B通入适量石灰乳中可以得到白色浑浊物D。请据此回答下列问题: (1)写出下列各反应的化学方程式。 ①纯净的A在B中安静地燃烧生成C:H2+Cl22HCl; ②将气体B通入水中:Cl2+H2O====HCl+HClO; ③将气体B通入NaOH溶液中:Cl2+2NaOH====NaCl+NaClO+H2O; ④将气体B通入适量石灰乳中:2Cl2+2Ca(OH)2====CaCl2+Ca(ClO)2+2H2O。 (2)把三种气体分别通入酸性硝酸银溶液中,出现白色沉淀的气体是BC(用字母表示)。 (3)将白色浑浊物D溶于水得到澄清溶液,分别取适量该澄清溶液两份。 ①向第一份中滴加碳酸钠溶液观察到出现沉淀,发生反应的化学方程式为CaCl2+Na2CO3====CaCO3↓+2NaCl、Ca(ClO)2+Na2CO3====CaCO3↓+2NaClO; ②向第二份溶液中滴加硝酸酸化的硝酸银溶液,会观察到生成白色沉淀(填现象); ③白色浑浊物D因具有漂白性又称为漂白粉,该物质在空气中容易变质的原因为Ca(ClO)2+H2O+CO2====2HClO+CaCO3、2HClO2HCl+O2↑(用化学方程式表示)。 (4)次氯酸与二氧化硫(SO2)反应可以生成两种强酸,请写出次氯酸溶液与二氧化硫反应的化学方程式:HClO+SO2+H2O====HCl+H2SO4。 4查看更多