- 2021-04-20 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019届高考化学二轮复习化学实验操作及实验方案正误辨析学案
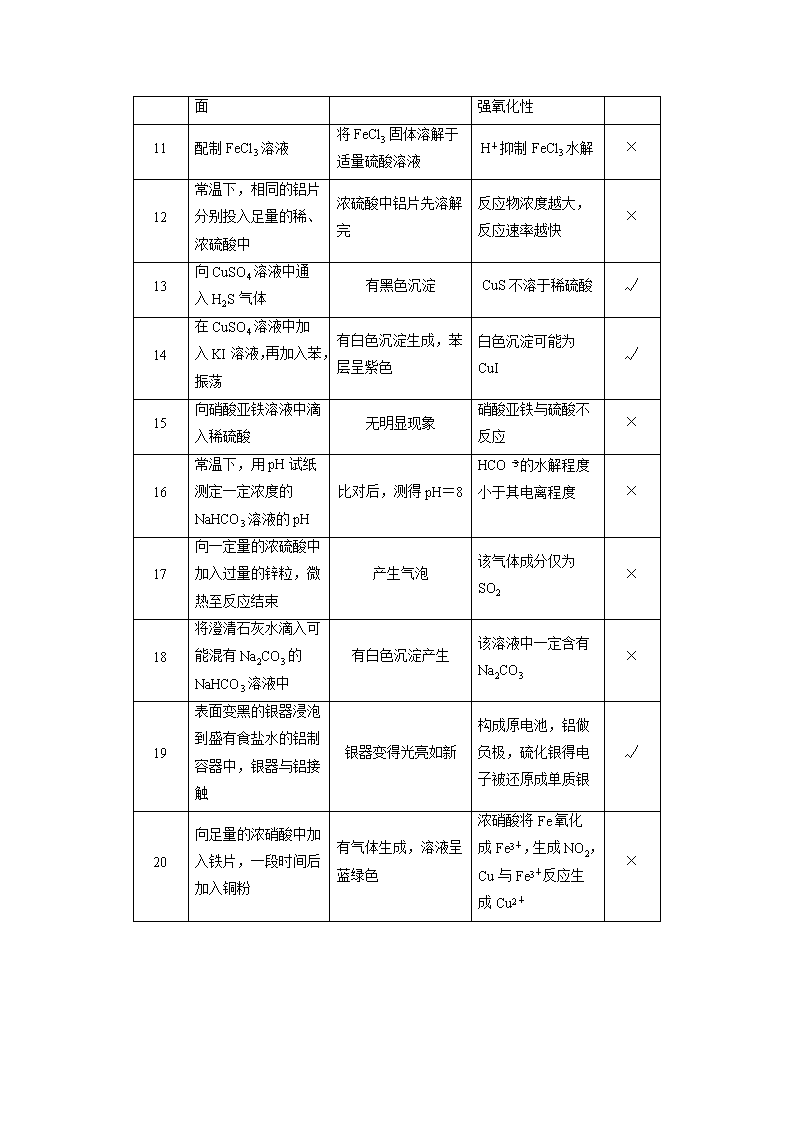
十、化学实验操作及实验方案正误辨析 (一)表格实验中的逻辑关系正误判断 题号 实验 现象 解释与结论 正误 1 用洁净铂丝蘸取溶液 进行焰色反应 火焰呈黄色 原溶液中有 Na+无 K+ × 2 滴加几滴稀 NaOH 溶 液,将湿润红色石蕊 试纸置于试管口 试纸不变蓝 原溶液中无 NH+ 4 × 3 用坩埚钳夹住一小块 用砂纸仔细打磨过的 铝箔在酒精灯上加热 熔化后的液态铝滴落 下来 金属铝的熔点较低 × 4 硝酸银溶液中加入足 量 NaCl 溶液,再加 入 KI 溶液 先出现白色沉淀,后 变为黄色沉淀 Ksp(AgCl)>Ksp(AgI) √ 5 2 mL 2% CuSO4 溶液 中加 4~6 滴 2% NaOH 溶液,振荡后 加入 0.5 mL X 溶液, 加热煮沸 未出现红色沉淀 X 不含有醛基 × 6 等体积 pH=3 的 HA 和 HB 两种酸分别与 足量的锌反应 相同时间内,HA 收 集到氢气多 HA 是强酸 × 7 将铝片和镁条作为电 极,插入 1.0 mol·L-1 的 NaOH 溶液中 电流表指针偏向镁片 金属铝比镁活泼 × 8 向 1.0 mol·L-1 的 NaHCO3 溶液中滴加 2 滴甲基橙 溶液呈黄色 NaHCO3 溶 液呈碱性 × 9 向 NaBr 溶液中加入 氯水,再加入淀粉KI 溶液 溶液变蓝 氧化性:Cl2>Br2>I2 × 10 将浓硫酸滴到蔗糖表 固体变黑膨胀 浓硫酸有脱水性和 √ 面 强氧化性 11 配制 FeCl3 溶液 将 FeCl3 固体溶解于 适量硫酸溶液 H+抑制 FeCl3 水解 × 12 常温下,相同的铝片 分别投入足量的稀、 浓硫酸中 浓硫酸中铝片先溶解 完 反应物浓度越大, 反应速率越快 × 13 向 CuSO4 溶液中通入 H2S 气体 有黑色沉淀 CuS 不溶于稀硫酸 √ 14 在 CuSO4 溶液中加入 KI 溶液,再加入苯, 振荡 有白色沉淀生成,苯 层呈紫色 白色沉淀可能为 CuI √ 15 向硝酸亚铁溶液中滴 入稀硫酸 无明显现象 硝酸亚铁与硫酸不 反应 × 16 常温下,用 pH 试纸 测定一定浓度的 NaHCO3 溶液的 pH 比对后,测得 pH=8 HCO - 3 的水解程度 小于其电离程度 × 17 向一定量的浓硫酸中 加入过量的锌粒,微 热至反应结束 产生气泡 该气体成分仅为 SO2 × 18 将澄清石灰水滴入可 能混有 Na2CO3 的 NaHCO3 溶液中 有白色沉淀产生 该溶液中一定含有 Na2CO3 × 19 表面变黑的银器浸泡 到盛有食盐水的铝制 容器中,银器与铝接 触 银器变得光亮如新 构成原电池,铝做 负极,硫化银得电 子被还原成单质银 √ 20 向足量的浓硝酸中加 入铁片,一段时间后 加入铜粉 有气体生成,溶液呈 蓝绿色 浓硝酸将 Fe 氧化成 Fe3+,生成 NO2, Cu 与 Fe3+反应生成 Cu2+ × (二)表格实验中实验操作与实验目的正误判断 题号 实验操作 实验目的 正误 1 向 2 mL 1 mol·L-1 NaOH 溶液中先加入 3 滴 1 mol·L-1 FeCl3 溶液,再加 入 3 滴 1 mol·L-1 MgCl2 溶液 证明 Ksp[Mg(OH)2]>Ksp[Fe(OH)3] × 2 相同温度下,向两支盛有 相同体积不同浓度 H2O2 溶液的试管中分别滴入适 量相同浓度的 CuSO4 溶液 和 FeCl3 溶液 探究 Cu2+、Fe3+对 H2O2 分 解速率的影响 × 3 室温下,用 pH 试纸分别 测定浓度为 0.1 mol·L-1 NaClO 溶液和 0.1 mol·L-1 CH3COONa 溶液的 pH 比较 HClO 和 CH3COOH 的 酸性强弱 × 4 向含有酚酞的 Na2CO3 溶 液中加入少量 BaCl2固体, 溶液红色变浅 证明 Na2CO3 溶液中存在水 解平衡 √ 5 分别测定室温下等物质的 量浓度的 Na2SO3 与 Na2CO3 溶液的 pH,后者 较大 证明非金属性:S>C × 6 将 NaOH 溶液滴入某溶液 中加热,放出的气体能使 湿润的红色石蕊试纸变蓝 证明溶液中有 NH+ 4 √ 7 分别通入硝酸银溶液中, 产生淡黄色沉淀的是溴蒸 气 鉴别溴蒸气和 NO2 √ 8 在醋酸钠溶液中滴入酚酞 溶液,加热后红色加深 证明盐类水解是吸热反应 √ 9 用硫酸酸化的 H2O2 溶液 滴入 Fe(NO3)2 溶液中,溶 证明氧化性:H2O2 比 Fe3+ 强 × 液变黄色 10 往黄色固体难溶物 PbI2 中 加水,振荡,静置。取上 层清液,然后加入 NaI 固 体,产生黄色沉淀 证明难溶物存在沉淀溶解 平衡 √ 11 向 AgCl 悬浊液中加入 NaI 溶液时出现黄色沉淀 Ksp(AgCl)查看更多
相关文章
- 当前文档收益归属上传用户
- 下载本文档