- 2021-05-21 发布 |
- 37.5 KB |
- 7页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
广东省湛江市第二十一中学2019-2020学年高一下学期开学考试化学试题
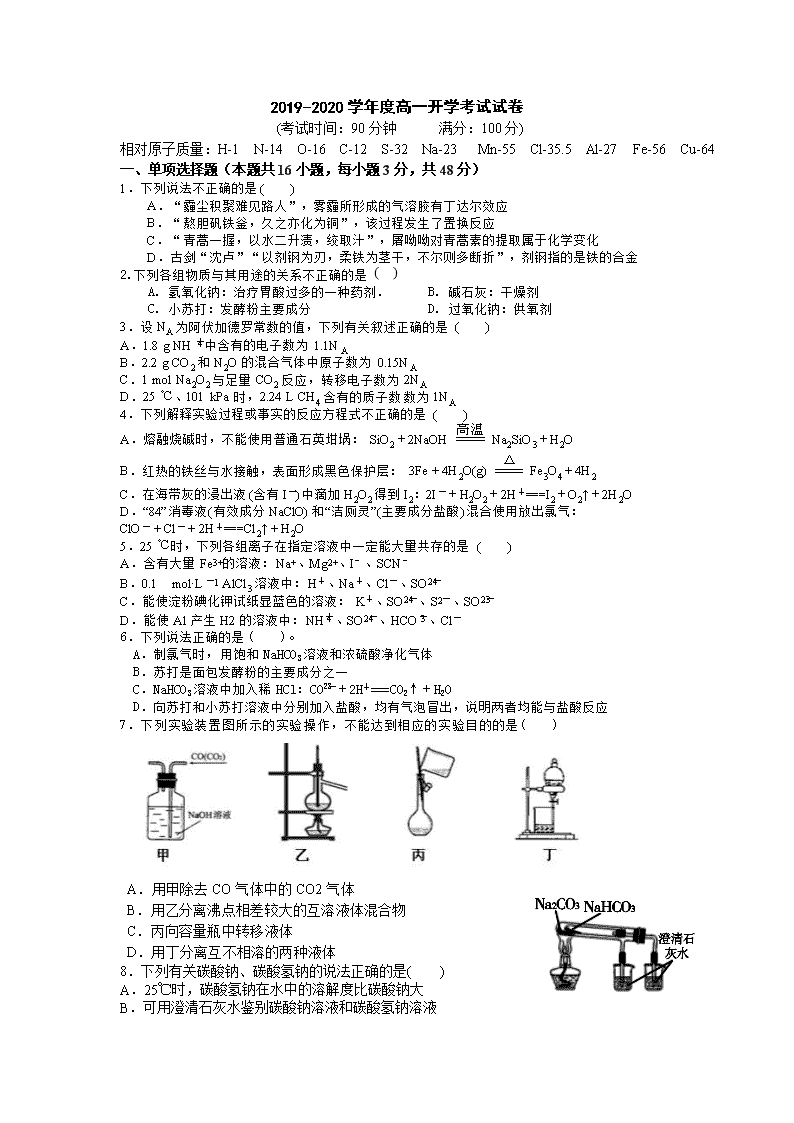
2019-2020学年度高一开学考试试卷 (考试时间:90分钟 满分:100分) 相对原子质量:H-1 N-14 O-16 C-12 S-32 Na-23 Mn-55 Cl-35.5 Al-27 Fe-56 Cu-64 一、单项选择题(本题共16小题,每小题3分,共48分) 1.下列说法不正确的是( ) A.“霾尘积聚难见路人”,雾霾所形成的气溶胶有丁达尔效应 B.“熬胆矾铁釡,久之亦化为铜”,该过程发生了置换反应 C.“青蒿一握,以水二升渍,绞取汁”,屠呦呦对青蒿素的提取属于化学变化 D.古剑“沈卢”“以剂钢为刃,柔铁为茎干,不尔则多断折”,剂钢指的是铁的合金 2.下列各组物质与其用途的关系不正确的是 A. 氢氧化钠:治疗胃酸过多的一种药剂. B. 碱石灰:干燥剂 C. 小苏打:发酵粉主要成分 D. 过氧化钠:供氧剂 3.设NA为阿伏加德罗常数的值,下列有关叙述正确的是( ) A.1.8 g NH中含有的电子数为1.1NA B.2.2 g CO2和N2O的混合气体中原子数为0.15NA C.1 mol Na2O2与足量CO2反应,转移电子数为2NA D.25 ℃、101 kPa时,2.24 L CH4含有的质子数数为1NA 4.下列解释实验过程或事实的反应方程式不正确的是( ) A.熔融烧碱时,不能使用普通石英坩埚:SiO2+2NaOHNa2SiO3+H2O B.红热的铁丝与水接触,表面形成黑色保护层:3Fe+4H2O(g)Fe3O4+4H2 C.在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+H2O2+2H+===I2+O2↑+2H2O D.“84”消毒液(有效成分NaClO)和“洁厕灵”(主要成分盐酸)混合使用放出氯气: ClO-+Cl-+2H+===Cl2↑+H2O 5.25 ℃时,下列各组离子在指定溶液中一定能大量共存的是( ) A.含有大量Fe3+的溶液:Na+、Mg2+、I﹣、SCN﹣ B.0.1 mol·L-1 AlCl3溶液中:H+、Na+、Cl-、SO C.能使淀粉碘化钾试纸显蓝色的溶液:K+、SO、S2-、SO D.能使Al产生H2的溶液中:NH、SO、HCO、Cl- 6.下列说法正确的是( )。 A.制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体 B.苏打是面包发酵粉的主要成分之一 C.NaHCO3溶液中加入稀HCl:CO+2H+===CO2↑+H2O D.向苏打和小苏打溶液中分别加入盐酸,均有气泡冒出,说明两者均能与盐酸反应 7.下列实验装置图所示的实验操作,不能达到相应的实验目的的是( ) A.用甲除去CO气体中的CO2气体 B.用乙分离沸点相差较大的互溶液体混合物 C.丙向容量瓶中转移液体 D.用丁分离互不相溶的两种液体 8.下列有关碳酸钠、碳酸氢钠的说法正确的是( ) A.25℃ 时,碳酸氢钠在水中的溶解度比碳酸钠大 B.可用澄清石灰水鉴别碳酸钠溶液和碳酸氢钠溶液 C.可用如图所示装置比较Na2CO3和 NaHCO3的热稳定性 D.常温下,浓度均为0.1mol·L时,碱性:NaHCO3> Na2CO3 9.Na2FeO4是一种高效多功能水处理剂,应用前景十分看好。一种制备Na2FeO4的方法可用化学方程式表示如下:2FeSO4+6Na2O2 ===2Na2FeO4+2Na2O+2Na2SO4 +O2↑,对此反应下列说法中正确的是( ) A.Na2O2只作氧化剂 B.2 mol FeSO4发生反应时,反应中共有8 mol电子转移 C.每生成16 g氧气就有1 mol Fe2+被还原 D.Na2FeO4既是还原产物又是氧化产物 10.为了除去粗盐中的Ca2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列操作:①过滤;②加适量的盐酸;③加过量的Na2CO3溶液;④加过量BaCl2溶液,正确的操作顺序是( ) A.①③④②B.③①④② C.①②③④ D.④③①② 11.下列除去杂质的方法不正确的是( ) A.镁粉中混有少量铝粉:加入过量烧碱溶液充分反应,过滤、洗涤、干燥 B.用过量氨水除去Fe3+溶液中的少量Al3+ C.Al(OH)3中混有少量Mg(OH)2:加入足量烧碱溶液,充分反应,过滤,向滤液中通入过量CO2后过滤 D.MgO中混有少量Al2O3:加入足量烧碱溶液,充分反应,过滤、洗涤、干燥得到MgO 12.下列实验操作及现象能够达成相应实验结论的是( ) 选项 实验操作及现象 结论 A 向某溶液中加入BaCl2溶液,有白色沉淀生成 溶液中一定含有 B 向某溶液中加入盐酸,产生能使澄清石灰水变浑浊的无色气体 溶液中一定含有 C 向某溶液中先加入盐酸酸化,没有明显现象,再加入BaCl2溶液,有白色沉淀产生 溶液中一定含有SO42- D 向5mL饱和氯水中滴加少量0.1 mol/L NaBr溶液,溶液由无色变为橙黄色,再滴加足量0.1 mol/L淀粉-KI溶液,溶液变蓝 氧化性强弱:Cl2>Br2>I2 13.下列各图示中能较长时间看到Fe(OH)2白色沉淀的是( ) A.①② B.①③ C.②③ D.①②③ 14.实验室利用以下反应制取少量氮气,NaNO2+NH4Cl===NaCl+N2↑+2H2O,下列关于该反应的说法正确的是( ) A.NaNO2发生氧化反应 B.NH4Cl中的氮元素被还原 C.N2既是氧化产物,又是还原产物 D.每生成1 mol N2转移电子的物质的量为6 mol 15.向含有1 mol FeCl2的溶液中通入0.2 mol Cl2,再加入含0.1 mol X2O的酸性溶液,使溶液中Fe2+恰好全部被氧化,并使X2O被还原为Xn+,则n值为( ) A.2 B.3 C.4 D.5 16.把V L含有MgSO4和K2SO4的混合溶液分成两等份,一份加入含a mol NaOH的溶液,恰好使镁离子完全沉淀为氢氧化镁;另一份加入含b mol BaCl2的溶液,恰好使硫酸根离子完全沉淀为硫酸钡。则原混合溶液中钾离子的浓度为( ) A. mol·L-1 B.mol·L-1 C. mol·L-1 D. mol·L-1 二、填空题(本题包括5小题,共52分) 17.工业上制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的Al2O3,然后电解Al2O3得到铝。下图是从铝土矿中提纯Al2O3的简单示意图。其中涉及到的一个反应:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓。 (1)图示中实验操作(1)是________;加入的试剂②是__________(填化学式) (2)试写出B溶液中的溶质的化学式:_____________ (3)写出化学方程式: ①铝土矿→A:_________________________________________________。 ②E→F:_______________________________________________________。 18.如图所示是一个制取Cl2并以Cl2为原料进行特定反应的装置,多余的Cl2可以贮存在b瓶中,其中各试剂瓶中所装试剂为:B(氢硫酸)、C(淀粉 KI溶液)、D(水)、F(紫色石蕊试液)。 (1)若装置A烧瓶中的固体为MnO2,液体为浓盐酸,则其发生反应的化学方程式为____________________________________________________。 (2)装置E中硬质玻璃管内盛有炭粉,若E中发生氧化还原反应,其产物为二氧化碳和氯化氢,写出E中反应的化学方程式:_________________________________________。 (3)D中溶液的存在含氯的阴离子为___________________________。 (4)在F中紫色石蕊试液的颜色由紫色变为红色,再变为无色,其原因是_______________________________________。 (5)若F中盛有NaOH溶液,其作用是_____________________________________________。 19.某无色稀溶液X中,可能含有下表所列离子中的某几种。 阴离子 CO、SiO、AlO、Cl- 阳离子 Al3+、Fe3+、Mg2+、NH、Na+ 现取该溶液适量,向其中加入某试剂Y,产生沉淀的物质的量(n)与加入试剂体积(V)的关系如图所示。 (1)若Y是盐酸,则oa段转化为沉淀的离子(指来源于X溶液的,下同)是________________________,ab段发生反应的离子是________,bc段发生反应的离子方程式为___________________________________。 (2)若Y是NaOH溶液,则X中一定含有的阳离子是____________________, ab段反应的离子方程式为_______________________________________________________________________。 20.某化学兴趣小组用只含有铝、铁、铜的工业合金制取纯净的氯化铝溶液、绿矾晶体(FeSO4·7H2O)和胆矾晶体,其实验方案如图所示: (1)合金与NaOH溶液反应的离子方程式为 。 (2)方案中途径②的离子方程式________________________________________________, D中加入适量盐酸的离子方程式为 。 (3)滤渣F的主要成分为 (4)CuSO4溶液中获得胆矾的操作为蒸发浓缩, 、过滤_,洗涤、自然干燥。 21.在用氨气饱和的食盐水中通入足量二氧化碳可生成NaHCO3固体,反应原理如下: NH3+CO2+H2O=NH4HCO3 NH4HCO3+NaCl=NaHCO3↓+NH4Cl 化学兴趣小组同学根据该原理和如下装置在实验室制备NaHCO3。 实验步骤如下: Ⅰ、连接好如图装置,检查气密性后,在仪器内装入相应药品。 Ⅱ、在丙装置制备氨气,并通入到丁中饱和食盐水中,直至不再溶解时,然后在饱和食盐水中通入二氧化碳气体,片刻后,丁装置广口瓶中出现固体。继续向广口瓶中通入两种气体,直到不再有固体产生。 Ⅲ、过滤丁中广口瓶中所得的混合物,洗涤、干燥,得到NaHCO3固体。 (1)盛装盐酸的仪器名称是_____________。 (2)乙中溶液是_______(填字母代号)。 A.浓硫酸 B.饱和Na2CO3溶液 C.饱和NaHCO3溶液 (3)装置的部分连接顺序是:a接________(填“c”或“d”);丁装置中球形干燥管的作用是_________________________________。 (4)请解释在实验步骤Ⅱ中,先通入氨气的理由是______ _______________ _______。 (5)取m g NaHCO3样品(杂质只含有少量NaCl)溶于足量盐酸,蒸干后称得固体质量为n g,则样品中NaHCO3的质量分数为_____________(用含m、n的代数式表示,不用化简)。 2019-2020学年度高一开学考试 化学参考答案 选择题答案 题号 1 2 3 4 5 6 7 8 答案 C A B C B D B C 题号 9 10 11 12 13 14 15 6 答案 D D B C B C B D 非选择题答案 17.(10分)(每空2分) (1)过滤 Ca(OH)2 或 Ba(OH)2 (2)NaAlO2 (3)①Al2O3+2NaOH=2NaAlO2+H2O ② 2Al(OH)3Al2O3+3H2O 18. (10分)(每空2分) (1)MnO2+4HCl(浓) = MnCl2+Cl2↑+2H2O(2分) (2)C+2H2O+2Cl2 = CO2+4HCl(2分) (3) Cl-、ClO-(2分) (4)E中生成的酸性气体进入F中可使紫色石蕊试液变红,未反应完的Cl2进入F中与水作用生成HClO,HClO具有漂白作用,使溶液的红色褪去(2分) (5)吸收尾气Cl2和HCl,防止污染空气(2分) 19. (10分)(每空2分) (1)SiO、AlO(2分) CO(2分) Al(OH)3+3H+===Al3++3H2O(2分) (2)Al3+、Mg2+、NH(2分) NH+OH-===NH3·H2O(2分) [解析] 溶液为无色,说明溶液X中不含Fe3+;若Y为盐酸,由图像的特点判断溶液X中一定含有AlO、SiO、CO,其中Oa段发生的反应为:AlO+H++H2O===Al(OH)3↓,SiO+2H+===H2SiO3↓,故转化为沉淀的离子为SiO、AlO;ab段发生的反应为:CO+H+===HCO,HCO+H+===H2O+CO2↑,但仅有CO来源于X溶液;bc段发生的反应为:Al(OH)3+3H+===Al3++3H2O。若Y为NaOH溶液,由图像特点判断溶液中一定含有Mg2+、Al3+、NH。其中Oa段发生反应为:Al3++3OH- ===Al(OH)3↓,Mg2++2OH-===Mg(OH)2↓;ab段发生的反应为:NH+OH-===NH3·H2O;bc段发生的反应为:Al(OH)3+OH-===AlO+2H2O; 20.(10分)(每空2分) (1) 2Al+2OH-+2H2O===2AlO+3H2↑(2分) (2)AlO+CO2+2H2O===Al(OH)3↓+HCO(2分) Al(OH)3+3H+===Al3++3H2O(2分) (3)Cu或铜单质(2分) (4)冷却结晶(2分) 21.(12分)(每空2分) (1)分液漏斗 (2)C (3)d 防止倒吸 (4)在相同条件下,氨气在水中的溶解度远大于二氧化碳,在饱和食盐水中先通入氨气,形成浓的食盐氨水混合溶液(1分),能与更多的二氧化碳反应,进而提高NaHCO3的产量(1分)。(其他合理答案均分步给分) (5) 或 (其他合理答案均给分)查看更多