山东省实验中学2021届高三化学上学期第一次诊断试题(Word版附解析)
山东省实验中学2021届高三第一次诊断考试
化学试题
(本试卷共8页,20题。全卷满分100分,考试用时90分钟)
注意事项:
1.答卷前,先将自己的姓名、准考证号填写在试卷和答题纸上。
2.选择题的作答:每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案标号。
3.非选择题的作答:用0.5mm黑色签字笔直接答在答题卡上对应的答题区域内,写在试卷、草稿纸和答题卡上的非答题区域均无效。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Mn 55 Cu 64
第I卷 (共40分)
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1. 下列有关说法正确的是
A. 反应Hg(1)+H2SO4(aq)=HgSO4(aq)+H2(g)在常温下不能自发进行,则△H<0
B. 在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法
C. SnCl2+H2O⇌Sn(OH)Cl↓+HC1配制氯化亚锡溶液时加入NaOH固体
D. 当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用
【答案】B
【解析】
【详解】A. 反应不能自发,应满足△G=△H-T•△S>0,即△H>T•△S,而该反应的△S>0,故△H>0,故A错误;
B. 海轮外壳连接锌块,锌为负极,保护外壳不受腐蚀,为牺牲阳极的阴极保护法,故B正确;
C. SnCl2在溶液中水解显酸性,加氢氧化钠会促进SnCl2水解,所以配制氯化亚锡溶液时加入HCl抑制水解,故C错误;
D. 铁比锡活泼,当镀锡铁制品的镀层破损时,金属铁为负极,金属锡为正极,铁易被腐蚀,故D错误;
故选B。
2. 常温,下列各组离子一定能在指定溶液中大量共存的是( )
A. =10-12的溶液中:、Cu2+、、
B. 滴加KSCN溶液显红色的溶液中:、K+、Cl-、I-
C. 0.1mol·L-1的NaHCO3溶液中:Fe3+、K+、Cl-、
D. 水电离产生的c(OH-)=10-12mol·L-1的溶液中:Na+、Al3+、Cl-、
【答案】A
【解析】
【详解】A. 常温下,在的溶液中,c(H+)=0.1mol·L-1,溶液显酸性,离子之间均不能发生反应,A项正确;
B. 滴加KSCN溶液显红色,说明溶液中存在Fe3+,Fe3+能够氧化I-,B项错误;
C. Fe3+与HCO3-发生相互促进的水解反应而不能大量共存,C项错误;
D. 由水电离的c(OH-)=10-12mol·L-1的溶液可能呈强酸性也可能呈强碱性,碱性溶液中Al3+不能大量存在,D项错误;
答案选A。
【点睛】离子共存问题,侧重考查学生对离子反应发生的条件及其实质的理解能力,题型不难,需要注意的是,溶液题设中的限定条件。如无色透明,则常见的有颜色的离子如Cu2+、Fe3+、Fe2+、MnO4-、Cr2O72-、CrO42-等不符合题意;还有一些限定条件如:常温下与Al反应生成氢气的溶液时,该溶液可能为酸溶液,也可能为碱溶液。做题时只要多加留意,细心严谨,便可快速选出正确答案。还有一些限定条件如:常温下水电离出来的 H+和 OH-浓度为1×10-10,小于1×10-7时,该溶液可能为酸溶液,也可能为碱溶液。做题时只要多加留意,细心严谨,便可快速选出正确答案。
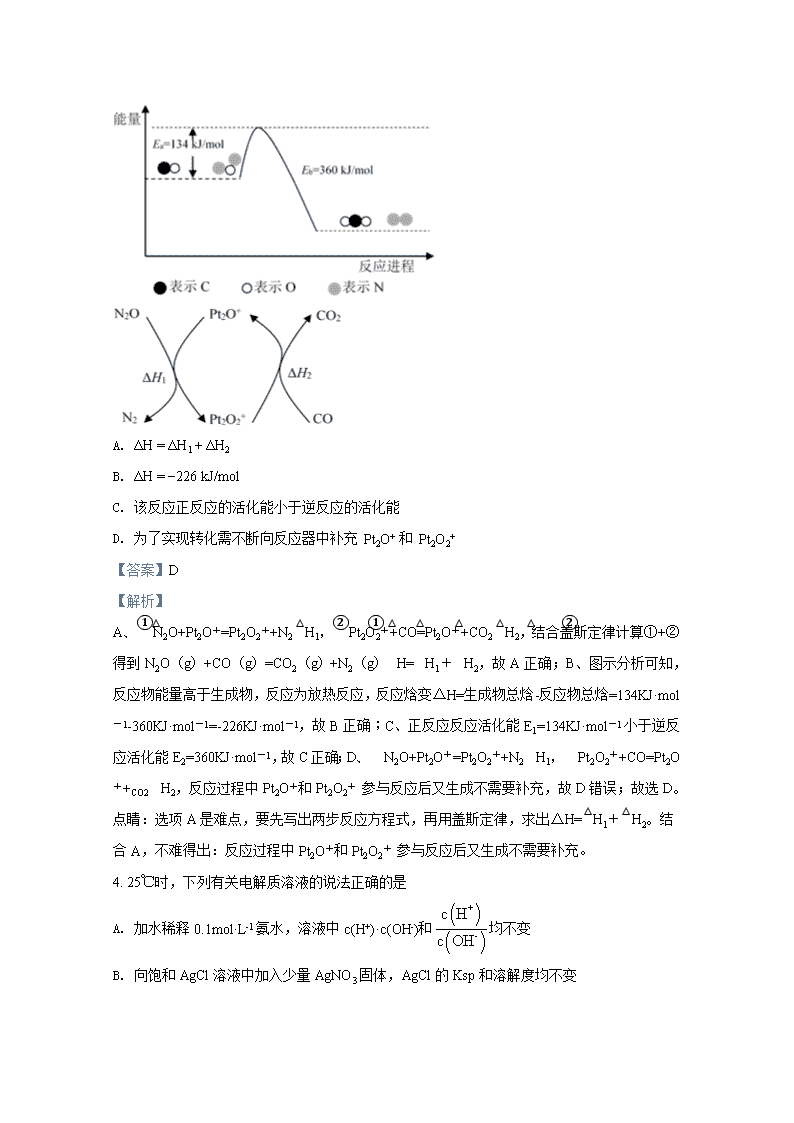
3. N2O和CO是环境污染性气体,可在Pt2O+ 表面转化为无害气体,其反应原理为N2O(g) + CO(g)CO2(g) + N2(g) ΔH,有关化学反应的物质变化过程及能量变化过程如下。下列说法不正确的是
A. ΔH = ΔH1 + ΔH2
B. ΔH = −226 kJ/mol
C. 该反应正反应的活化能小于逆反应的活化能
D. 为了实现转化需不断向反应器中补充 Pt2O+ 和 Pt2O2+
【答案】D
【解析】
A、①N2O+Pt2O+=Pt2O2++N2 △H1,②Pt2O2++CO=Pt2O++CO2 △H2,结合盖斯定律计算①+②得到N2O(g)+CO(g)=CO2(g)+N2(g)△H=△H1+△H2,故A正确;B、图示分析可知,反应物能量高于生成物,反应为放热反应,反应焓变△H=生成物总焓-反应物总焓=134KJ·mol-1-360KJ·mol-1=-226KJ·mol-1,故B正确;C、正反应反应活化能E1=134KJ·mol-1小于逆反应活化能E2=360KJ·mol-1,故C正确;D、①N2O+Pt2O+=Pt2O2++N2 △H1,②Pt2O2++CO=Pt2O++CO2 △H2,反应过程中Pt2O+和Pt2O2+ 参与反应后又生成不需要补充,故D错误;故选D。
点睛:选项A是难点,要先写出两步反应方程式,再用盖斯定律,求出△H=△H1+△H2。结合A,不难得出:反应过程中Pt2O+和Pt2O2+ 参与反应后又生成不需要补充。
4. 25℃时,下列有关电解质溶液的说法正确的是
A. 加水稀释0.1mol·L-1氨水,溶液中c(H+)·c(OH-)和均不变
B. 向饱和AgCl溶液中加入少量AgNO3固体,AgCl的Ksp和溶解度均不变
C. 向CH3COONa溶液中加入少量CH3COONa固体,溶液中增大
D. 向盐酸中滴加氨水,由水电离出的c(H+)=10-7mol·L-1时,溶液一定显中性
【答案】C
【解析】
【详解】A. 溶液中c(H+)c(OH−)=Kw,Kw只与温度有关,则c(H+)⋅c(OH−)不变,=,稀释过程中c(OH−)发生变化,则变化,故A错误;
B. Ksp只与温度有关,饱和AgCl中加入少量AgNO3,导致AgCl溶解度降低,则Ksp不变,溶解度改变,故B错误;
C. 向CH3COONa溶液中加入少量CH3COONa,溶液中=,加入CH3COONa,溶液碱性增强,则c(H+)降低,所以值增大,故C正确;
D. 向盐酸中滴加氨水,由水电离出的c(H+)=10−7mol/L时,整个溶液c(H+)=10−7mol/L说明溶液显中性,不是指由水电离出的c(H+)=10−7mol/L时,溶液一定显中性,故D错误;
故选C。
5. 速率与限度是研究化学反应的重要视角,下列叙述错误的是( )
A. 对于反应,其他条件不变,增加木炭的量,反应速率不变
B. 某物质化学反应速率为是指时该物质的浓度为
C. 氯酸钾分解制取氧气时添加少量二氧化锰,可增大反应速率
D. 在给定条件下,达到平衡时,可逆反应完成程度达到最大
【答案】B
【解析】
【详解】A.对于反应,其他条件不变,增加木炭的量不能改变其浓度,故反应速率不变,A正确;
B.某物质化学反应速率为是指平均内该物质的浓度的变化量为,
B错误;
C.二氧化锰可以催化氯酸钾分解,因此,氯酸钾分解制取氧气时添加少量二氧化锰,可增大反应速率,C正确;
D.化学平衡状态就是在给定条件下某可逆反应所能达到的最大限度,D正确;
综上所述,相关叙述错误的是B。
6. 如下图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X 为阳离子交换膜。下列有关说法正确的是
A. 反应一段时间后,乙装置中生成的氢氧化钠在铁极区
B. 乙装置中铁电极为阴极,电极反应式为Fe-2e-= Fe2+
C. 反应一段时间后,丙装置中硫酸铜溶液浓度保持不变
D. 通入氧气的一极为正极,发生的电极反应为O2 - 4e- + 2H2O = 4OH-
【答案】A
【解析】
【分析】
甲装置为甲醚燃料电池,通入氧气的一极发生还原反应,为电极的正极,投放燃料的为电极的负极;乙装置为电解饱和氯化钠的装置,根据串联电池中,电子的转移,可知Fe电极为阴极,C极为阳极;丙装置为电解精炼铜的装置,精铜为阴极,粗铜为阳极。
【详解】A.乙装置中铁极反应2H++2e-=H2↑,所以反应一段时间后,装置中生成氢氧化钠在铁极区,选项A正确;
B.乙装置中铁极反应为2H++2e-=H2↑, 选项B错误;
C.投放氧气的一极发生还原反应,为电极的正极,发生的电极反应为:O2+2H2O+4e-=4OH-,选项C错误;
D
.丙装置中,粗铜极除了铜发生氧化反应外,活动性在铜前面的金属也要反应,但是在精铜极,除铜离子被还原外,没有其他离子能被还原,根据得失电子相等,可知硫酸铜溶液浓度减小,选项D错误,
答案选A。
【点睛】本题考查原电池和电解池知识,侧重于学生的分析能力和计算能力的考查,注意把握电极方程式的书写,为解答该题的关键,结合串联电路的特点解答该题,解题关键是理解:燃料电池中通入氧气的电极是正极,正极上得电子发生还原反应,负极上燃料失电子发生氧化反应。
7. 为了探究温度、硫酸铜对锌与稀硫酸反应生成氢气速率的影响,某同学设计了如下方案:
下列推断合理的是
A. 选择II和III实验探究硫酸铜对反应速率的影响,必须控制t=25
B. 待测物理量是收集等体积(相同条件)的气体所需要的时间,时间越长,反应越快
C. 根据该方案,还可以探究稀硫酸浓度对反应速率的影响
D. 根据该实验方案得出反应速率大小可能是III>II>I>IV
【答案】D
【解析】
【详解】A. 要选择Ⅱ和Ⅲ实验探究硫酸铜对反应速率的影响,只有硫酸铜不同,其余条件都相同,所以必须控制t=35,故A错误;
B. 待测物理量是收集等体积(相同条件)气体所需要的时间,时间越长,反应越慢,故B错误;
C.该方案中,三组实验稀硫酸浓度都相等,不可以探究稀硫酸浓度对反应速率的影响,故C错误;
D. 温度越高反应速率越快,原电池加快反应速率,Ⅲ、Ⅳ温度相同且都能形成原电池,但Ⅳ硫酸铜量太多与Zn反应影响生成氢气的速率,则反应速率的大小可能是Ⅲ>Ⅱ>Ⅰ>Ⅳ,故D正确;。
故选:D。
8. 在某一恒温体积可变的密闭容器中发生反应:A(g)+B(g)2C(g) ΔH<0。t1
时刻达到平衡后,在t2时刻改变某一条件,其反应过程如下图所示。下列说法正确的是( )
A. O~t2时,v正>v逆
B. Ⅰ、Ⅱ两过程达到平衡时,A的体积分数Ⅰ>Ⅱ
C. t2时刻改变的条件是向密闭容器中加C
D. Ⅰ、Ⅱ两过程达到平衡时,平衡常数Ⅰ<Ⅱ
【答案】C
【解析】
【详解】A.0~t1,反应正向进行,说明v正>v逆,t1~t2,反应到达平衡,v正=v逆,t2时,反应逆向进行,v逆>v正,A错误;
B. 0~t1,反应正向进行,说明v正>v逆,t1~t2,反应到达平衡,v正=v逆,t2时,反应逆向进行,v逆>v正,因此达到平衡时A的体积分数Ⅰ<Ⅱ,B错误;
C.向密闭容器中加C,逆反应速率瞬间增大,再次建立的平衡与原平衡等效,说明和原平衡相同,符合图象,C正确;
D.该反应是在恒温下进行,化学平衡常数只与温度有关,温度不变,化学平衡常数不变,所以Ⅰ、Ⅱ两过程达到平衡时,平衡常数KI=KⅡ,D错误;
故合理选项是C。
9. 在一定条件下,利用CO2合成CH3OH的反应为CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) △H1,研究发现,反应过程中会发生副反应为CO2(g)+H2(g)⇌CO(g)+H2O(g) △H2,温度对CH3OH、CO的产率影响如图所示。下列说法中不正确的是
A. △H1<0,△H2>0
B. 增大压强有利于加快合成反应的速率
C. 选用合适的催化剂可以减弱副反应的发生
D. 生产过程中,温度越高越有利于提高CH3OH的产率
【答案】D
【解析】
【详解】A.根据图示升高温度CH3OH的产率降低,反应CO2(g)+3H2(g)CH3OH (g)+H2O(g) 向逆反应方向移动,ΔH10,升高温度CO的产率增大,反应CO2(g)+H2(g)CO(g)+H2O(g)向正反应方向移动,ΔH20,选项A正确;
B.反应有气体参与,增大压强有利于加快合成反应的速率,选项B正确;
C.催化剂有一定的选择性,选用合适的催化剂可以减弱副反应的发生,选项C正确;
D.由图像可见,温度越高CH3OH的产率越低,选项D错误;
答案选C。
10. 下列图示或根据图示所得出的结论正确的是
A. 图甲表示相同pH的盐酸和醋酸加水稀释过程中pH的变化,则曲线a代表醋酸
B. 图乙表示温度不变,向0.1mol·L-1NH4Cl溶液中滴加0.1mol·L-1盐酸时,溶液中随盐酸体积的变化关系
C. 图丙表示密闭容器中CH4(g)+ H2O(g)⇌CO(g)+3H2(g)到达平衡时,CH4的平衡转化率与压强、温度的变化关系曲线,说明P1
Ksp[Cu(OH)2]
C
向Na2CO3溶液中加入浓盐酸,将产生的气体通入硅酸钠溶液中
产生白色浑浊
酸性:盐酸>碳酸>硅酸
D
向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液
前者溶液变蓝色,后者有黄色沉淀
KI3溶液中存在II2+I−平衡
A. A B. B C. C D. D
【答案】C
【解析】
【详解】A. NaHS溶液中存在平衡:HS-+H2OH2S+OH-,HS-H++S2-,向NaHS溶液中滴入酚酞,溶液变红色,溶液呈碱性,说明HS-水解程度大于电离程度,实验目的和结论一致,A项正确;
B. 溶度积小的先生成沉淀,向浓度为0.1mol•L-1的MgCl2、CuCl2混合溶液中逐滴加入氨水先出现蓝色沉淀,说明Ksp[Cu(OH)2]较小,B项正确;
C.
浓盐酸具有挥发生,反应产生的二氧化碳中含有氯化氢气体,干扰二氧化碳与硅酸钠反应生成硅酸,无法证明碳酸酸性强于硅酸,C项错误;
D. 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液,前者溶液变蓝色,说明溶液中含有碘,后者有黄色沉淀,说明溶液中含有碘离子,原来的溶液是KI3溶液,由现象可知,KI3溶液中存在I3-I2+I-平衡,D项正确;
答案选C。
12. 硼化钒(VB2)空气电池是目前储电能力最高的电池,电池示意图如图,该电池工作时发生的反应为:4VB2+11O2=4B2O3+2V2O5。下列说法不正确的是( )
A. 电极a电池正极
B. 电池工作过程中,电极a附近区域pH减小
C. 图中选择性透过膜为阴离子透过膜
D. VB2极发生的电极反应为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O
【答案】B
【解析】
【分析】
根据题中硼化钒(VB2)空气电池可知,本题考查燃料电池,运用原电池原理和氧化还原反应知识分析。
【详解】A.硼化帆一空气燃料电池中,VB2在负极失电子,氧气在正极上得电子,所以a为正极,A项正确;
B.硼化钒-空气燃料电池中,氧气在a极上得电子,氧气得电子生成氢氧根离子,所以a电极附近溶液pH增大,B项错误;
C.氧气在正极上得电子生成OH-,OH-通过选择性透过膜向负极移动,所以图中选择性透过膜应只允许阴离子通过,C项正确;
D.负极上是VB2失电子发生氧化反应,则VB2极发生的电极反应为:2VB2+22OH--22e-=V2O5+2B2O3+11H2O,D项正确。
答案选B。
【点睛】燃料电池正负极判断:燃料电池中氧气做正极,燃料做负极。
13. 下列示意图表示正确的是
A. 甲图表示Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)(△H>0)反应的能量变化
B. 乙图表示碳的燃烧热
C. 丙图表示实验的环境温度20℃,将物质的量浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,测量混合液温度,结果如图(已知Vl+V2=60mL)
D. 由丁图可知A、B、C的稳定性顺序为:B0为吸热反应,选项A错误;
B. 碳的燃烧热是指1molC完全燃烧放出的热量,选项B错误;
C. 酸碱中和反应为放热反应,物质的量浓度相等、体积分别为V1、V2的H2SO4、NaOH溶液混合,V1+V2=60mL,则V1=20mL,V2=40mL时硫酸与氢氧化钠恰好完全反应,放出的热量最多,温度最高,与图象不符,选项C错误;
D.物质的总能量越低,越稳定,所以三种化合物的稳定性顺序:B<A<C,选项D正确;
故选D。
14. 常温下,用0.1mol·L-1NaOH溶液滴定20mL 0.1mol·L-1H3PO4溶液,曲线如图所示,下列说法中正确的是
A. 当2c(HPO)>c(PO)>c(H2PO)
D. 等浓度的NaH2PO4和Na2HPO4的混合溶液中有2c(H+)+c(H2PO)+3c(H3PO4)=2c(OH-)+c(HPO)+3c(PO)
【答案】AD
【解析】
【分析】
根据图像可知,当加入NaOH为零时,pH=2,说明磷酸为弱酸;加入NaOH的体积为20mL时,恰好生成磷酸二氢钠;加入NaOH的体积为40mL时,恰好生成磷酸一氢钠。
【详解】A.H3PO4的第一步电离平衡常数与温度有关,与溶液的pH大小无关,因此当2<pH<4.7时,H3PO4的第一步电离平衡常数均相同,A说法正确;
B.根据电荷守恒得到A点溶液中有:c(Na+)+c(H+)=c()+2c()+3c()+c(OH-),B说法错误;
C.B点溶液中溶质为Na2HPO4,溶液pH=9.7,溶液显碱性,说明是水解大于电离,因此c(Na+)>c()>c()>c(),C说法错误;
D.等浓度的NaH2PO4和Na2HPO4的混合溶液中电荷守恒为:c(Na+)+c(H+)=c()+2c()+3c()+c(OH-),再根据物料守恒:2c(Na+)=3c()+3c()+3c(),将第一个等式乘以2再减去第二个等式:2c(H+)+c()=2c(OH+)+c()+3c(),D说法正确。
综上所述,答案为AD。
15. 在3个初始温度均为T℃的密闭容器中发生反应:2SO2(g)+O2(g)⇌2SO3(g)(正反应放热)。下列说法正确的是
A. a<1.6
B. b>0.8
C. 平衡时V正(SO2):v(I)”“=”或“<”)
(2)如图是一种用电解原理来制备H2O2,并用产生的H2O2处理废氨水的装置。
①为了不影响H2O2的产量,需要向废氨水中加入适量HNO3调节溶液的pH约为5,则所得溶液中c(NH)_________(填“>”“<”或“=”)c(NO)。
②Ir-Ru惰性电极吸附O2生成H2O2,其电极反应式为_______。
③理论上电路中每转移3mol电子,最多可以处理废氨水中溶质(以NH3计)的质量是______g。
【答案】 (1). Fe+8OH--6e-=FeO+4H2O (2). 氢气 (3). 阴 (4). < (5). < (6). O2+2H++2e−═H2O2 (7). 17
【解析】
【分析】
电解时,阳极铁电极反应为:Fe+8OH--6e-=FeO+4H2O,OH-通过右侧交换膜向右侧移动,则右侧为阴离子交换膜;阴极反应式为:2H2O+2e-=H2↑+2OH-,Na+
通过左侧离子交换膜向左侧移动,则左侧为阳离子交换膜,一段时间后,装置中部氢氧化钠溶液变稀,可以将左侧流出的氢氧化钠溶液补充到该装置中部,以保证装置连续工作,以此解答。
【详解】(1)①由分析可知,电解时,阳极铁电极反应为:Fe+8OH--6e-=FeO+4H2O,故答案为:Fe+8OH--6e-=FeO+4H2O;
②根据以上分析可知,左侧为阳离子交换膜,右侧为阴离子交换膜,阴极Cu电极反应式为:2H2O+2e-=H2↑+2OH-,所以生成氢气,故答案为:氢气;
③由分析可知,OH-通过右侧交换膜向右侧移动,则右侧为阴离子交换膜,阴极反应式为:2H2O+2e-=H2↑+2OH-,则阴极区氢氧根浓度增大,阴极区a%c(OH−),所以c(NH)”“<”或“=”)k逆增大的倍数。
②若在2L的密闭容器中充入1molCO和1molNO,在一定温度下达到平衡时,CO的转化率为40%,则_______。(保留一位小数)
(3)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步I2(g)⇌2I(g) (快反应)
第二步I(g)+N2O(g)→N2(g)+IO(g) (慢反应)
第三步IO(g)+N2O(g)→N2(g)+O2(g)+I2(g) (快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_____(填标号)。
A.N2O分解反应中:k值与是否含碘蒸气无关
B.第二步对总反应速率起决定作用
C.第二步活化能比第三步大
D.IO为反应的催化剂
【答案】 (1). 12△H3+5△H2-2△H1 (2). < (3). (4). B
【解析】
【详解】(1)已知:①6C(s)+5H2(g)+3N2(g)+9O2(g)=2C3H5(ONO2)3(1) △H1
②2H2(g)+O2(g)=2H2O(g) △H2
③C(s)+O2(g)=CO2(g) △H3
由盖斯定律:5×②+12×③-2×①得:4C3H5(ONO2)3(1)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)△H=12△H3+5△H2-2△H1;
(2)①该反应为放热反应,升高温度,平衡逆向移动,此时v正<v逆;
②若在1L的密闭容器中充入1mol CO和1mol NO,在一定温度下达到平衡时,CO的转化率为40%,根据题意有:
反应达平衡时,v正<v逆,即k正·c2(NO)·c2(CO)=k逆·c(N2)·c2(CO2),则;
(3)A.由含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数),所以N2O分解反应中:k值与是否含碘蒸气有关,选项A错误;
B.第二步是慢反应,则第二步对总反应速率起决定作用,选项B正确;
C.第二步是慢反应,则第二步活化能比第三步大,选项C错误;
D.IO为反应的中间产物,不是催化剂,选项D错误;
答案选B。
19. 碳热还原法广泛用于合金及材料的制备。下列是碳热还原制锰合金的三个反应,CO与CO2平衡分压比的自然对数(In[])与温度的关系如图所示(已知Kp是用平衡分压代替浓度计算所得的平衡常数,分压=总压×气体的物质的量分数)。
Ⅰ.Mn3C(s)+4CO2(g)⇌3MnO(s)+5CO(g) Kp(Ⅰ)
Ⅱ.Mn(s)+CO2(g)⇌MnO(s)+CO(g) Kp(Ⅱ)
Ⅲ.Mn3C(s)+CO2(g)⇌3Mn(s)+2CO(g) Kp(Ⅲ)
回答下列问题:
①△H>0的反应是_______(填“I”“Ⅱ”或“Ⅲ”)
②1200K时在一体积为2L的恒容密闭容器中有17.7gMn3C(s)和0.4molCO2,只发生反应I,5min后达到平衡,此时CO的浓度为0.125mol·L-1,则0~5min内V(CO2)=_____mol·L-1·min-1。
③在一体积可变的密闭容器中加入一定量的Mn(s)并充入一定量的CO2(g),只发生反应Ⅱ,下列能说明反应II达到平衡状态的是__________(填标号)。
A.容器的体积不再改变
B.固体的质量不再改变
C.气体的总质量不再改变
④向恒容密闭容器中加入Mn3C并充入0.1molCO2,若只发生反应Ⅲ。则在A点反应达到平衡时,容器的总压为akPa,CO2的转化率为_______(保留一位小数),A点对应温度下的Kp(Ⅲ)=________。
【答案】 (1). Ⅲ (2). 0.02 (3). BC (4). 33.3% (5). 0.5akPa
【解析】
【分析】
①随温度升高,In[增大,说明升高温度CO的浓度增大,平衡正向移动;
②据公式V(CO2)=进行计算;
③根据平衡标志分析;
④利用“三段式”计算CO2的转化率、Kp(Ⅲ);
【详解】①Ⅰ、Ⅱ随温度升高,In[减小,说明升高温度CO的浓度减小,平衡逆向移动;反应Ⅲ随温度升高,In[增大,说明升高温度CO的浓度增大,平衡正向移动;所以△H>0的反应是Ⅲ;
②1200K时在一体积为2L的恒容密闭容器中有17.7gMn3C(s)和0.4molCO2,只发生反应I,5min后达到平衡,此时CO的浓度为0.125mol·L-1,则CO2浓度减小了0.1 mol·L-1,则0~5min内V(CO2)= 0.02mol·L-1·min-1。
③A. Mn(s)+CO2(g)⇌MnO(s)+CO(g)反应前后气体物质的量不变,体积是恒量,容器的体积不再改变,反应不一定平衡,故不选A;
B.固体的质量不再改变,说明CO2浓度不变,反应一定达到平衡状态,故选B;
C. Mn(s)+CO2(g)⇌MnO(s)+CO(g),有固体参与反应,气体总质量是变量,气体的总质量不再改变,反应一定达到平衡状态,故选C;
选BC。
④
A点In[,则=1,说明n(CO)= n(CO2),即0.1-x=2x,x=,CO2的转化率为 ;A点对应温度下的Kp(Ⅲ)=
kPa;
【点睛】本题考查化学平衡判断、化学平衡计算,明确化学平衡常数、平衡转化率概念是解题关键,熟悉温度对化学平衡移动的影响,注意用根据“变量不变”判断反应是否达到平衡状态。
20. (1)25℃时,部分物质的电离平衡常数如表所示:
①0.1mol·L-1NH4ClO溶液中离子浓度由大到小的顺序是_______,ClO-水解反应的平衡常数Kh=_____(保留两位有效数字)。
②少量SO2通入过量的Na2CO3溶液中,发生反应的离子方程式为________。
(2)某小组同学探究饱和NaClO和KAl(SO4)2溶液混合反应的实验。打开活塞向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀。出现上述现象的原因是_________(请用反应的离子方程式表示)。
(3)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+) ·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至________。
(4)用沉淀滴定法快速测定NaI等碘化物溶液中c(I-),实验过程包括准备标准溶液和滴定待测溶液。
I.准备标准溶液
a.准确称取AgNO3基准物4.2468 g(0.0250mol)后,配制成250mL标准溶液,放在棕色试剂瓶中避光保存,备用。
b.配制并标定100 mL 0.100 0mol·L-1NH4SCN标准溶液,备用。
II.滴定主要步骤
a.取待测NaI溶液25.00mL于锥形瓶中。
b.加入25.00mL 0.100 0mol·L-1 AgNO3溶液(过量),使I-完全转化为AgI沉淀。
c.加入NH4Fe(SO4)2溶液作指示剂。
d.用0.100 0mol·L-1 NH4SCN溶液滴定过量的Ag+,使其恰好完全转化为AgSCN沉淀后,体系出现淡红色,停止滴定。
e.重复上述操作两次。三次测定数据如表:
f.数据处理。
回答下列问题:
①滴定应在pH<0.5的条件下进行,其原因是________
②测得c(I-)=_________mol·L-1。
③在滴定管中装入NH4SCN标准溶液的前一步,应进行的操作为________。
④下列操作对c(I-)测定结果的影响偏高的是__________
A.若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出
B.若在滴定终点读取滴定管刻度时,俯视标准液液面
C.用滴定管量取25.00mL待测NaI溶液,读取初始液面示数时有气泡,后来无气泡。
【答案】 (1). c()>c(ClO-)>c(OH-)>c(H+) (2). 3.3×10-7 (3). H2O+SO2+2=+2 (4). Al3++3ClO-+3H2O=Al(OH)3↓+3HClO (5). 5 (6). 抑制铁离子水解 (7). 0.06 (8). 用NH4SCN标准溶液进行润洗 (9). AB
【解析】
【详解】(1)①根据表中数据可知,氨水的电离程度大于次氯酸的,则NH4ClO为相对的强碱弱酸盐,溶液显碱性,溶液中发生少量的水解,则铵根离子浓度大于次氯酸根离子浓度,氢氧根离子浓度大于氢离子浓度,离子浓度的大小顺序为c()>c(ClO-)>c(OH-)>c(H+);Kh===3.3×10-7;
②根据表中数据,亚硫酸的酸性大于碳酸,亚硫酸氢根离子的酸性弱于碳酸,则少量二氧化硫与碳酸根离子反应生成亚硫酸根离子和碳酸氢根离子,离子方程式为H2O+SO2+2=+2;
(2)向烧瓶中的NaClO加入饱和KAl(SO4)2溶液,产生大量的白色胶状沉淀,Al3+与ClO-
发生相互促进的水解反应,生成次氯酸和氢氧化铝沉淀,离子方程式为Al3++3ClO-+3H2O=Al(OH)3↓+3HClO;
(3)根据Ksp=c(Cr3+)·c3(OH-),c(Cr3+)=10-5mol·L-1,则c3(OH-)==10-27,c(OH-)=10-9mol/L,c(H+)==10-5mol/L,pH=5;
(4)①溶液中的铁离子易发生水解反应,为防止铁离子水解影响滴定终点,故滴定应在pH<0.5的条件下进行;
②根据表中数据,第一组数据偏差较大,舍去不用,二、三组数据的平均值为10.00mL,根据题目信息可知,n(AgNO3)=n(NaI)+n(NH4SCN),25.00mL×0.100 0mol·L-1=c(NaI) ×25.00mL+0.100 0mol·L-1×10.00mL,c(NaI)=0.06mol/L,即c(I-)=0.06mol/L;
③装入NH4SCN标准溶液应避免浓度降低,应先用标准液进行润洗;
④A.若在配制AgNO3标准溶液时,烧杯中的溶液有少量溅出,导致溶质的物质的量减小,配制溶液的浓度偏小,则消耗的n(NH4SCN)偏小,测定c(I-)偏高,A符合题意;
B.若在滴定终点读取滴定管刻度时,俯视标准液液面,则读取NH4SCN的体积偏小,n(NH4SCN)偏小,测定c(I-)偏高,B符合题意;
C.用滴定管量取25.00mL待测NaI溶液,读取初始液面示数时有气泡,后来无气泡,则n(NaI)减小,滴定时,需要的NH4SCN的体积偏大,n(NH4SCN)偏大,测定c(I-)偏低,C与题意不符;
答案为AB。
【点睛】溶液中存在n(AgNO3)=n(NaI)+n(NH4SCN),根据关系式进行判断c(I-)。