2017-2018学年内蒙古太仆寺旗宝昌一中高二下学期期中考试化学试题 解析版
2017-2018学年内蒙古太仆寺旗宝昌一中高二下学期期中考试化学试题
考试时间:100分钟;命题人:管绪彬
题号
一
二
总分
得分
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将选择题答案写在第Ⅱ卷上
第I卷(选择题)
单选,每小题3分
评卷人
得分
一、选择题
1.下列过程是非自发的是( )
A.水由高处向低处流 B.天然气的燃烧
C.铁在潮湿的空气中生锈 D.水在室温下结冰
2.碳酸铵(NH4)2CO3在室温下就能自发的分解产生氨气,对其说法正确的是( )
A.碳酸铵分解是因为生成了易挥发的气体,使体系的熵增大
B.碳酸铵分解是因为外界给予了能量
C.碳酸铵分解是吸热反应,根据能量判据不能自发分解
D.碳酸盐都不稳定,都能自发分解
3.下列关于焓判据和熵判据的说法中,不正确的是( )
A.放热的自发过程可能是熵减小的过程,吸热的自发过程一定为熵增加的过程
B.由焓判据和熵判据组合成的复合判据,将更适合于所有的过程
C.在室温下碳酸钙的分解反应不能自发进行,但同样是这个吸热反应在较高温度(1200 K)下则能自发进行
D.放热过程(ΔH<0)或熵增加(ΔS>0)的过程一定是自发的
4.判断强弱电解质的标准是( )
A.导电能力 B.相对分子质量
C.电离程度 D.溶解度
5.下列有关“电离平衡”的叙述中正确的是( )
A.电解质在溶液里达到电离平衡时,分子的浓度和离子的浓度相等
B.达到电离平衡时,由于分子和离子的浓度不再发生变化,所以说电离平衡是静态平衡
C.电离平衡是相对的、暂时的,外界条件改变时,平衡就会发生移动
D.电解质达到电离平衡后,各种离子的浓度相等
6.将1 mol冰醋酸加入到一定量的蒸馏水中最终得到1 L溶液。下列各项中,表明已达到电离平衡状态的是( )
A.醋酸的浓度达到1 mol·L-1
B.H+的浓度达到0.5 mol·L-1
C.醋酸分子的浓度、醋酸根离子的浓度、H+的浓度均为0.5 mol·L-1
D.醋酸分子电离成离子的速率和离子重新结合成醋酸分子的速率相等
7.c(OH-)相同的氢氧化钠溶液和氨水,分别用蒸馏水稀释至原体积的m倍和n倍,若稀释后两溶液的c(OH-)仍相同,则m和n的关系是( )
A.m>n B.m=nC.m
c(OH-)的操作是( )
A.向水中投入一小块金属钠 B.将水加热煮沸
C.向水中通入二氧化碳气体 D.向水中加食盐晶体
11.向纯水中加入少量NaHSO4,在温度不变时,溶液中( )
A.c(H+)/c(OH-)增大 B.c(H+)减小
C.水中c(H+)与c(OH-)的乘积增大 D.c(OH-)增大
12.下列关于水的离子积常数的叙述中,正确的是( )
A.因为水的离子积常数的表达式是KW=c(H+)·c(OH-),,所以KW随溶液H+和OH-浓度的变化而变化
B.水的离子积常数KW与水的电离平衡常数K电离是同一个物理量
C.水的离子积常数仅仅是温度的函数,随着温度的变化而变化
D.水的离子积常数KW与水的电离平衡常数K电离是两个没有任何关系的物理量
13.下列关于溶液pH的说法正确的是( )
A.pH是表示溶液酸碱性的多种方式中的一种
B.只有c(H+)和c(OH-)都小于1mol/L的稀溶液,才有pH
C.pH<7的溶液一定显酸性
D.用试纸测定溶液的pH时,需要将pH试纸进入溶液后取出,再与比色卡对比
14.下列叙述正确的是( )
A.100 ℃纯水的pH=6,所以水在100 ℃时呈酸性
B.pH=3的盐酸溶液,稀释至10倍后pH>4
C.0.2 mol·L-1的醋酸,与等体积水混合后pH=1
D.常温时,pH=3的盐酸与pH=11的氢氧化钠等体积混合后pH=7
15.在室温下等体积的酸和碱的溶液,混合后pH一定小于7的是( )
A.pH=3的硝酸和pH=11的氢氧化钾溶液
B.pH=3的盐酸和pH=11的氨水
C.pH=3的硫酸和pH=11的氢氧化钠溶液
D.pH=3的醋酸和pH=11的氢氧化钡溶液
16.在25℃时,某稀溶液中由水电离产生的c(OH-)=10-10mol/L。下列有关该溶液的叙述正确的是( )
A.该溶液一定呈酸性
B.该溶液中的c(H+)可能等于10-5
C.该溶液的pH可能为4,可能为10
D.该溶液有可能呈中性
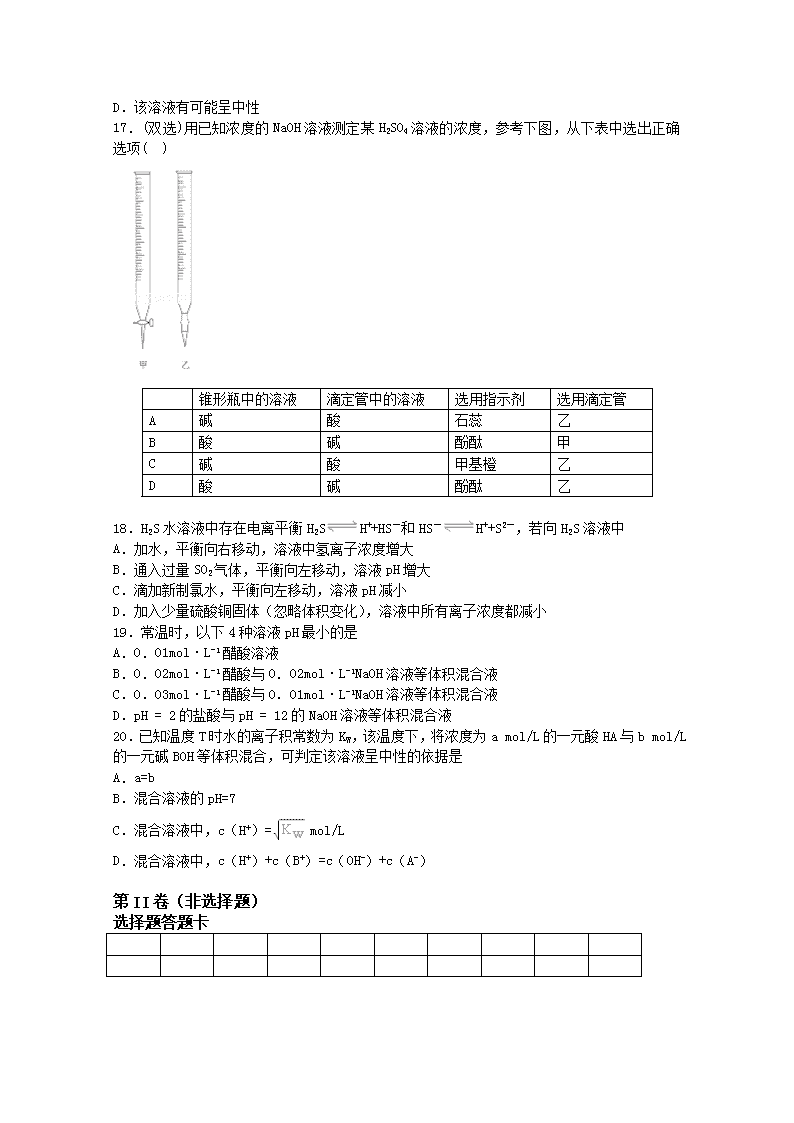
17.(双选)用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考下图,从下表中选出正确选项( )
锥形瓶中的溶液
滴定管中的溶液
选用指示剂
选用滴定管
A
碱
酸
石蕊
乙
B
酸
碱
酚酞
甲
C
碱
酸
甲基橙
乙
D
酸
碱
酚酞
乙
18.H2S水溶液中存在电离平衡H2SH++HS-和HS-H++S2-,若向H2S溶液中
A.加水,平衡向右移动,溶液中氢离子浓度增大
B.通入过量SO2气体,平衡向左移动,溶液pH增大
C.滴加新制氯水,平衡向左移动,溶液pH减小
D.加入少量硫酸铜固体(忽略体积变化),溶液中所有离子浓度都减小
19.常温时,以下4种溶液pH最小的是
A.0.01mol·L-1醋酸溶液
B.0.02mol·L-1醋酸与0.02mol·L-1NaOH溶液等体积混合液
C.0.03mol·L-1醋酸与0.01mol·L-1NaOH溶液等体积混合液
D.pH = 2的盐酸与pH = 12的NaOH溶液等体积混合液
20.已知温度T时水的离子积常数为KW,该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,可判定该溶液呈中性的依据是
A.a=b
B.混合溶液的pH=7
C.混合溶液中,c(H+)=mol/L
D.混合溶液中,c(H+)+c(B+)=c(OH-)+c(A-)
第II卷(非选择题)
选择题答题卡
评卷人
得分
二、填空题
21.在a、b两支试管中,分别装入形态相同、质量相等的锌粒,然后向两试管中分别加入相同物质的量浓度、相同体积的稀盐酸和稀醋酸。填写下列空白:
(1)a、b两支试管中的现象;相同点是________;不同点是________;原因是_________。
(2)a、b两支试管中生成气体的体积开始时是V(a)________V(b);反应完毕后生成气体的总体积是V(a)________V(b),原因是________________。
22.勒夏特列原理适用于许多平衡体系。试用该原理分析水的电离平衡(H2OH++OH-),填写下列表格(除④外,其余都假设溶液温度不变):
改变条件
平衡移动方向
c(H+)的变化
c(OH-)的变化
Kw
①加入醋酸
②加入烧碱
③加入CH3COONa
④升高温度
23.(1)常温下,将pH=10和pH=12的NaOH溶液以1∶1的体积比混合,则混合后所得溶液的pH约为________。
(2)0.2 mol·L-1 NaHSO4和0.1 mol·L-1 BaCl2溶液按等体积混合后,则溶液的pH等于________。
(3)用pH=4和pH=11的强酸和强碱混合,使pH=10,则两溶液的体积比为________。
24.某温度(T℃)时,测得0.01mol·L-1的NaOH溶液的pH为11,该温度下水的KW=。该温度(填“大于”、“小于”或“等于”)25℃,其理由是。
此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合,通过计算填写以下不同情况时两溶液的体积比:
(1)若所得混合溶液为中性,且a=12,b=2,则Va:Vb=________。
(2)若所得混合溶液为中性,且a+b=12,则Va:Vb=________。
(3)若所得混合溶液的pH=10,且a=12,b=2,Va:Vb=________9。
参考答案
1.D
【解析】由高能量转向低能量,由有序变为无序,一般讲都是自发过程。自然界中水由高处向低处流、天然气的燃烧、铁在潮湿的空气中生锈、冰在室温下融化,都是自发过程,其逆过程都是非自发过程。答案选D。
2.A
【解析】(NH4)2CO3的分解为吸热反应,而吸热反应不易自发进行;根据焓变与熵变对化学反应的共同影响,该反应熵值一定增大。答案选A。
3.D
【解析】反应自发进行的判断依据是△H-T△S<0,自发进行的反应也需要一定条件才可以发生,放热的自发过程,△H<0,△S可能小于0也可能大于0,所以,放热的自发过程可能是熵减小的过程,吸热的自发过程,△H>0,因T>0,须△H-T△S<0,取决于△S>0,所以吸热的自发过程一定为熵增加的过程,故A正确;化学反应能否自发进行,取决于焓变和熵变的综合判据,当△G=△H-T?△S<0时,反应能自发进行,当△H<0,△S>0时,△G=△H-T△S<0,一定能自发进行,而△H>0,△S<0时不能自发进行,△H>0,
△S>0或△H<0,△S<0能否自发进行,取决于反应的温度,所以,由能量判据和熵判据组合成的复合判据,将更适合于所有的过程,故B正确;在室温下碳酸钙的分解反应不能自发进行,△H-T△S>0,因△H>0,△S>0所以当反应温度高到一定程度,T△S>△H,此时△H-T△S<0,反应能自发进行,故C正确;当△G=△H-T?△S<0时,反应能自发进行,当△H<0,△S>0时,△G=△H-T?△S<0,一定能自发进行,而△H>0,△S<0时不能自发进行,△H>0,△S>0或△H<0,△S<0能否自发进行,取决于反应的温度,故D错误;故选D。
4.C
【解析】依据强弱电解质的定义可知,它们之间最根本的区别在于它们在水溶液中的电离程度的大小,答案选C。
5.C
【解析】达到电离平衡时,分子浓度和离子浓度均不变,但未必相等,A项错误;达到电离平衡时,分子仍然要电离为离子,离子也要结合为分子,只是二者速率相等,B项错误;电离平衡是动态平衡,随着外界条件的改变而发生移动,C项正确;达到电离平衡时,各离子浓度不变,但不一定相等,D项错误。
6.D
【解析】在未电离时c(CH3COOH)=1 mol·L-1,当醋酸、H+、CH3COO-的浓度不再变化时(但此时三者的浓度不一定是0.5 mol·L-1),醋酸的电离达到平衡状态,故A、B、C均错。依据平衡状态的标志即电离成离子的速率与离子结合成分子的速率相等,可知D项正确。
【答案】C
【解析】加水稀释时一水合氨的电离平衡向右移动,NaOH溶液加水稀释至原体积的m倍,c(OH-)变为原来的,而氨水稀释至原体积的n倍时,c(OH-)大于原来的,所以mc(H+),A项错误;加热促进水的电离,但c(H+)=c(OH-),B项错误;二氧化碳与水反应生成碳酸,碳酸电离出H+则溶液中的c(H+)>c(OH-),C项正确;加食盐对水的电离平衡没有影响,c(H+)=c(OH-),D项错误。
11.A
【解析】NaHSO4=Na++H++SO42-溶液呈酸性,c(H+)增大,c(OH-)减小,故A正确。
12.C
【解析】水的离子积常数KW=K电离·c(H2O),一定温度下K电离和c(H2O)都是不变的常数,所以KW仅仅是温度的函数。水的离子积常数的表达式是KW=c(H+)·c(OH-),只与温度有关溶液中H+的浓度变大,OH-的浓度就变小,反之亦然。
13.A
【解析】表示溶液酸碱性的方式有多种:如pH、c(H+)等,A项正确;任何溶液都可以用pH=﹣求其pH,只是当c(H+)和c(OH-)都小于1mol/L的稀溶液,用pH表示比较直观方便,B项错误;pH<7的溶液不一定显酸性,可能显中性,如100℃的水的pH=6,仍显中性,C项错误;用试纸测定溶液的pH时,需将试纸放于表面面上,用玻璃棒蘸取溶液滴于试纸中部,试纸变色后再与比色卡对比,D项错误。
14.D
【解析】纯水不管其pH为多少都是呈中性,A项错误;盐酸是强酸,所以每稀释10倍pH增大1,故pH=4,B项错误;将0.2 mol·L-1的醋酸,与等体积水混合后,溶液的浓度变为0.1 mol·L-1,但由于醋酸是弱酸,所以pH大于1,C项错误;盐酸与氢氧化钠恰好完全反应,所以呈中性,D项正确。
15.D
【解析】A项,HNO3+KOHKNO3+H2O,二者完全反应,溶液呈中性;B项,NH3·H2O是弱电解质,HCl+NH3·H2ONH4Cl+H2O,NH3·H2O过量,溶液呈碱性,pH>7;C项,H2SO4+2NaOHNa2SO4+2H2O,二者完全反应,溶液呈中性;D中,CH3COOH是弱电解质,二者反应后CH3COOH过量,溶液呈酸性,pH<7。
16.C
【解析】由水电离出来的c(OH-)=10-10,故溶液中的c(H+)水=c(OH-)水=1×10-10mol/L,若溶液中的c(OH-)=10-10,则该溶液中的c(H+)应等于10-4,则溶液的pH应为4,溶液呈酸性;若溶液中的c(H+)=10-10,则溶液的pH应为10,(该溶液中的c(OH-)应等于10-4),溶液呈碱性;溶液可能是呈酸性也可能是呈碱性,但溶液不可能是pH=5的溶液,当然也不可能呈中性。
17.CD
【解析】本题考查中和滴定中酸式滴定管、碱式滴定管和酸碱指示剂的选择。甲为酸式滴定管,乙为碱式滴定管。酸性溶液、强氧化性溶液(如KMnO4溶液)一般装在酸式滴定管中,碱性溶液一般装在碱式滴定管中。指示剂的选择比较复杂,一般情况下,强碱滴定强酸用酚酞指示剂,强酸滴定强碱用甲基橙或酚酞指示剂。当指示剂可以有多种选择时,选择的指示剂最好是到达滴定终点时由浅变深发生变化。中和滴定时,一般情况下是把已知物质的量浓度的标准溶液滴入待测的未知浓度的溶液中,但把未知物质的量浓度的溶液滴入已知物质的量浓度的溶液中,只要操作正确,也可以求得待测溶液浓度。在中和滴定实验中,已知浓度的标准溶液是放在锥形瓶中还是滴定管中是人为规定的,只要指示剂和滴定管能够和实验要求相符合(指示剂变色范围在终点pH突变范围之内,滴定管不过大或过小)即可。注意:指示剂变色要灵敏,酸式滴定管不能盛放碱性溶液,碱式滴定管不能盛放强氧化性溶液及酸性溶液等。
18.C
【解析】
试题分析:A.加水稀释促进硫化氢电离,但氢离子浓度减小,A项错误;B.二氧化硫和硫化氢反应方程式为SO2+2H2S=3S↓+2H2O,通入过量二氧化硫平衡向左移动,二氧化硫和水反应方程式为H2O+SO2=H2SO3,亚硫酸酸性大于氢硫酸,所以溶液的pH减小,B项错误;C.氯气和硫化氢反应方程式为Cl2+H2S=S↓+2HCl,通入氯气平衡向左移动,盐酸的酸性大于氢硫酸,所以溶液的pH减小,C项正确;D.加入硫酸铜溶液发生反应CuSO4+H2S=H2SO4+CuS↓,硫酸的酸性大于氢硫酸,所以氢离子浓度增大,D项错误;答案选C。
【考点定位】考查弱电解质在水溶液中的电离平衡。
【名师点睛】本题考查弱电解质在水溶液中的电离平衡,明确离子间发生的反应是解本题关键,注意加水稀释时,虽然促进氢硫酸电离,但氢离子浓度减小,溶液的pH增大,为易错点。①加水稀释促进弱电解质电离;②硫化氢和二氧化硫反应生成硫和水,亚硫酸酸性大于氢硫酸;③氯气和硫化氢反应生成硫和盐酸,盐酸酸性大于氢硫酸;④硫化氢和硫酸铜反应生成硫酸和硫化铜,硫酸酸性大于氢硫酸
19.A
【解析】
试题分析:A.醋酸是弱电解质,所以0.01mol/L的醋酸溶液中氢离子浓度小于0.01mol/L;B.0.02mol/L醋酸与0.02mol/LNaOH溶液等体积混合,二者恰好反应生成CH3COONa,醋酸钠是强碱弱酸盐,CH3COO-因水解导致溶液呈碱性,氢离子浓度小于10-7mol/L;C.0.03mol/L醋酸与0.01mol/LNaOH溶液等体积混合,溶液中的溶质是0.01mol/L的醋酸和0.005mol/L的醋酸钠,氢离子浓度小于0.01mol/L,由于CH3COO-的抑制作用,氢离子浓度小于A中氢离子浓度;D.pH=2的盐酸中氢离子浓度为0.01mol/L,pH=12的NaOH溶液中氢离子浓度为0.01mol/L,二者等体积混合,恰好反应生成强酸强碱盐,其溶液呈中性,则氢离子浓度等于10-7mol/L;所以氢离子浓度最大的是A,则pH最小的是A,答案选A。
【考点定位】考查溶液酸碱性的判断。
【名师点睛】本题考查溶液酸碱性的判断,明确溶液中的溶质及溶质的性质即可解答,难度中等。常温下,溶液中pH最小说明溶液中氢离子浓度最大,根据溶液中溶质结合氢离子浓度大小判断即可。
20.C
【解析】
试题分析:A.因酸碱的强弱未知,a=b,只能说明酸碱恰好完全反应,但如为强酸弱碱盐或强碱弱酸盐,则溶液不呈中性,A项错误;B.因温度未知,则pH=7不一定为中性,B项错误;C.混合溶液中,c(H+)=mol/L,根据c(H+)×c(OH-)=KW,可知溶液中c(H+)=c(OH-)=mol/L,溶液呈中性,C项正确;D.任何溶液都存在电荷守恒,即c(H+)+c(B+)=c(OH-)+c(A-),不能确定溶液的酸碱性,D项错误;答案选C。
【考点定位】考查酸碱混合的定性判断。
【名师点睛】本题考查酸碱混合的定性判断,题目难度中等,注意溶液呈中性应存在c(H+)=c(OH-)。由于温度未知,且酸碱的强弱未知,不能根据pH以及酸碱的物质的量关系判断溶液的酸碱性。温度T时水的离子积常数为KW,浓度为a mol/L的一元酸HA与b mol/L的一元碱BOH等体积混合,若溶液呈中性,反应后的溶液中应存在c(H+)=c(OH-)=mol/L。
21.(1)都产生无色气泡 a中反应速率较快 盐酸是强酸,醋酸是弱酸,盐酸溶液中c(H
+)大
(2)> = 开始反应时,盐酸溶液中H+浓度较大,但二者的H+的总的物质的量相等
【解析】
22.①向左 变大 变小 不变 ②向左 变小 变大 不变
③向右 变小 变大 不变 ④向右 变大 变大 变大
【解析】向纯水中加入醋酸,醋酸电离出H+;抑制水的电离,平衡向左移动,OH-浓度减小,H+浓度增大,温度不变。KW不变;同理加入烧碱,平衡左移,c(OH-)增大,c(H+)减小,KW不变;加入CH3COONa后,CH3COO-与H+结合生成弱电解质CH3COOH;c(H+)减小,水的电离平衡项右移动,c(OH-)增大,KW不变;弱电解质的电离是吸热反应,升高温度,平衡向吸热方向移动,c(H+)、c(OH-)均增大,水的离子积变大。
23.(1)11.7(2)1(3)9∶2
【解析】欲求混合后溶液的pH,应先判断混合后溶液的酸碱性。若呈碱性,应先求溶液中c(OH-),再求c(H+),而后计算pH;若呈酸性,可直接求出混合后c(H+),再计算pH。由题意可得:
(1)c(OH-)==≈5×10-3
c(H+)·c(OH-)=KW=1×10-14
c(H+)==2×10-12
pH=-lgc(H+)=-lg(2×10-12)=12-0.3=11.7
(2)NaHSO4为强电解质
c(H+)==0.1(mol·L-1)
pH=-lgc(H+)=1
(3)混合后溶液呈碱性,则
10-4=
整理可得:2×10-4V(酸)=9×10-4V(碱)
所以,=
24.10-22;大于;水的电离是吸热的,升温时水的电离平衡正向移动,KW增大,因该温度下的KW大于25℃时水的KW=1×10-14,所以该温度大于25℃
(1)1:10;(2)10:1;(3)1:9。
【解析】
试题分析:0.01mol•L-1的NaOH溶液的pH为11,则氢离子浓度=10-11 mol/L,氢氧化钠是强电解质完全电离,所以溶液中氢氧根离子浓度是0.01mol/L,则Kw=c(H+).c(OH-)=0.01×10-11=10-13,水的电离是吸热的,升温时水的电离平衡正向移动,KW增大,因该温度下的KW大于25℃时水的KW=1×10-14,所以该温度大于25℃,故答案为:10-13;大于;水的电离是吸热的,升温时水的电离平衡正向移动,KW增大,因该温度下的KW大于25℃时水的KW=1×10-14,所以该温度大于25℃;
(1)若所得混合溶液为中性,且a=12,b=2,因c(OH-)×Va=c(H+)×Vb,a=12,b=2,则0.1×Va=0.01Vb,则Va:Vb=1:10故答案为:1:10;
(2)若所得混合液为中性,且a+b=12,Va:Vb==1013-a-b=10,则Va:Vb=10:1,故答案为:10:1
(3)若所得混合溶液的pH=10,碱过量,且a=12,b=2,则溶液中c(OH-)==0.001,则Va:Vb=1:9;故答案为:1:9。
【考点定位】考查pH的简单计算
【名师点晴】本题考查了水的离子积常数的计算、酸碱混合的计算,注意水的离子积常数只与温度有关,与溶液是酸碱性无关,为易错点。明确该温度下的Kw及pH与浓度的换算是解答本题的关键,注意酸碱反应的实质。