- 2024-01-10 发布 |
- 37.5 KB |
- 6页

申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
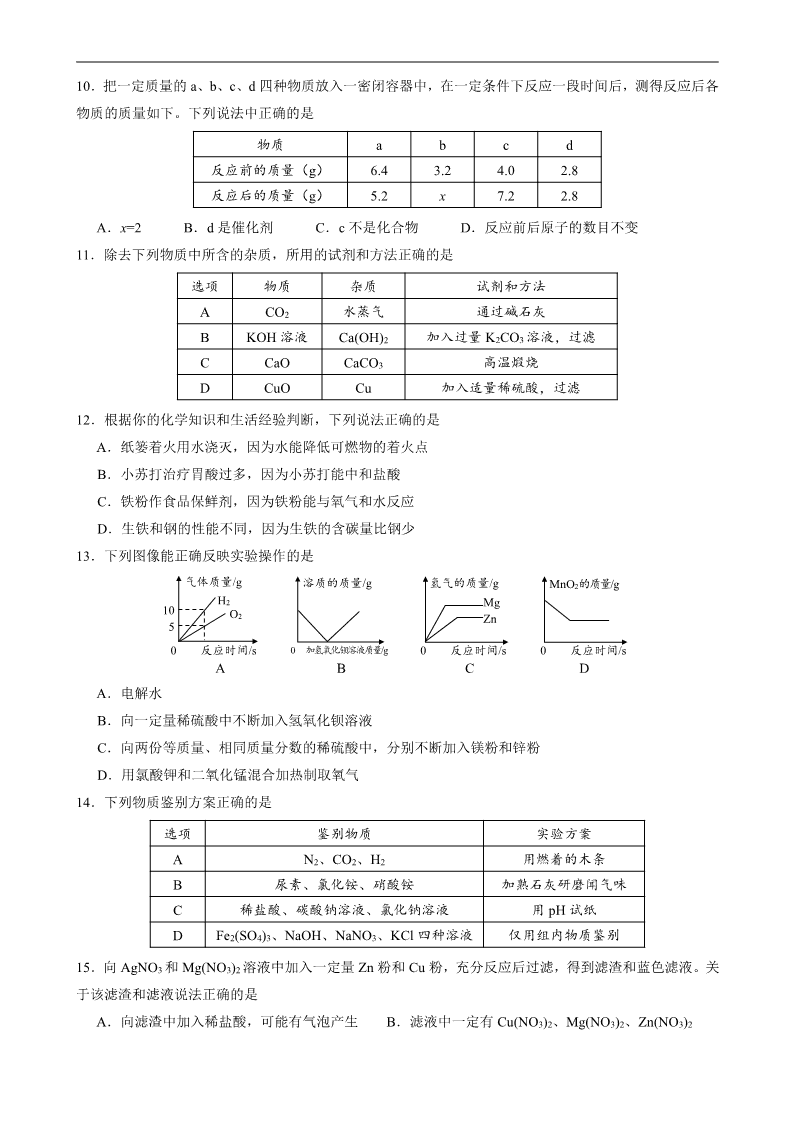
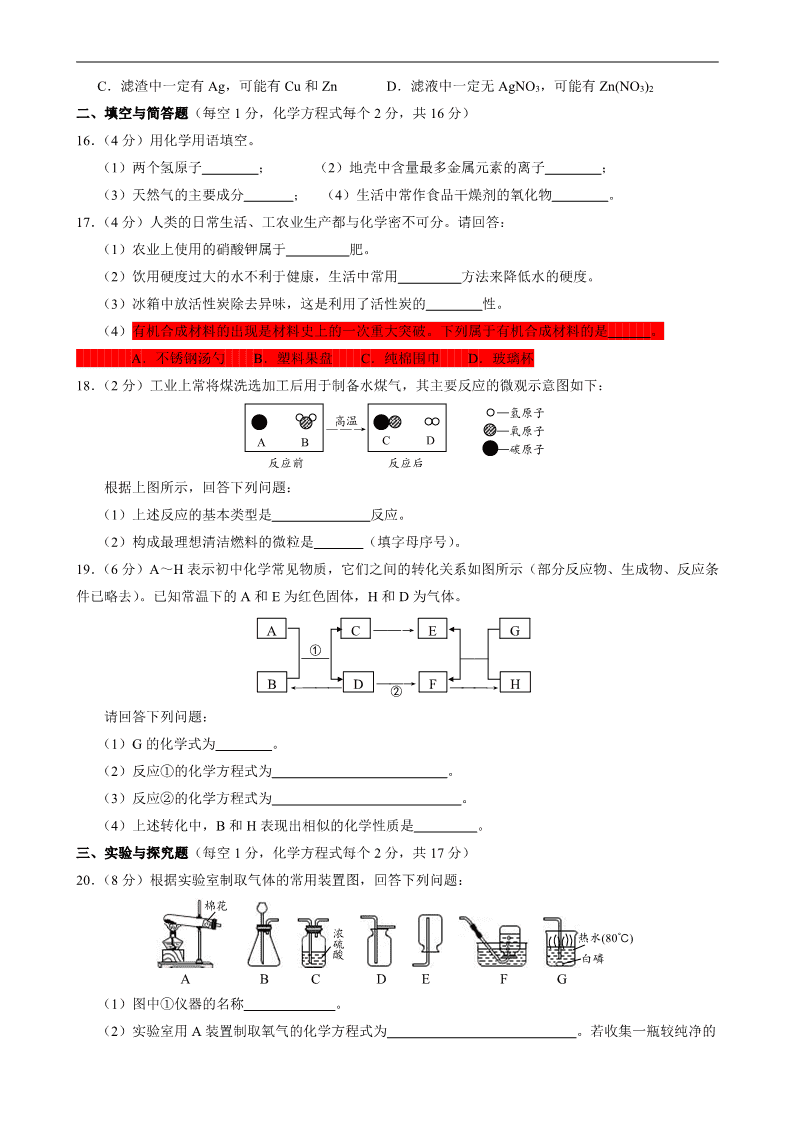
2019年全国各地中考化学试题-甘肃省天水(含答案)
2019 年甘肃省天水市初中毕业与升学学业考试(中考)试卷 物理 化学(化学部分) (满分 70 分) 可能用到的相对原子质量:H—1 C—12 O—16 Na—23 Cl—35.5 一、选择题(每小题只有一个....选项符合题意。每小题 2 分,共 30 分) 1.下列属于物理变化的是 A.油锅着火 B.米饭变馊 C.洗洁精除油 D.菜刀生锈 2.为建设天蓝地绿水净的美丽天水,下列做法不合理...的是 A.禁止燃放烟花爆竹 B.生活垃圾就地焚烧处理 C.工业废水处理达标后再排放 D.废旧金属回收再利用 3.下列物质属于纯净物的是 A.石灰石 B.食醋 C.碘酒 D.冰水 4.下列基本实验操作,你认为错误..的是 —浓硫酸 水 A.稀释浓硫酸 B.倾倒液体 C.蒸发盐水 D.检查气密性 5.化学与生活密切相关。下列做法有益于身体健康的是 A.饮用工业酒精勾兑的白酒 B.吃水果和蔬菜补充维生素 C.不吃油脂减肥 D.霉变大米经淘洗后可食用 6.空气是一种宝贵的自然资源,由多种物质组成。下列说法错误..的是 A.氦气可用来填充探空气球 B.氮气充入食品包装袋防腐 C.二氧化碳是植物光合作用的基本原料 D.氧气可用作火箭发射的燃料 7.静静发现炒菜所用的食盐为加碘食盐。经查阅资料可知碘元素在元素周期表中有下图所示信息。下列 说法正确的是 A.缺碘易患贫血症 B.碘的相对原子质量为 126.90g C.x 的值可能为 7 D.加碘食盐中的“碘”指原子 8.甲醛(CH2O)是一种无色、有刺激性气味的气体,对人体有害。不合格的家居用品或装修材料中常常 含有甲醛,损害人体健康。下列说法正确的是 A.一个甲醛分子由 4 个原子构成 B.甲醛燃烧前后各元素的化合价不变 C.甲醛是氧化物 D.甲醛分子中的原子都由质子、中子和电子构成 9.甲、乙两种固体(不含结晶水)的溶解度曲线如图所示。下列说法正确的是 A.t1℃时,甲、乙饱和溶液溶质的质量分数相等 B.乙中含有少量甲时,可用降温结晶法提纯乙 C.t2℃时,将 50g 甲加入 50g 水中,可得到 100g 溶液 D.t2℃时的甲、乙饱和溶液分别降温到 t1℃时,析出晶体的质量甲大于乙 53 I 碘 126.90 2 81818 x+53 甲 乙 0 t1 t2 温度/℃ 溶解度/g 80 10.把一定质量的 a、b、c、d 四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得反应后各 物质的质量如下。下列说法中正确的是 物质 a b c d 反应前的质量(g) 6.4 3.2 4.0 2.8 反应后的质量(g) 5.2 x 7.2 2.8 A.x=2 B.d 是催化剂 C.c 不是化合物 D.反应前后原子的数目不变 11.除去下列物质中所含的杂质,所用的试剂和方法正确的是 选项 物质 杂质 试剂和方法 A CO2 水蒸气 通过碱石灰 B KOH 溶液 Ca(OH)2 加入过量 K2CO3 溶液,过滤 C CaO CaCO3 高温煅烧 D CuO Cu 加入适量稀硫酸,过滤 12.根据你的化学知识和生活经验判断,下列说法正确的是 A.纸篓着火用水浇灭,因为水能降低可燃物的着火点 B.小苏打治疗胃酸过多,因为小苏打能中和盐酸 C.铁粉作食品保鲜剂,因为铁粉能与氧气和水反应 D.生铁和钢的性能不同,因为生铁的含碳量比钢少 13.下列图像能正确反映实验操作的是 0 反应时间/s 气体质量/g H2 O210 5 0 加氢氧化钡溶液质量/g 溶质的质量/g Mg Zn 0 反应时间/s 氢气的质量/g MnO2的质量/g 0 反应时间/s A B C D A.电解水 B.向一定量稀硫酸中不断加入氢氧化钡溶液 C.向两份等质量、相同质量分数的稀硫酸中,分别不断加入镁粉和锌粉 D.用氯酸钾和二氧化锰混合加热制取氧气 14.下列物质鉴别方案正确的是 选项 鉴别物质 实验方案 A N2、CO2、H2 用燃着的木条 B 尿素、氯化铵、硝酸铵 加熟石灰研磨闻气味 C 稀盐酸、碳酸钠溶液、氯化钠溶液 用 pH 试纸 D Fe2(SO4)3、NaOH、NaNO3、KCl 四种溶液 仅用组内物质鉴别 15.向 AgNO3 和 Mg(NO3)2 溶液中加入一定量 Zn 粉和 Cu 粉,充分反应后过滤,得到滤渣和蓝色滤液。关 于该滤渣和滤液说法正确的是 A.向滤渣中加入稀盐酸,可能有气泡产生 B.滤液中一定有 Cu(NO3)2、Mg(NO3)2、Zn(NO3)2 C.滤渣中一定有 Ag,可能有 Cu 和 Zn D.滤液中一定无 AgNO3,可能有 Zn(NO3)2 二、填空与简答题(每空 1 分,化学方程式每个 2 分,共 16 分) 16.(4 分)用化学用语填空。 (1)两个氢原子 ; (2)地壳中含量最多金属元素的离子 ; (3)天然气的主要成分 ; (4)生活中常作食品干燥剂的氧化物 。 17.(4 分)人类的日常生活、工农业生产都与化学密不可分。请回答: (1)农业上使用的硝酸钾属于 肥。 (2)饮用硬度过大的水不利于健康,生活中常用 方法来降低水的硬度。 (3)冰箱中放活性炭除去异味,这是利用了活性炭的 性。 (4)有机合成材料的出现是材料史上的一次重大突破。下列属于有机合成材料的是 。 A.不锈钢汤勺 B.塑料果盘 C.纯棉围巾 D.玻璃杯 18.(2 分)工业上常将煤洗选加工后用于制备水煤气,其主要反应的微观示意图如下: —氢原子 —氧原子 —碳原子A B C D 反应前 反应后 ——→高温 根据上图所示,回答下列问题: (1)上述反应的基本类型是 反应。 (2)构成最理想清洁燃料的微粒是 (填字母序号)。 19.(6 分)A~H 表示初中化学常见物质,它们之间的转化关系如图所示(部分反应物、生成物、反应条 件已略去)。已知常温下的 A 和 E 为红色固体,H 和 D 为气体。 A C ——→ E G ——① —— B ←——— D ——→② F ———→ H 请回答下列问题: (1)G 的化学式为 。 (2)反应①的化学方程式为 。 (3)反应②的化学方程式为 。 (4)上述转化中,B 和 H 表现出相似的化学性质是 。 三、实验与探究题(每空 1 分,化学方程式每个 2 分,共 17 分) 20.(8 分)根据实验室制取气体的常用装置图,回答下列问题: 棉花 浓 硫 酸 热水(80℃) 白磷 A B C D E F G (1)图中①仪器的名称 。 (2)实验室用 A 装置制取氧气的化学方程式为 。若收集一瓶较纯净的 氧气,可选用的装置为 (填字母序号,下同)。 (3)若要制取和收集一瓶干燥的 CO2,所选装置正确的连接顺序是 ,制取该气体的化学 方程式为 。 (4)若将 B 和 G 连接,可探究物质燃烧所需的条件,则 B 中产生的气体是 。 21.(9 分)为探究盐酸的化学性质,某化学小组做了如下实验: 紫色石 蕊溶液 稀盐酸 ↓ 铁片 稀盐酸 ↓ 氧化铁 稀盐酸 ↓ Ca(OH)2 溶液 稀盐酸 ↓ 稀盐酸 ↓ Na2CO3 溶液 AgNO3 溶液 稀盐酸 ↓ A B C D E F (1)上述反应中无现象的为 (填字母序号,下同),有白色沉淀出现的是 ;B 试管中 所发生反应的化学方程式为 。 (2)将反应后 D 和 E 试管中的废液倒入一个洁净的烧杯中,观察到烧杯中先有气泡产生,后有白色 沉淀出现。将烧杯中的混合物过滤,得到白色沉淀和无色滤液。同学们对滤液中溶质的成分进行 探究。 【提出问题】滤液中溶质的成分是什么? 【假设与猜想】猜想一:NaCl 猜想二:NaCl 和 CaCl2 猜想三:NaCl、Ca(OH)2 和 HCl 猜想四: 【讨论与交流】经讨论,同学们一致认为猜想 是错误的。 【实验与结论】 实验步骤 实验现象 实验结论 取少量滤液于试管中,滴加适量碳酸钠溶液 无现象 猜想四成立 取少量滤液于试管中,滴加适量 【拓展与迁移】稀盐酸和稀硫酸有相似的化学性质,是因为它们的溶液中都存在 。 四、计算题(共 7 分) 22.(2 分)维生素 C(C6H8O6)对人体皮肤和牙龈健康有重要作用。缺乏维生素 C 会引起坏血病,中学 生每天需要补充约 60 mg 维生素 C。请回答下列问题: (1)维生素 C 中,碳、氧元素的质量比为 。 (2)维生素 C 的相对分子质量是 。 23.(5 分)某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液 50g 装入烧杯中,每次滴加 50g 稀盐酸 充分反应。测得部分数据及图像如下: 次数 1 2 3 4 5 加入稀盐酸的质量/g 50 50 50 50 50 烧杯中物质的质量/g 100 150 197.8 245.6 295.6 请根据有关信息计算: (1)a 的数值为 。 a 气体的质量/g 0 100 稀盐酸的质量/g (2)求稀盐酸中溶质的质量分数。(写出计算过程) (3)求恰好完全反应后所得溶液中溶质的质量。(写出计算过程) 2019 年甘肃省天水市初中毕业与升学学业考试(中考)试卷化学试题参考答案及评分标准 一、选择题(每小题只有一个选项符合题意。每小题 2 分,共 30 分) 1~5:CBDAB 6~10:DCAAD 11~15:CCBCB 二、填空与简答题(每空 1 分,化学方程式每个 2 分,共 16 分) 16.(4 分)(1)2H (2)Al3+ (3)CH4 (4)CaO 17.(4 分)(1)复合 (2)煮沸 (3)吸附 (4)B 18.(2 分)(1)置换 (2)D 19.(6 分)(1)CuO (2)3CO+Fe2O3 高温 =====2Fe+3CO2 (3)CO2+Ca(OH)2===CaCO3↓+H2O(或 CO2+2NaOH===Na2CO3+H2O 合理即可) (4)还原性 三、实验与探究题(每空 1 分,化学方程式每个 2 分,共 17 分) 20.(8 分)(1)长颈漏斗 (2)2KMnO4 △====K2MnO4+MnO2+O2↑ F (3)BCD CaCO3+2HCl===CaCl2+H2O+CO2↑ (4)O2(或氧气) 21.(9 分)(1)D F Fe+2HCl===FeCl2+H2↑ (2)【假设与猜想】NaCl 和 Na2CO3 【讨论与交流】三 【实验与结论】稀盐酸(或氯化钙溶液或氯化钡溶液) 有气泡产生(或有白色沉淀产生)(合理即可) 【拓展与迁移】H+(或氢离子) 四、计算题(共 7 分) 22.(2 分)(1)3:4 (2)176 23.(5 分)(1)4.4 (2)解:设与 Na2CO3 反应的 HCl 的质量为 x,同时生成 NaCl 的质量为 y。 Na2CO3+2HCl===2NaCl+H2O+CO2↑ 73 117 44 x y 4.4g 73 44 == x 4.4g x=7.3g 117 44 == y 4.4g y=11.7g 稀盐酸中溶质的质量分数为:7.3g 100g ×100%=7.3% 答:稀盐酸中溶质的质量分数为 7.3%。 (3)解:设 HCl 和 NaOH 反应生成 NaCl 的质量为 m。 与 NaOH 反应的 HCl 质量为:100g×7.3%=7.3g HCl+NaOH=== NaCl+H2O 36.5 58.5 7.3g m 36.5 58.5 == 7.3g m m=11.7g NaCl 的总质量为:11.7g+11.7g=23.4g 答:恰好完全反应后,所得溶液溶质的质量为 23.4g。查看更多