- 2021-06-08 发布 |
- 37.5 KB |
- 7页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
2019-2020学年安徽省蚌埠铁中高二上学期期中考试 化学 Word版
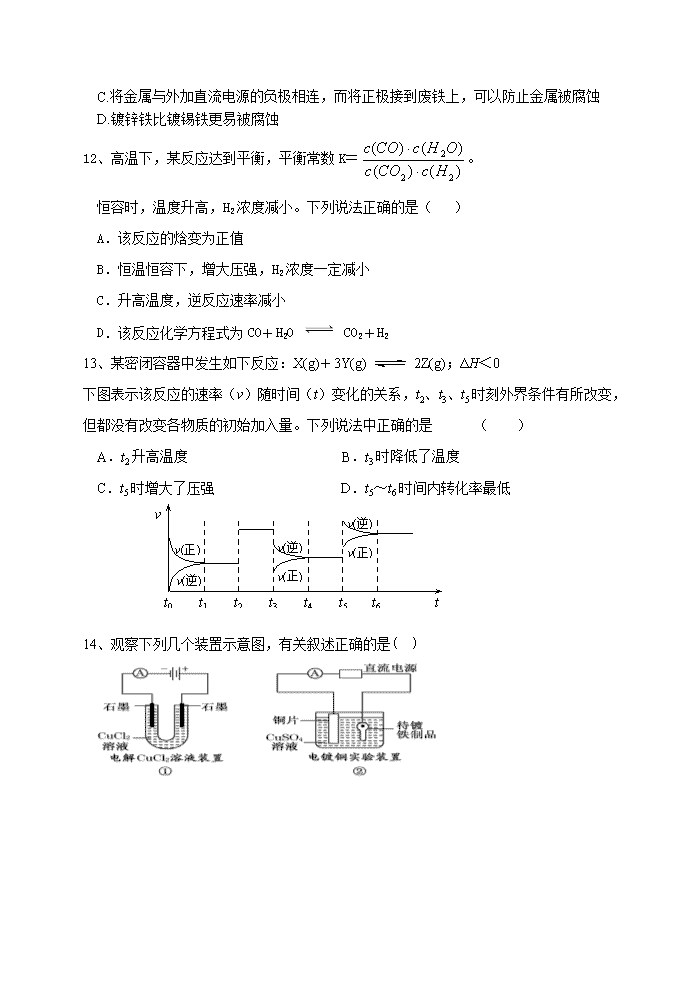
蚌埠铁中2019-2020学年度第一学期期中检测试卷 高二化学 考试时间:90分钟 试卷分值:100分 一、选择题:(每题只有一个正确答案,每题3分,共18题,54分) 1、下列反应中,熵减小的是( ) A、(NH4)2CO3(s)=NH4HCO3(s)+NH3(g) B、2N2O5(g)=4NO2(g)+O2(g) C、 MgCO3(s)=MgO(s)+CO2(g) D、2CO(g)=2C(s)+O2(g) 2、生产生活中的下列做法正确的是( ) A.2009年春,全国众多省份遭遇旱灾,使用液态二氧化碳进行人工降雨 B.用电解熔融态的AlCl3来制备金属铝 C.废弃的干电池不能随意丢弃,但可以土埋处理 D.电工操作中,不能把铜线和铝线拧在一起连接线路 3、右图曲线a表示放热反应 X(g)+Y(g) Z(g)+M(g)+N(s)进行过程中X的转化率随时间变化的关系。若要改变起始条件,使反应过程按b曲线进行,可采取的措施是 ( ) A.升高温度 B.加大X的投入量 C.加催化剂 D.增大体积 4、用电解水的方法分析水的组成时,需加入一些物质以增强水的导电性,一般不宜加入的物质是( ) A.NaNO3 B.NaCl C.H2SO4 D.KOH 5、在一密闭容器中进行反应:2SO2(g)+O2(g)催化剂 加热 2SO3(g)。已知反应过程中某一时 刻SO2、O2、SO3的浓度分别为0.2 mol·L-1、0.1 mol·L-1、0.2 mol·L-1。当反应达到平衡时,可能存在的数据是( ) A.SO2为0.4 mol·L-1,O2为0.2 mol·L-1 B.SO2为0.25 mol·L-1 C.SO2、SO3均为0.15 mol·L-1 D.SO3为0.4 mol·L-1 6、已知25℃、101 kPa条件下: 4Al(s)+3O2(g)===2Al2O3(s)ΔH=-2834.9 kJ/mol 4Al(s)+2O3(g)===2Al2O3(s)ΔH=-3119.1 kJ/mol 由此得出的正确结论是 ( ) A.等质量的O2比O3能量低,由O2变O3为放热反应 B.等质量的O2比O3能量高,由O2变O3为吸热反应 C.O3比O2稳定,由O2变O3为放热反应 D.O2比O3稳定,由O2变O3为吸热反应 7、100mL浓度为2mol·L-1的盐酸跟过量的锌片反应,为加快反应速率,又不影响生成氢气总量,可采用的方法是( ) A.加入少量浓盐酸 B.加入几滴氯化铜溶液 C.加入适量蒸馏水 D.加入适量的氯化钠溶液 8、一定温度下,在容积固定的密闭容器中进行的可逆反应:2NO22NO+O2,达到平衡的标志是( ) ①相同时间内,氧气的生成速率为n mol·L-1·s-1,NO2的生成速率为2n mol·L-1·s-1 ②单位时间内生成n mol O2的同时生成2n mol的NO ③混合气体的颜色不再变化 ④混合气体的密度保持不变 ⑤混合气体的平均相对分子质量不再改变 ⑥压强不随时间变化而变化 A.①③⑤⑥ B.②③⑤ C.①③④ D.①②③④⑤⑥ 9、在一密闭的容器中,反应aA(g) bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度是原来的60%,则 ( ) A.平衡向正反应方向移动了 B.物质A的转化率减少了 C.物质B的质量分数减少了 D.a > b 10、以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。关于该电池的叙述正确的是( ) A.该电池能够在高温下工作 B.电池的负极反应为:C6H12O6+6H2O―→6CO2↑+24H++24e- C.放电过程中,H+从正极区向负极区迁移 D.在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体 22.4/6 L 11、2008年美籍华裔化学家钱永健获得该年度诺贝尔化学奖。少年时代,他就对化学产生了浓厚的兴趣。16岁时,他凭借一个金属易受硫氰酸盐腐蚀的调查项目,荣获具有“少年诺贝尔奖”之称的著名奖项。以下说法正确的是( ) A.金属腐蚀就是金属原子失去电子被还原的过程 B.合金都比纯金属易被腐蚀 C.将金属与外加直流电源的负极相连,而将正极接到废铁上,可以防止金属被腐蚀 D.镀锌铁比镀锡铁更易被腐蚀 12、高温下,某反应达到平衡,平衡常数K=。 恒容时,温度升高,H2浓度减小。下列说法正确的是( ) A.该反应的焓变为正值 B.恒温恒容下,增大压强,H2浓度一定减小 催化剂 高温 C.升高温度,逆反应速率减小 D.该反应化学方程式为CO+H2O CO2+H2 13、某密闭容器中发生如下反应:X(g)+3Y(g)2Z(g);ΔH<0 下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 ( ) A.t2升高温度 B.t3时降低了温度 C.t5时增大了压强 D.t5~t6时间内转化率最低 t4 t5 t3 t2 t1 t0 v v(逆) v(正) v(逆) v(正) t v(逆) v(正) t6 14、观察下列几个装置示意图,有关叙述正确的是( ) A.装置①中阳极上析出红色固体 B.装置②的待镀铁制品应与电源正极相连 C.装置③中外电路电子由a极流向b极 D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 15、对于可逆反应 2AB3(g) A2(g) + 3B2(g) ; ΔH>0,下列图像正确的是( ) υ υ逆 υ正 温度 A AB3% 500℃ 时间 100℃ B AB3% 温度 1×106 Pa 1×105Pa C AB3% 压强 100℃ 500℃ D 16、将固体NH4I置于密闭容器中,在一定温度下发生下列反应: ①NH4I(s) NH3(g)+HI(g); ②2HI(g) H2(g)+I2(g) 达到平衡时,c(H2)=0.5 mol·L-1,c(HI)=4 mol·L-1,则此温度下反应①的平衡常数(单位:mol2·L-2)为( ) A.9 B.16 C.20 D.25 17、(08广东卷)LiFePO4电池具有稳定性高、安全、对环境友好等优点,可用于电动汽车。电池反应为: FePO4+LiLiFePO4,电池的正极材料是LiFePO4,负极材料是石墨,含U导电固体为电解质。下列有关LiFePO4电池说法正确的是( ) A.可加入硫酸以提高电解质的导电性 B放电时电池内部Li+ 向负极移动. C.充电过程中,电池正极材料的质量减少 D.放电时电池正极反应为:FePO4+Li++e-=LiFePO4 18、已知: (1)H2(g)+O2(g)===H2O(g) ΔH1=a kJ·mol-1 (2)2H2(g)+O2(g)===2H2O(g) ΔH2=b kJ·mol-1 (3)H2(g)+O2(g)===H2O(l) ΔH3=c kJ·mol-1 (4)2H2(g)+O2(g)===2H2O(l) ΔH4=d kJ·mol-1 下列关系式中正确的是( ) A.a查看更多