- 2021-06-05 发布 |
- 37.5 KB |
- 6页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
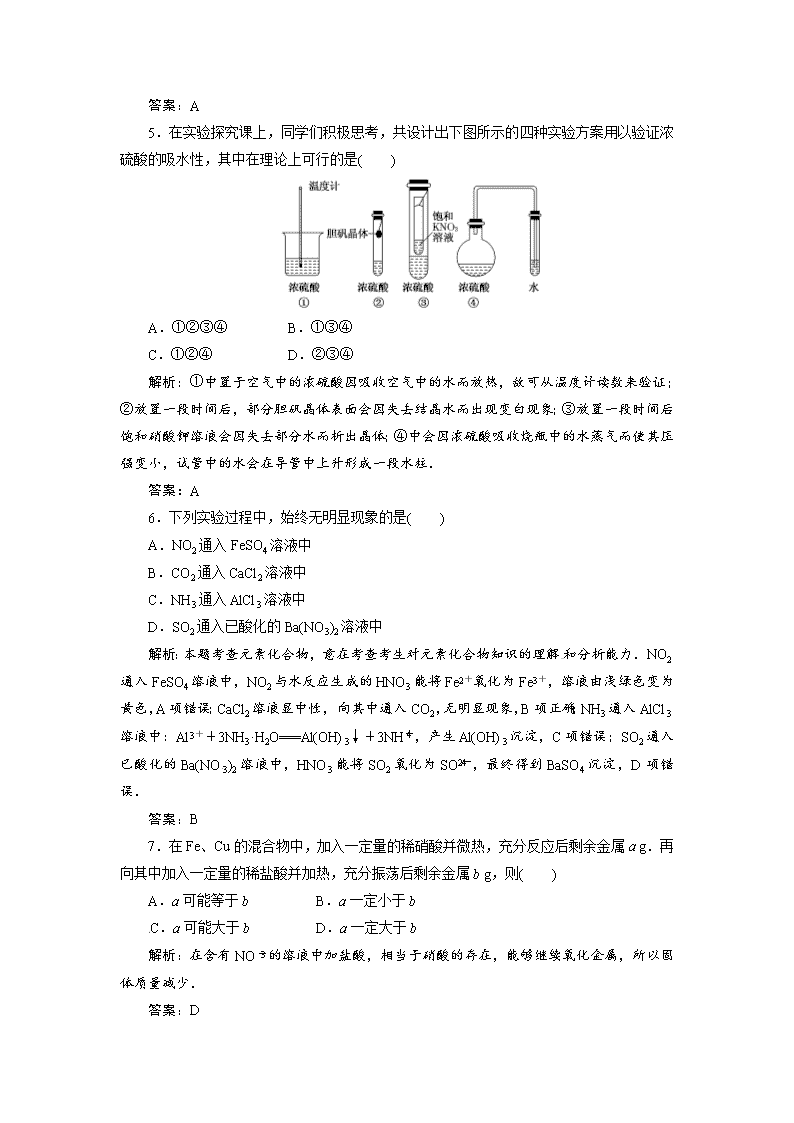
高一化学同步巩固练习解析:第4章 第4节第2课时(新人教版必修1)
高一同步巩固练习试题解析(新人教版必修1) (时间45分钟,满分100分) 一、选择题(本题包括8小题,每小题6分,共48分) 1.如图小试管中盛有几毫升水,与大试管连通的U形细玻璃管内放有少量水(已染成红色).如沿小试管壁小心地慢慢注入3 mL浓硫酸,静置片刻后,U形细玻璃管中可观察到的液面现象是( ) A.左高右低 B.左低右高 C.左右一样高 D.来回振动 解析:浓硫酸溶于水时,放出大量的热,使被封闭气体的体积膨胀,从而使U形管左侧液面下降,右侧液面上升. 答案:B 2.下列反应中,硝酸既表现了氧化性又表现了酸性的是( ) A.C+浓HNO3 B.Cu+稀HNO3 C.CuO+浓HNO3 D.NaOH+HNO3 解析:浓HNO3与C反应只表现氧化性,与CuO,NaOH反应只表现酸性,与Cu反应生成NO2表现氧化性,生成Cu(NO3)2表现酸性. 答案:B 3.下列有关浓硫酸的叙述正确的是( ) A.浓硫酸具有吸水性,因而能使蔗糖炭化 B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体 C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体 D.浓硫酸在常温下能够使铁、铝等金属钝化 解析:浓硫酸使蔗糖炭化表现了浓硫酸的脱水性,A错误.浓硫酸与铜片的反应需要加热,在常温下不反应,B错误.浓硫酸是一种干燥剂,但是它是具有强氧化性的酸性干燥剂,所以不能干燥碱性气体氨气,C错误. 答案:D 4.下列关于浓HNO3和浓H2SO4的叙述中正确的是( ) A.常温下都可用铝制容器贮存 B.露置在空气中,容器内酸液的质量都减轻 C.常温下都能与铜较快反应 D.露置在空气中,容器内酸液的浓度都增大 解析:浓硫酸吸水增重,浓硫酸常温下与Cu不反应,露置在空气中,浓度都减小. 答案:A 5.在实验探究课上,同学们积极思考,共设计出下图所示的四种实验方案用以验证浓硫酸的吸水性,其中在理论上可行的是( ) A.①②③④ B.①③④ C.①②④ D.②③④ 解析:①中置于空气中的浓硫酸因吸收空气中的水而放热,故可从温度计读数来验证;②放置一段时间后,部分胆矾晶体表面会因失去结晶水而出现变白现象;③放置一段时间后饱和硝酸钾溶液会因失去部分水而析出晶体;④中会因浓硫酸吸收烧瓶中的水蒸气而使其压强变小,试管中的水会在导管中上升形成一段水柱. 答案:A 6.下列实验过程中,始终无明显现象的是( ) A.NO2通入FeSO4溶液中 B.CO2通入CaCl2溶液中 C.NH3通入AlCl3溶液中 D.SO2通入已酸化的Ba(NO3)2溶液中 解析:本题考查元素化合物,意在考查考生对元素化合物知识的理解和分析能力.NO2通入FeSO4溶液中,NO2与水反应生成的HNO3能将Fe2+氧化为Fe3+,溶液由浅绿色变为黄色,A项错误;CaCl2溶液显中性,向其中通入CO2,无明显现象,B项正确;NH3通入AlCl3溶液中:Al3++3NH3·H2O===Al(OH)3↓+3NH,产生Al(OH)3沉淀,C项错误;SO2通入已酸化的Ba(NO3)2溶液中,HNO3能将SO2氧化为SO,最终得到BaSO4沉淀,D项错误. 答案:B 7.在Fe、Cu的混合物中,加入一定量的稀硝酸并微热,充分反应后剩余金属a g.再向其中加入一定量的稀盐酸并加热,充分振荡后剩余金属b g,则( ) A.a可能等于b B.a一定小于b C.a可能大于b D.a一定大于b 解析:在含有NO的溶液中加盐酸,相当于硝酸的存在,能够继续氧化金属,所以固体质量减少. 答案:D 8.用右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应.下列实验不合理的是( ) A.上下移动①中铜丝可控制SO2的量 B.②中选用品红溶液验证SO2的生成 C.③中选用NaOH溶液吸收多余的SO2 D.为确认CuSO4生成,向①中加水,观察颜色 解析:本题考查铜和浓硫酸反应的实验,意在考查考生对化学实验原理的分析能力.上下移动铜丝可以控制铜与浓硫酸的接触面积的大小,从而可以控制反应生成SO2的量,A项正确;SO2可使品红溶液褪色,因此B项正确;SO2有毒,能与NaOH溶液反应,因此C项正确;铜与浓硫酸反应后①中溶液显蓝色即可证明有CuSO4生成,无需向其中加水,D项错误. 答案:D 二、非选择题(本题包括5小题,共52分) 9.(9分)浓硫酸具有:A.强酸性B.强氧化性C.高沸点、难挥发性D.脱水性E.吸水性等性质.以下过程主要表现了浓硫酸的哪些性质?请将答案前的字母分别填入括号中. (1)用NaCl固体和浓H2SO4在加热条件下制氯化氢气体( ) (2)用磷矿粉〔主要成分Ca3(PO4)2〕和硫酸反应制磷酸( ) (3)热的浓硫酸与铜片反应( ) (4)浓硫酸干燥H2、O2、Cl2、HCl和SO2等气体( ) (5)常温下可以用铁或铝的容器贮存浓硫酸( ) (6)胆矾放在盛浓硫酸的干燥器中变成白色粉末( ) (7)不能用浓硫酸干燥HBr、HI和H2S等气体( ) (8)浓硫酸使湿润的蓝色石蕊试纸先变红后变黑( ) (9)热的浓硫酸分别和木炭、硫粉反应( ) 解析:(1)浓硫酸具有高沸点、难挥发性,氯化氢气体易挥发. (2)磷酸是高沸点的中强酸,利用强酸与弱酸盐反应制弱酸的原理制磷酸. (3)浓硫酸在加热条件下将不活泼的金属铜转化成硫酸铜,不仅表现了浓硫酸的强氧化性,还表现了酸性. (4)浓硫酸吸收混在上述气体中的杂质水蒸气. (5)常温下,浓硫酸和铝、铁反应,在金属表面生成一层致密的氧化物薄膜,阻止内部的金属和浓硫酸继续反应. (6)浓硫酸间接吸收胆矾晶体中的结晶水,使之变成无水硫酸铜白色粉末. (7)浓硫酸具有强氧化性,而HBr、HI、H2S具有强还原性. (8)浓硫酸既具有酸的通性,可使酸碱指示剂变色,又具有脱水性,可使有机物炭化. (9)热的浓硫酸分别与木炭、硫粉反应表现的是强氧化性. 答案:(1)C (2)A (3)AB (4)E (5)B (6)E (7)B (8)AD (9)B 10.(11分)某兴趣小组设计出如图所示装置来改进教材中“铜与浓硫酸反应”实验 (1)试管A中反应的化学方程式是________________________________________. (2)试管B用来探究SO2的漂白性,则应装的试剂是__________________________. (3)试管C中的实验现象为溴水褪色,则可证明SO2具有________性. (4)实验中采用可抽动的铜丝,与直接放铜片相比优点是 ________________________________________________________________________. (5)该装置存在明显的缺陷,应如何改进________________________________. 答案:(1)Cu+2H2SO4(浓)CuSO4+SO2+2H2O (2)品红 (3)还原 (4)可控制反应的起始与停止 (5)增加尾气吸收装置 11.(9分)实验证明铜在低温下不能和O2发生反应,也不能和稀硫酸共热发生反应,但工业上却是将废铜屑倒入热的稀硫酸中并不断地通入空气来制取CuSO4溶液的.铜屑在此状态下发生的一系列化学反应的方程式为:____________________,_______________.利用铜和浓H2SO4在加热条件下也能制备CuSO4溶液,其化学方程式为______________.以上两种方法是前者好还是后者好________.原因是什么?_____________________________ ________________________________________________________________________. 解析:在稀硫酸存在的条件下,Cu与O2反应后的生成物迅速溶解在热的稀硫酸中生成CuSO4;第二种方法是在加热条件下铜与浓硫酸反应,H2SO4会被还原为SO2,其利用率降低且生成的气体有毒. 答案:2Cu+O22CuO,CuO+H2SO4(稀)===CuSO4+H2O Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O 第一种方法好 原因是①制得相同质量的产品,第一种方法消耗的硫酸少,②第二种方法生成SO2,会造成大气污染 12.(10分)为了验证木炭可被浓H2SO4氧化成CO2,选用如图所示仪器(内含物质)组装成实验装置: (1)如按气流由左向右流向,连接上述装置的正确顺序是(填各接口字母): ________接________,________接________,________接________. (2)仪器乙、丙应有怎样的实验现象才表明已检验出CO2? 乙中______________________________________________________________________, 丙中______________________________________________________________________. (3)丁中酸性KMnO4溶液的作用是_____________________________________. (4)写出甲中反应的化学方程式__________________________________. 解析:木炭与浓硫酸加热反应生成CO2、SO2和H2O.其中CO2、SO2在化学性质上的相同点都是酸性氧化物,都跟澄清石灰水中的Ca(OH)2反应,使澄清石灰水变浑浊,这会干扰CO2的鉴别.SO2和CO2在化学性质上的明显不同点是SO2有漂白性和强的还原性,而CO2都没有.所以,在鉴别CO2时,首先用酸性KMnO4溶液将SO2氧化除去,再用品红溶液检验是否被完全除去,最后用澄清石灰水检验CO2的存在,是一种确认CO2存在的好方案. 答案:(1)A F E C D B (2)乙中澄清石灰水变浑浊 丙中品红溶液未褪色 (3)吸收SO2 (4)C+2H2SO4(浓)CO2↑+2SO2↑+2H2O 13.(13分)实验室用稀硝酸与铜反应制备NO气体,如果采用如图Ⅰ装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为观察到的现象不能有力证明反应产物是NO.有人设计了图Ⅱ装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果. (1)用Ⅰ装置做实验时,用排水法收集到的气体中的颜色为________色;实验过程中由于____________________________,不易观察到______________生成,从而不能有力证明反应产物是NO. (2)用Ⅱ装置做实验时,将有关操作补充完全: ①将分液漏斗的活塞打开,从U形管的B侧管口注入稀硝酸,一直注到_________为止. ②关闭活塞,用酒精灯在U形管的A侧加热,当____________时,立即撤去酒精灯. (3)完成下列问题: ①反应在什么情况下可以自动停止? 答:________________________________________________________________________ ________________________________________________________________________. 可在何处观察到无色的NO气体? 答:________________________________________________________________________ ________________________________________________________________________. ②如果将分液漏斗的活塞慢慢打开,可立即观察到哪些明显现象? 答:________________________________________________________________________ ________________________________________________________________________. 解析:由于NO易被空气中O2氧化成NO2(红棕色),所以在金属与稀HNO3反应的常规实验中,很难观察到无色NO气体的生成,而是观察到红棕色气体.本题实验Ⅱ中的意图是创设无氧气环境,使NO能存在相当长一段时间. 答案:(1)无 烧瓶中有空气,可以将产生的NO氧化成NO2,NO2又与水反应生成NO 无色的NO (2)①液面与胶塞接触(或A侧管中恰好充满液体) ②铜丝上有气泡产生 (3)①当反应产生的NO气体将稀HNO3排入U形管B侧管,使铜丝与稀HNO3脱离接触时,反应立刻停止 在U形管A侧管内可观察到无色NO气体 ②U形管B侧管内的稀HNO3又回到A侧管中,分液漏斗中有红棕色气体产生查看更多