- 2021-06-04 发布 |
- 37.5 KB |
- 10页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
徐州专版2020中考化学复习方案第5章金属的冶炼与利用专项07金属活动性顺序及其应用课件
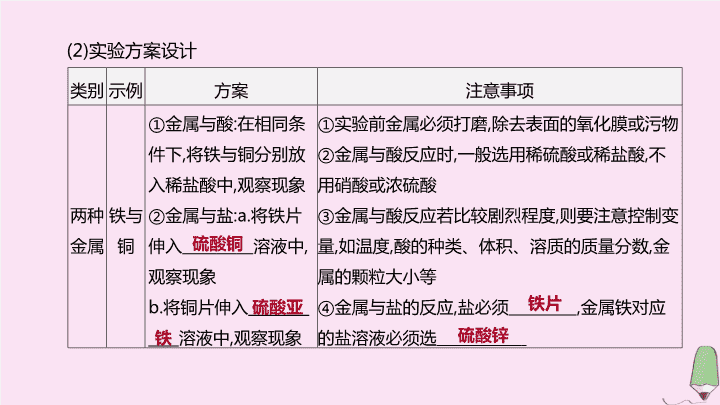
专项(七) 金属活动性顺序及其应用 第 5 章 金属的冶炼与利用 考点突破 1. 金属活动性顺序及探究 (1) 判断金属活动性顺序的依据 方法 1: 金属是否与酸反应或与酸反应的剧烈程度。 方法 2: 一种金属能否把另一种金属从其盐溶液中置换出来。 (2) 实验方案设计 类别 示例 方案 注意事项 两种 金属 铁与 铜 ① 金属与酸 : 在相同条件下 , 将铁与铜分别放入稀盐酸中 , 观察现象 ② 金属与盐 :a. 将铁片伸入 溶液中 , 观察现象 b. 将铜片伸 入 ________ ____ 溶液 中 , 观察现象 ① 实验前金属必须打磨 , 除去表面的氧化膜或污物 ② 金属与酸反应时 , 一般选用稀硫酸或稀盐酸 , 不用硝酸或浓硫酸 ③ 金属与酸反应若比较剧烈程度 , 则要注意控制变量 , 如温度 , 酸的种类、体积、溶质的质量分数 , 金属的颗粒大小等 ④ 金属与盐的反应 , 盐必须 , 金属铁对应的盐溶液必须选 硫酸铜 硫酸亚 铁片 硫酸锌 铁 (续表) 类别 示例 方案 注意事项 三种 金属 锌、铁、 铜 ① “两盐夹一金” : 将 分别伸入盛 有 溶液 、 _________ 溶液 中 , 观察现象 ② “两金夹一盐” : 将 __________ 、 __________ 分别 伸 入 溶液 中 , 观察现象 ① 实验前金属必须打磨 , 除去表面的氧化膜或污物 ② 金属与酸反应时 , 一般选用稀硫酸或稀盐酸 , 不用硝酸或浓硫酸 ③ 金属与酸反应若比较剧烈程度 , 则要注意控制变量 , 如温度 , 酸的种类、体积、溶质的质量分数 , 金属的颗粒大小等 ④ 金属与盐的反应 , 盐必须 , 金属铁对应的盐溶液必须选 硫酸铜 锌片 铜片 硫酸 亚铁 可溶 亚铁盐 溶液 2. 金属与盐反应 金属与盐溶液反应遵循“远距离先置换”的规律。反应结束后 , 固体的成分不与溶液的成分反应 , 能共存。 例如 , 向一定量 AgNO 3 和 Cu(NO 3 ) 2 的混合溶液中逐渐加入足量的锌粒过程中 : (1) 溶液中溶质成分、固体成分变化 步骤 1: 判断金属的活动性顺序为 Zn>Cu>Ag 。 步骤 2: 涉及的化学反应方程式 : 先 ; 后 。 Zn+2AgNO 3 2Ag+Zn(NO 3 ) 2 Zn+Cu(NO 3 ) 2 Cu+Zn(NO 3 ) 2 步骤 3: 分析反应过程 反应顺序 金属锌质量 得到固体 溶液中溶质 ① 少量 ( 用完 ) 银 ( 部分 ) AgNO 3 ( 部分 ) 和 Cu(NO 3 ) 2 、 Zn(NO 3 ) 2 ( 生成少量 ) ② 少量 ( 用完 ) 银 ( 全部 ) Cu(NO 3 ) 2 、 Zn(NO 3 ) 2 ( 生成量增多 ) ③ 少量 ( 用完 ) 银 ( 全部 ) 、铜 ( 少量 ) Cu(NO 3 ) 2 ( 部分 ) 、 Zn(NO 3 ) 2 ( 生成量增多 ) (续表) 反应顺序 金属锌质量 得到固体 溶液中溶质 ④ 恰好完全反应 ( 用完 ) 银 ( 全部 ) 、铜 ( 全部 ) Zn(NO 3 ) 2 ( 生成量增多 , 不再改变 ) ⑤ 足量 ( 剩余 ) 银 ( 全部 ) 、铜 ( 全部 ) 、锌 ( 剩余 ) Zn(NO 3 ) 2 ( 质量不再改变 ) (2) 溶液质量、固体质量变化 : 金属与盐溶液反应得到新金属和溶液质量的多少与金属的相对原子质量有关。 Zn+2AgNO 3 2Ag+Zn(NO 3 ) 2 Zn+Cu(NO 3 ) 2 Cu+Zn(NO 3 ) 2 65 216 65 64 ①Zn 与 AgNO 3 反应 , 反应后固体质量 , 溶液质量 ; ②Zn 和 Cu(NO 3 ) 2 反应 , 与 ① 相比 , 固体质量 , 故溶液质量 。 增加 减少 减少 增加 3. 金属与酸反应 金属与酸反应涉及三个量 : 反应物质量、生成物质量、反应速率。 金属与酸反应图像类型 : 气体 - 时间图、气体 - 金属图、气体 - 稀酸图 , 其中只有气体 - 时间图可以反映反应的速率 , 从而判断金属的活动性顺序。 分类 足量金属与等量酸反应 足量酸与等量的金属反应 图像 (续表) 分类 足量金属与等量酸反应 足量酸与等量的金属反应 归纳 ① 如图甲 , 金属活动性 :Mg>Al>Zn>Fe ② 酸质量相等 , 生成氢气质量相等 , 即 Al=Mg=Fe=Zn ③ 如图乙 , 相对原子质量越小、化合价越高 , 消耗金属质量越小 , 即 Al查看更多