化学卷·2018届云南省云天化中学高二上学期期末考试(2017
云天化中学2016—2017学年秋季学期期末考试试卷
高 二 化 学
说明:1.时间:90分钟;分值:100分;
2.本卷分Ⅰ、Ⅱ卷,请将第Ⅰ卷选择题答案及II卷答案在答题卡填涂和作答。
3.可能用到的相对原子质量:H-1 C-12 O-16
第Ⅰ卷 选择题(共54分)
一、选择题:(每小题3分,共54分。每小题只有一个选项符合题意。)
1.下列关于反应热的表述正确的是
A.当△H<0时,表示该反应为吸热反应
B.需要加热才能进行的反应是吸热反应
C.反应热的大小与反应物所具有的能量和生成物所具有的能量无关
D.1molNaOH分别和1molCH3COOH、1molHNO3反应放出的热量:CH3COOH
△H1
C.浓硫酸与稀NaOH溶液反应的中和热为-57.3kJ/mol
D.稀醋酸与稀NaOH溶液反应生成1mol水,放出57.3kJ热量
6.烷烃的命名正确的是
A.4甲基3丙基戊烷 B.3异丙基己烷
C.2甲基3丙基戊烷 D.2甲基3乙基己烷
7.下列关于有机物的说法正确的是
A. 淀粉、纤维素、蛋白质都是天然高分子化合物,都能发生水解反应
B. 蔗糖和葡萄糖不是同分异构体,但属同系物
C. 苯酚、甲醛通过加聚反应可制得酚醛树脂
D. 石油裂解和煤的干馏都是化学变化,而石油的分馏和煤的气化都是物理变化
8.根据下列实验操作和现象所得出的结论正确的是
选项
实验操作与现象
结论
A
向油脂皂化反应后的溶液中滴入酚酞,溶液变红
油脂已经完全皂化
B
蔗糖溶液在稀硫酸存在下水浴加热一段时间后,再与银氨溶液混合加热,有光亮的银生成
蔗糖溶液已经水解完全
C
向溶液X中滴入NaHCO3溶液,产生无色气体
X中的溶质一定是酸
D
向鸡蛋清溶液中滴加醋酸铅溶液,产生白色沉淀,加水沉淀不消失
蛋白质发生了变性
9.下列说法不正确的是
A.聚合物可由单体CH3CH=CH2和CH2=CH2加聚制得
B.1 molCH3COOH与1mol CH3CH2OH在浓硫酸共热下生成的乙酸乙酯分子数为NA
C.乙醇、苯酚、乙酸都有羟基,但是羟基上的H活泼性不同,主要是基团之间相互影响造成的
D.等物质的量的乙炔和乙醛分别充分燃烧,所耗用氧气的量相同
10.某有机物X的结构简式如下图所示,则下列有关说法中不正确的是
A.能发生加成、取代、氧化反应
B.1 mol该物质最多可与7mol NaOH反应
C.1 mol该物质最多可与6 mol H2反应
D.能与FeCl3溶液发生显色反应
11.物质制备是化学研究的主要任务之一。下列操作正确的是
A.制取溴苯:将铁屑、溴水、苯混合加热
B.除去乙烷中混有的少量乙烯:将混合气体通入足量酸性KMnO4溶液中
C.提取溶解在水中的少量碘:加入CCl4振荡、静置、分层后放出下面有机层再分离
D.检验某溶液中是否含有甲醛:在盛有2 mL 10%CuSO4溶液的试管中滴加0.5mL10%
NaOH溶液,混合均匀,滴入待检液,加热
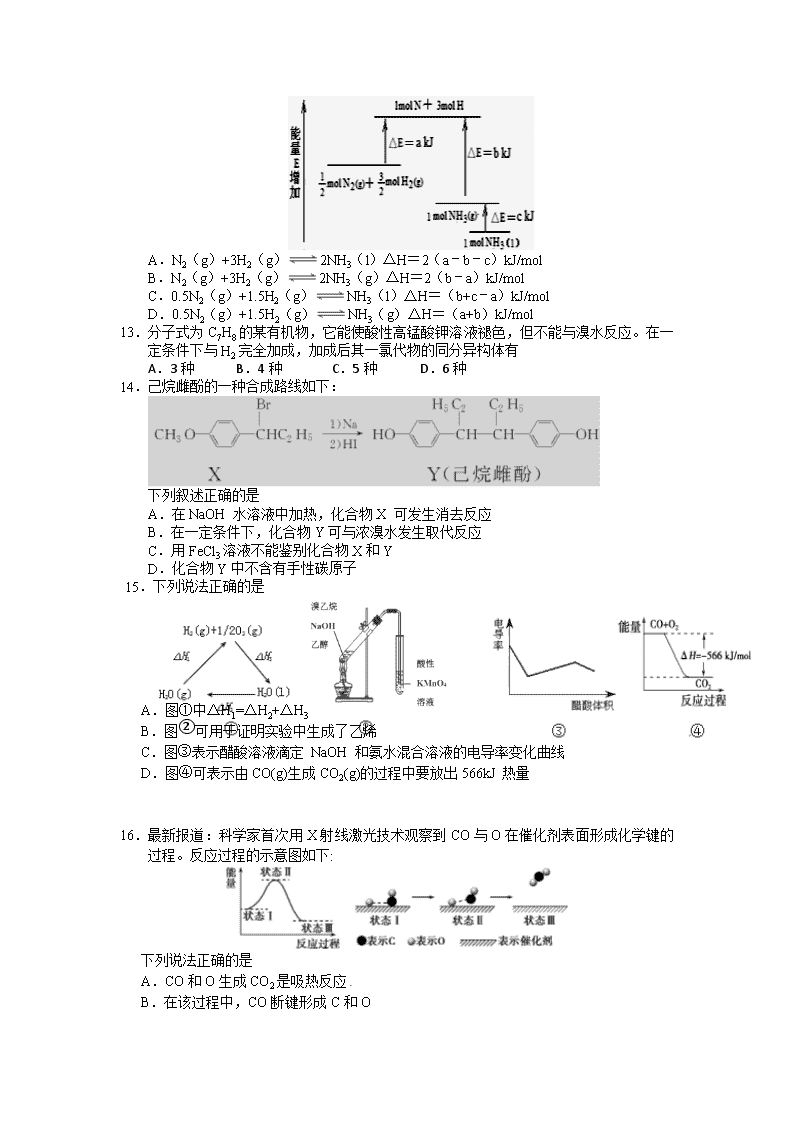
12.化学反应N2+3H22NH3的能量变化如图所示,该反应的热化学方程式是
A.N2(g)+3H2(g)2NH3(l)△H=2(a﹣b﹣c)kJ/mol
B.N2(g)+3H2(g)2NH3(g)△H=2(b﹣a)kJ/mol
C.0.5N2(g)+1.5H2(g)NH3(l)△H=(b+c﹣a)kJ/mol
D.0.5N2(g)+1.5H2(g)NH3(g)△H=(a+b)kJ/mol
13.分子式为C7H8的某有机物,它能使酸性高锰酸钾溶液褪色,但不能与溴水反应。在一定条件下与H2完全加成,加成后其一氯代物的同分异构体有
A.3种 B.4种 C.5种 D.6种
14.己烷雌酚的一种合成路线如下:
下列叙述正确的是
A.在NaOH 水溶液中加热,化合物X 可发生消去反应
B.在一定条件下,化合物Y可与浓溴水发生取代反应
C.用FeCl3溶液不能鉴别化合物X和Y
D.化合物Y中不含有手性碳原子
1 15.下列说法正确的是
A.图①中△H1=△H2+△H3
B.图②可用于证明实验中生成了乙烯
C.图③表示醋酸溶液滴定 NaOH 和氨水混合溶液的电导率变化曲线
D.图④可表示由CO(g)生成CO2(g)的过程中要放出566kJ 热量
16.最新报道:科学家首次用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下:
下列说法正确的是
A.CO和O生成CO2是吸热反应m
B.在该过程中,CO断键形成C和O
C.CO和O生成了具有极性共价键的CO2
D.状态Ⅰ→状态Ⅲ表示CO与O2反应的过程
17.已知:HCN(aq)与NaOH(aq)反应的ΔH=-12.1 kJ·mol-1;HCl(aq)与NaOH(aq)反应的ΔH=-57.3 kJ·mol-1,则HCN在水溶液中电离的ΔH等于
A.-69.4 kJ·mol-1 B.-45.2 kJ·mol-1 C.+45.2 kJ·mol-1 D.+69.4 kJ·mol-1
18.有机物甲分子式为C11H14O2,在酸性条件下水解生成乙和丙,丙遇FeC13溶液显色,丙的相对分子质量比乙大20,甲的结构有
A.3种 B.4种 C.8 种 D.6 种
第Ⅱ卷 非选择题(共46分)
二、非选择题:
19.(6分)已知E1=134 kJ/mol、E2=368 kJ/mol,请参考题中图表,按要求填空:
图Ⅰ 图Ⅱ
(1)图Ⅰ是1 mol NO2(g)和1 mol CO(g)反应生成CO2(g)和NO(g)过程中的能量变化示意图, NO2和CO反应的热化学方程式为:_______ _____________________。
(2)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应。
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g) (NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g) NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g) 2NH4HCO3(aq) ΔH3
则ΔH3与ΔH1、ΔH2之间的关系是:ΔH3=________。
(3)下表所示是部分化学键的键能参数:
化学键
P—P
P—O
O===O
P===O
键能/(kJ/mol)
a
b
c
x
已知白磷的燃烧热为d kJ/mol,白磷及其完全燃烧生成的产物的结构如图Ⅱ所示,表中
x=________________ kJ/mol(用含a、b、c、d的代数式表示)。
20.(8分)碳是形成化合物种类最多的元素,其单质及化合物是人类生产生活的主要能源物质。请回答下列问题:
(1)有机物M经过太阳光光照可转化成N,转化过程如下:
ΔH=+88.6 kJ/mol,则M、N相比,较稳定的是________。
(2)已知CH3OH(l)的燃烧热ΔH=-238.6 kJ/mol,CH3OH(l)+O2(g)===CO2(g)+2H2(g) ΔH=-a kJ/mol,则a________238.6(填“>”“<”或“=”)。
(3)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1 mol Cl2参与反应时释放出145 kJ热量,写出该反应的热化学方程式:______________________________________________________。
(4)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)===2Al2O3(s)+3TiC(s) ΔH=-1176 kJ/mol,则反应过程中,每转移1 mol电子放出的热量为___________________。
(5)汽车排出的尾气中含有CO和NO等气体。为了解决污染问题,在汽车排气管内安装的催化转化器,可使汽车尾气中的主要污染物CO和NO转化为无毒的大气循环物质。已知:
N2(g)+O2(g) ===2NO(g) ΔH=+180.5 kJ/mol
2C(s)+O2(g)===2CO(g) ΔH=-221.0 kJ/mol
C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
请写出污染物CO和NO转化为无毒的大气循环物质的热化学方程式是:
_______ _
21.(15分)有机化合物X、Y、A、B、C、D、E、F、G之间的转化关系如下图。
已知以下信息:
①RCHO
②RCOOHRCOOR'(R、R'代表烃基)
③X在催化剂作用下可与H2反应生成化合物Y。
④化合物F的核磁共振氢谱图中只有一个吸收峰。
回答下列问题:
(1) X中含氧官能团的名称是 ,X与HCN反应生成A的反应类型是 。
(2) 酯类化合物B的分子式是C15H14O3,其结构简式是 。
(3) X发生银镜反应的化学方程式是 。
(4) G在NaOH溶液中发生水解反应的化学方程式是 。
(5) 的同分异构体中:①能发生水解反应;②能发生银镜反应;③能与氯化铁溶液发生显色反应;④含氧官能团处在对位。满足上述条件的同分异构体共有 种(不考虑立体异构),写出核磁共振氢谱图中有五个吸收峰的同分异构体的结构简式: 。
(6) 写出以C2H5OH为原料合成乳酸()的路线(其他无机试剂任选)。合成路线流程图示例如下:
CH3CH2BrCH3CH2OHCH3COOCH2CH3
22.(17分)菠萝酯是一种带有浓郁的菠萝香气和香味的食用香料,其合成路线如下(部分反应条件及产物已略去):
请回答下列问题:
(1) A可用于制备顺丁橡胶(顺式聚1,3-丁二烯),顺丁橡胶的结构简式为__________,若顺丁橡胶的平均相对分子质量为540108,则平均聚合度为__________。
(2) F的结构简式为__________,反应④的条件是________________。
(3) ①一⑥反应中属于取代反应的是__________。
(4) 下列有关B的说法正确的是__________(填字母序号)。
a. 元素分析仪可确定B的实验式为C6H10
b. 质谱仪可检测B的最大质荷比的数值为82
c. 红外光谱仪可测定B中六个碳原子一定在同一平面上
d. 核磁共振仪可测定B有两种类型氢原子吸收峰
(5) 写出反应③的化学方程式__________________________________________。
(6) 同时满足下列条件的E的同分异构体的数目为__________种。
①遇氯化铁溶液显紫色 ②苯环上只有2个取代基且处于对位
(7) 参照上述合成路线,现仅以A为有机原料,无机试剂任选,设计制备的合成路线。
已知:①反应物分子的环外双键比环内双键更容易被氧化;
②(R,R’代表烃基或氢)
__________________________________________________________ 。
云天化中学2016—2017学年秋季学期期末考试试卷
高 二 化 学(答案)
1-5 DBBCA 6-10 DADBC 11-15 CACBC 16-18 CCD
19.(6分)(1)NO2(g)+CO(g)===CO2(g)+NO(g ) ΔH=-234 kJ/mol(2分)
(2)2ΔH2-ΔH1 (2分)
(3)(d+6a+5c-12b) (2分)
20.(8分) (1)M (1分)
(2)< (1分)
(3)2Cl2(g)+2H2O(g)+C(s)===4HCl(g)+CO2(g) ΔH=-290 kJ/mol (2分)
(4)98 kJ(2分)
(5)2NO(g)+2CO(g)===N2(g)+2CO2(g) ΔH=-746.5 kJ/mol。(2分)
21.(15分)
(1) 醛基(1分) 加成反应(1分)
(2) (2分)
(3) +2Ag(NH3)2OH +3NH3+2Ag↓+H2O(2分)
(4) +2NaOH++H2O(2分)
(5) 3 (2分) (2分)
(6) CH3—CH2—OHCH3—CHO
(3分)
22.(17分)
(1) (2分) 10002 (2分)
(2) CH2=CH-CH2-OH (1分) Cu/O2 加热(1分)
(3) ③⑥(2分)
(4) b(2分)
(5) (2分)
(6) 12 (2分)
(7) (3分)