- 2021-06-02 发布 |
- 37.5 KB |
- 3页


申明敬告: 本站不保证该用户上传的文档完整性,不预览、不比对内容而直接下载产生的反悔问题本站不予受理。
文档介绍
九年级人教版化学24
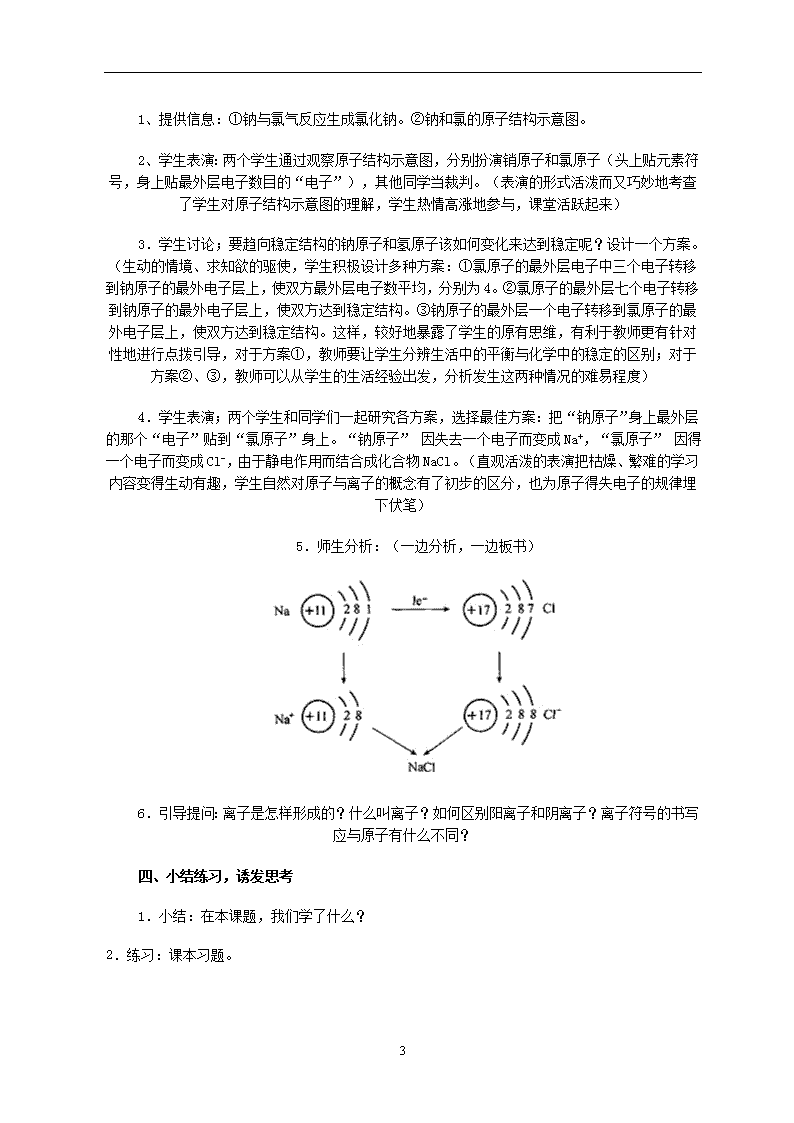
课题2 离子 教学目标 知识与能力目标: 1.知道原子核外电子是分层排布的。(难点) 2.了解离子的形成,初步认识离子是构成物质的一种粒子。(重点) 3.了解原子结构示意图涵义及原子最外层电子数与元素性质的关系。 过程与方法目标: 1.通过想象、猜想→探索证明→归纳原子核外电子的排布,培养学生空间想象力。 2.观察l~18号元素的原子结构示意图,归纳小结原子最外层电子数与元素性质的关系。 3.探究分析NaCl的形成过程,了解离子的形成,初步认识离子是构成物质的一种粒子。 情感态度与价值观目标: 1.培养学生对微观世界学习的兴趣。 2.唤起学生对科学的好奇与向往。 教学过程 一、情境导入 1.教师富有感情地朗读学生作品──科普小论文《漫游原子世界》,巩固原子结构的知识。 附文:我是一个小小的电子,我在原子里围绕着原子核不停地转动,虽然空间很大,但我和我的同伴总想挣脱原子核的吸引。可是原子核这个小老头很有能耐,虽然只占原子的一丁点空间,里面却由质子和中子构成,中子不带电,质子带正电,正好把我身上的负电深深吸引。 2.设问:原子核外电子是如何运动的呢?它们能否挣脱原子核的吸引呢? 二、引导探究核外电子的排布 3 1学生猜想:核外电子是如何运动的? 2.学生交流:向你的同学说一说你想象中核外电子如何运动? 3.探究证明假设:阅读课本图文。(把图4-9“核外电子分层排布示意图” 制作成挂图,借此引导学生空间想象能力,理解电子分层排布) 4.归纳结论:核外电子是分层排布的。 5.教师启发:科学家在探索原子核外电子运动时,也经历了假设、猜想的阶段,然后通过科学的手段、借助先进的仪器进行实验测定、检验而得到真理的。那么电子为什么有的排在第一层?有的排在第二层?各电子层上电子数目有什么规律?(让学生体验科学探究的过程后,进一步启发学生对电子排布的通想,提醒学生到高中后还会有更深入的研究,有兴趣的同学可自己查阅有关资料) 6.学习原子结构示意图表示的意义: 7.练习巩固:向你的同桌说一说下列原子结构示意图的意义: 8.展示挂图:1~18号元素的原子结构示意图。学生观察、互相讨论、归纳原子最外层电子数目与元素性质的关系: 元素 最外层电子数 元素化学性质 稀有气体元素 8个(He为 2) 比较稳定 金属元素 少于4个 不稳定 非金属元素 多于4个 不稳定 9.教师设问:稀有气体元素原子最外层电子数为8(He为2),达到稳定结构,故化学性质比较稳定。金属元素原子和非金属元素原子最外层电子未排满,要趋向稳定,怎么样才能达到目的呢?(制造探究情境,诱导学生下一步的探究) 三、探究离子的形成 3 1、提供信息:①钠与氯气反应生成氯化钠。②钠和氯的原子结构示意图。 2、学生表演:两个学生通过观察原子结构示意图,分别扮演销原子和氯原子(头上贴元素符号,身上贴最外层电子数目的“电子”),其他同学当裁判。(表演的形式活泼而又巧妙地考查了学生对原子结构示意图的理解,学生热情高涨地参与,课堂活跃起来) 3.学生讨论;要趋向稳定结构的钠原子和氢原子该如何变化来达到稳定呢?设计一个方案。(生动的情境、求知欲的驱使,学生积极设计多种方案:①氯原子的最外层电子中三个电子转移到钠原子的最外电子层上,使双方最外层电子数平均,分别为4。②氯原子的最外层七个电子转移到钠原子的最外电子层上,使双方达到稳定结构。③钠原子的最外层一个电子转移到氯原子的最外电子层上,使双方达到稳定结构。这样,较好地暴露了学生的原有思维,有利于教师更有针对性地进行点拨引导,对于方案①,教师要让学生分辨生活中的平衡与化学中的稳定的区别;对于方案②、③,教师可以从学生的生活经验出发,分析发生这两种情况的难易程度) 4.学生表演;两个学生和同学们一起研究各方案,选择最佳方案:把“钠原子”身上最外层的那个“电子”贴到“氯原子”身上。“钠原子” 因失去一个电子而变成Na+,“氯原子” 因得一个电子而变成Cl-,由于静电作用而结合成化合物NaCl。(直观活泼的表演把枯燥、繁难的学习内容变得生动有趣,学生自然对原子与离子的概念有了初步的区分,也为原子得失电子的规律埋下伏笔) 5.师生分析:(一边分析,一边板书) 6.引导提问:离子是怎样形成的?什么叫离子?如何区别阳离子和阴离子?离子符号的书写应与原子有什么不同? 四、小结练习,诱发思考 1.小结:在本课题,我们学了什么? 2.练习:课本习题。 3查看更多